[学习目标]1.了解理想气体的模型,并知道实际气体看成理想气体的条件。2.掌握理想气体状态方程的内容和表达式,并能应用方程解决实际问题(重难点)。3.能用气体分子动理论解释三个气体实验定律(重点)。
一、理想气体
1.理想气体:在温度、压强下都遵从气体实验定律的气体。
2.理想气体与实际气体
实际气体在温度不低于、压强不超过时,可以当成理想气体来处理。
3.从微观的角度看,理想气体的特点
(1)气体分子与分子间距离相比忽略不计。
(2)气体分子间的忽略不计。
(3)气体分子与器壁碰撞的忽略不计。
4.理想气体是对实际气体的一种科学抽象,是一种理想化模型,实际并不存在。
一定质量的理想气体的内能与什么因素有关?
________________________________________________________________________________________________________________________________________________________________________________________二、理想气体的状态方程
如图所示,一定质量的某种理想气体从状态A到B经历了一个等温过程,又从状态B到C经历了一个等容过程,请推导状态A的三个参量pA、VA、TA和状态C的三个参量pC、VC、TC之间的关系。
________________________________________________________________________________________________________________________________________________________________________________________
1.内容:一定的某种理想气体,在从一个状态(p1、V1、T1)变化到另一个状态(p2、V2、T2)时,压强p跟体积V的乘积与的比值保持不变。
2.表达式: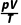 =C或
=C或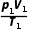 =
=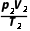 。
。
公式中常量C仅由气体的和决定,与状态参量(p、V、T)无关。
3.成立条件:一定的理想气体。
4.理想气体状态方程与气体实验定律的关系
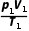 =
=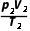 ⇒
⇒
例1(2024·郑州市高二月考)湖底温度为7 ℃,有一球形气泡从湖底升到水面(气体质量恒定)时,其直径扩大为原来的2倍。已知水面温度为27 ℃,大气压强p0=1×105 Pa,湖水的密度为1×103 kg/m3,g取10 m/s2,则湖水深度约为( )
A.65 mB.55 mC.45 mD.25 m
 例2 汽缸长为L=1 m(汽缸厚度可忽略不计),固定在水平面上,汽缸中有横截面积为S=100 cm2的光滑活塞(厚度不计)封闭了一定质量的理想气体,已知当温度为t=27 ℃,大气压强为p0=1×105 Pa时,气柱长为L0=0.4 m。现用水平拉力向右缓慢拉动活塞。
例2 汽缸长为L=1 m(汽缸厚度可忽略不计),固定在水平面上,汽缸中有横截面积为S=100 cm2的光滑活塞(厚度不计)封闭了一定质量的理想气体,已知当温度为t=27 ℃,大气压强为p0=1×105 Pa时,气柱长为L0=0.4 m。现用水平拉力向右缓慢拉动活塞。
(1)若拉动活塞过程中温度保持27 ℃,求活塞到达缸口时缸内气体压强;
(2)若汽缸、活塞绝热,拉动活塞到达缸口时拉力大小为500 N,求此时缸内气体温度。
________________________________________________________________________________________________________________________________________________________________________________________
应用理想气体状态方程解题的一般步骤
1.明确研究对象,即一定质量的理想气体;
2.确定气体在初、末状态的参量p1、V1、T1及p2、V2、T2;
3.由理想气体状态方程列式求解;
4.必要时讨论结果的合理性。
 例3内径较小且均匀的L形直角细玻璃管,一端封闭,一端开口竖直向上,用水银柱将一定质量的空气封存在封闭端内,空气柱长4 cm,水银柱高58 cm,进入封闭端水银柱长2 cm,如图所示,温度是87 ℃,大气压强为75 cmHg,求:
例3内径较小且均匀的L形直角细玻璃管,一端封闭,一端开口竖直向上,用水银柱将一定质量的空气封存在封闭端内,空气柱长4 cm,水银柱高58 cm,进入封闭端水银柱长2 cm,如图所示,温度是87 ℃,大气压强为75 cmHg,求:
(1)在如图所示位置空气柱的压强p1;
(2)在如图所示位置,要使空气柱的长度变为3 cm,温度必须降低到多少摄氏度?
________________________________________________________________________________________________________________________________________________________________________________________三、气体实验定律的微观解释
从微观角度来说,气体压强由什么因素决定?
________________________________________________________________________________________________________________________________________________________________________________________
1.玻意耳定律的微观解释
一定质量的某种理想气体,温度保持不变时,分子的不变。体积减小时,分子的数密度,单位时间内、单位面积上碰撞器壁的分子数就,气体的压强就。
2.盖—吕萨克定律的微观解释
一定质量的某种理想气体,温度升高时,分子的平均动能,只有气体的体积同时,使分子的数密度,才可能保持压强不变。
3.查理定律的微观解释
一定质量的某种理想气体,体积保持不变时,分子的数密度,温度升高时,分子的平均动能,气体的压强。
通过网盘分享的文件:【学生用书Word版文档】整书等6个文件
链接: https://pan.baidu.com/s/1WrqhWD388uzcm3Z1gXKHEA?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享