【学习笔记】关于生物刺激法(bio-stimulation)和生物强化法(bio-augmentation)MICP 的讨论
- 2026-03-14 14:49:26

图1. 关于“About calcium carbonate precipitation on sand biocementation” 文章的讨论
01
—
内容概述
越来越多的研究表明,本地尿素酶阳性细菌能够产生足够的生物胶结作用来增强土壤强度,而无需引入任何外来细菌(以下称为生物刺激MICP)(Jiang et al., 2020; Terzis and Laloui, 2019)。其达到的强度可与生物强化MICP处理相当甚至更高(Gomez et al., 2017)。本讨论聚焦于阐述与生物强化(引入外来细菌)相比,生物刺激MICP的优势。
(1)尿素酶阳性细菌在天然土壤中普遍存在。首先,原生尿素酶阳性菌能被轻易富集(enrichment)。尽管在恶劣的条件下(如贫瘠的营养条件),天然微生物群落可能较少,但由于原生尿素酶阳性菌与原生环境的适应性,仍可成功实现富集。考虑到原生尿素酶阳性菌在土体中无处不在,生物刺激适用于各种物体和环境条件。不过需要注意的是,需要对不同的自然环境设计特别的富集溶液。尽管生物刺激MICP法可以通过原位和异位富集菌种,不过原位富集是更优选的,因为其成本更低,这也是另一个与生物强化MICP相比更有优势的原因。
(2)外源细菌菌株在原生环境中的适应性不足。即使提高生物强化效果能通过不断提供喂养营养液被观察到,但是生物强化的效果是否归因于外加细菌还是富集的原生菌种,这一点有待考证。总体上来说,细菌在土壤中的存活和可适用性高度依赖于原生土壤环境参数(例如,温度、PH等等)。因此,添加的细菌必须能够在一个陌生的、可能非友好的外来环境保持活性稳定并且能够在土体空隙中自由移动。然而,与原生菌种相比,外来菌种是非常脆弱的竞争者因为他们对于原生环境更低的适应性。Graddy 等人(2018)的研究证实了外来菌在与原生菌种竞争营养物和生长机会中处于劣势(图2)。
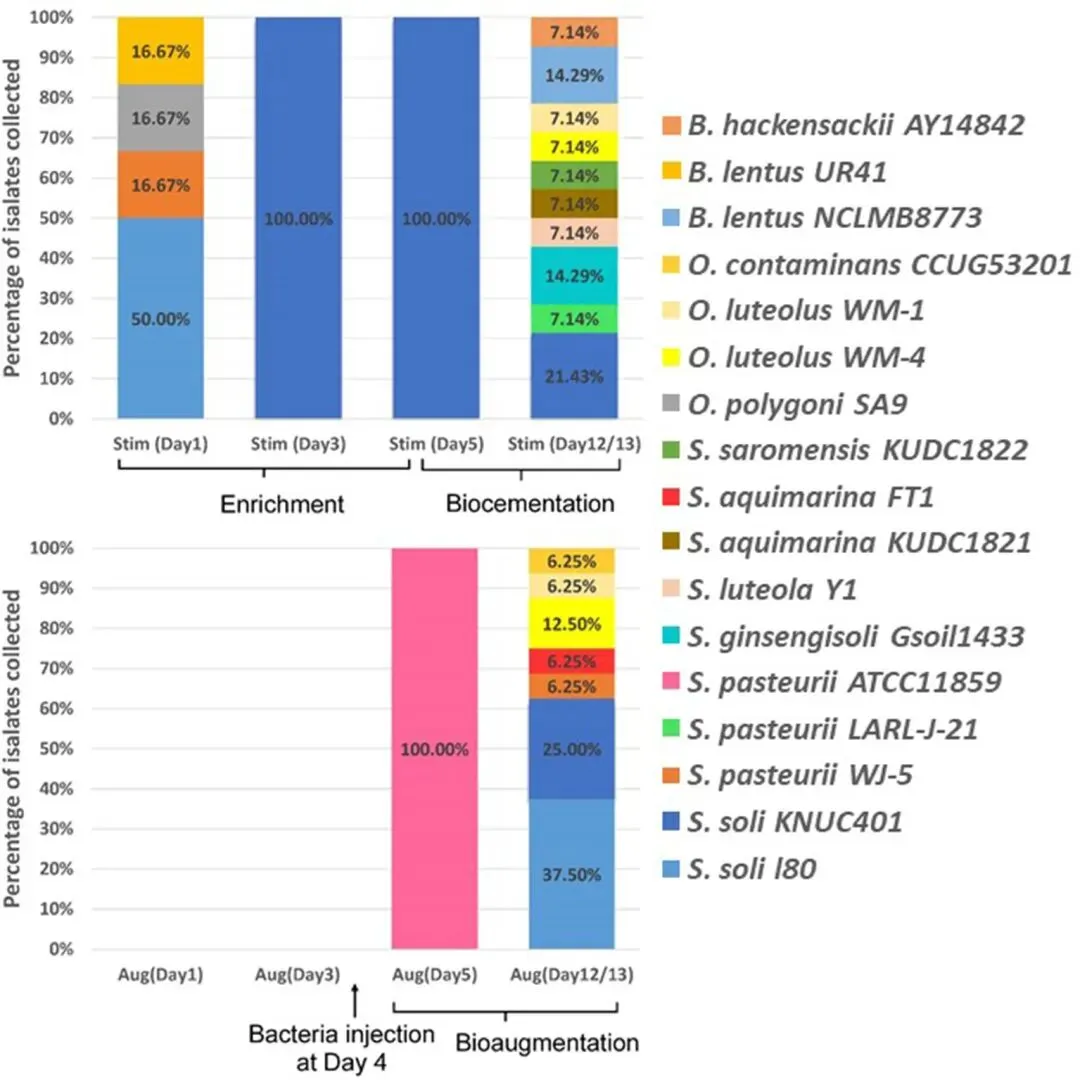
图2. 在生物刺激和生物强化MICP处理过程中尿素优势细菌在物种上的变化(Graddy et al. 2018)
(3)原位生物刺激MICP的稳健性。在生物修复领域,Davoodi等人通过异位(ex-situ)生物刺激MICP法,把合适的原生菌提取后注射回受污染的原生土体和水源。在土体加固领域,原位(in-situ)生物刺激法是更稳健的。在原位生物刺激的微生物增强固化处理过程中,无需对尿素酶阳性菌株进行测序和鉴定。实际上,根据Graddy等人(2018)的研究,在富集和生物固结阶段,尿素酶阳性菌株的种群数量和多样性可能发生剧烈变化(见图2)。因此追踪原位生物活化过程中的菌群变化意义有限。相反,通过监测整体土壤尿素降解活性(即尿素降解速率)即可有效控制生物活化MICP过程,该指标与生物固结程度存在显著相关性(Lee et al., 2019)。通过使用复合营养基替代简单营养基,并延长周期性施用时间,可显著提升尿素分解活性(Lee et al., 2019; Tsesarsky et al., 2017)。
本讨论讨论了生物刺激MICP的优势,但并不代表生物强化MICP是没有必要的。例如,生物强化MICP可能更适用于长期效果的处理措施。另外,值得提及的是,生物刺激和生物强化MICP具有共同的副作用:MICP会因氨氧化作用,导致土壤酸化并形成生物固结。
02
—
主要参考文献
Davoodi, S.M., Miri, S., Taheran, M., Brar, S.K., Galvez-Cloutier, R., Martel, R., 2020. Bioremediation of unconventional oil contaminated ecosystems under natural and assisted conditions: a review. Environ. Sci. Technol. 54 (4), 2054–2067.
Gomez, M.G., Anderson, C.M., Graddy, C.M.R., DeJong, J.T., Nelson, D.C., Ginn, T.R., 2017. Large-scale comparison of bioaugmentation and biostimulation approaches for biocementation of sands. J. Geotech. Geoenviron. 143 (5), 04016124.
Graddy, C.M.R., Gomez, M.G., Kline, L.M., Morrill, S.R., DeJong, J.T., Nelson, D.C., 2018. Diversity of Sporosarcina-like bacterial strains obtained from meter-scale augmented and stimulated biocementation experiments. Environ. Sci. Technol. 52 (7), 3997–4005.
Jiang, N.J., Tang, C.S., Hata, T., Courcelles, B., Dawoud, O., Singh, D.N., 2020. Biomediated soil improvement: the way forward. Soil Use Manag. 36 (2), 185–188.
Lee, M., Gomez, M.G., San Pablo, A.C.M., Kolbus, C.M., Graddy, C.M.R., DeJong, J.T., Nelson, D.C., 2019. Investigating ammonium by-product removal for ureolytic biocementation using meter-scale experiments. Sci. Rep. 9 (1), 1–15.
Tsesarsky, M., Gat, D., Ronen, Z., 2017. Biological aspects of microbial-induced calcite precipitation. Environ. Geotechnics 5 (2), 69–78.
