卵黄囊瘤是一种高度恶性的生殖细胞肿瘤,其命名源于其分化特点与胚胎发育早期的卵黄囊相似。卵黄囊瘤来源于原始生殖细胞,可发生于卵巢、睾丸或性腺外部位(如纵隔、骶尾部、腹膜后、颅内等)。本病以往被称为内胚窦瘤,但鉴于人类胚胎发育中并无内胚窦结构,这一名称不宜再继续使用。
【组织学起源】
卵黄囊瘤(Yolk Sac Tumor,YST)主要起源于原始生殖细胞,这是最常见的发生途径,主要有三种分化路径:①直接分化,原始生殖细胞在胚胎发育过程中,从卵黄囊壁迁移至生殖嵴(未来的卵巢或睾丸)的路径上发生“错位”或异常分化,直接向胚外结构(卵黄囊)方向分化形成肿瘤。②间接分化:由更具侵袭性的胚胎性癌细胞分化而来。胚胎性癌作为多潜能干细胞,可以向卵黄囊、绒毛膜或体细胞组织分化。③性腺母细胞瘤转化:在性腺发育不良(如46,XY女性)的患者中,性腺母细胞瘤内的生殖细胞成分可进一步恶变为卵黄囊瘤。
少数情况下卵黄囊瘤可起源于非生殖细胞的体细胞,通常见于中老年人,主要有两种分化路径:①逆向分化,已分化的体细胞在癌变过程中发生去分化,逆转为具有生殖细胞特性的干细胞状态,进而向卵黄囊结构分化。②异常化生,常与子宫内膜样癌、尿路上皮癌等体细胞癌共存,被认为是体细胞癌的一种罕见分化形式。
【临床流行病学特征】
卵黄囊瘤在所有恶性生殖细胞肿瘤中约占20%,在15岁以下儿童恶性肿瘤中占比约为3.5%,其中以0-3岁婴幼儿为发病高峰,尤其是睾丸卵黄囊瘤,中位年龄约1.5岁;而在15~19岁青少年中占比上升至16%。在青少年及青年中,中位发病年龄约为19-23岁。40岁以上患者极为罕见。但与体细胞肿瘤混合存在的卵黄囊瘤常见于40岁以上的患者。病变早期患者无特殊症状,卵巢来源的卵黄囊瘤最常见的临床症状为腹部包块、腹痛、腹胀及腹水,肿瘤扭转或破裂出血可引发急腹症。70%的肿瘤为临床I期,术前血清AFP水平几乎均有增高,甚至高达1000ng/ml以上(正常值<20ng/ml),因此AFP血清学检查对卵黄囊瘤诊断具有重要参考价值。
【大体病理学】
肿瘤多为单侧发生(约94.9%),右侧卵巢略多于左侧,双侧发病者多为晚期转移所致。肿瘤体积一般较大,直径为5~35cm不等(其中约70%的肿瘤直径超过15cm)。肿瘤呈圆形、卵圆形或分叶状,表面光滑,常有一层纤维性包膜,由于生长迅速,包膜常因张力过高而出现撕裂或与周围组织粘连。切面质软、实性或质脆、鱼肉状;由于肿瘤血供丰富且生长迅速,广泛出血和坏死极为常见,因此切面呈灰白、灰黄或灰粉的多彩状(图1),部分肿瘤伴有含粘稠胶冻样物质的囊性区,切面呈蜂窝状或海绵状外观。对侧卵巢常伴有成熟性囊性畸胎瘤。
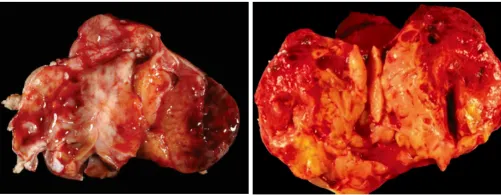
图1:大体图片,肿瘤表面光滑,可见包膜,切面呈囊实性,可见出血坏死(图片来源于网络)
【组织病理学】
卵黄囊瘤的组织学结构具有高度异质性,常以多种形态混合存在,以下是其核心亚型:
1.微囊/网型,是卵黄囊瘤最常见的生长方式,约68%以上的病例可见此结构。肿瘤细胞排列成疏松的网状或迷路样结构,背景为黏液样基质,内含大小不一的微囊或裂隙(图2),微囊和裂隙内衬扁平、多边形细胞,伴有大的泡状核,内有明显核仁。常可见嗜酸性透明小体(PAS染色阳性),为细胞内或细胞外的蛋白性沉积物,可作为诊断线索。
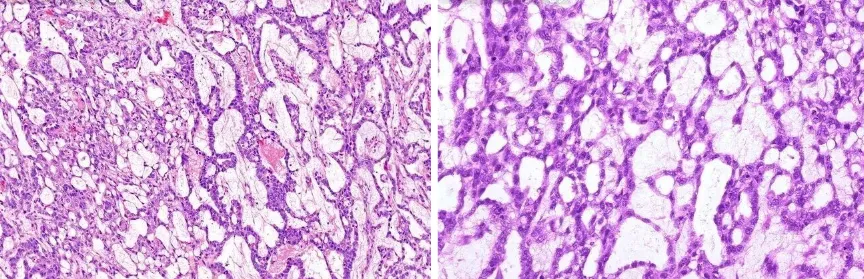
图2:微囊/网型,疏松的空泡状网状结构,伴有小囊或微囊,可以形成蜂窝状结构(图片来源于网络)
2.大囊型,常与微囊型共存,由大的、不规则的囊腔组成(图3)。
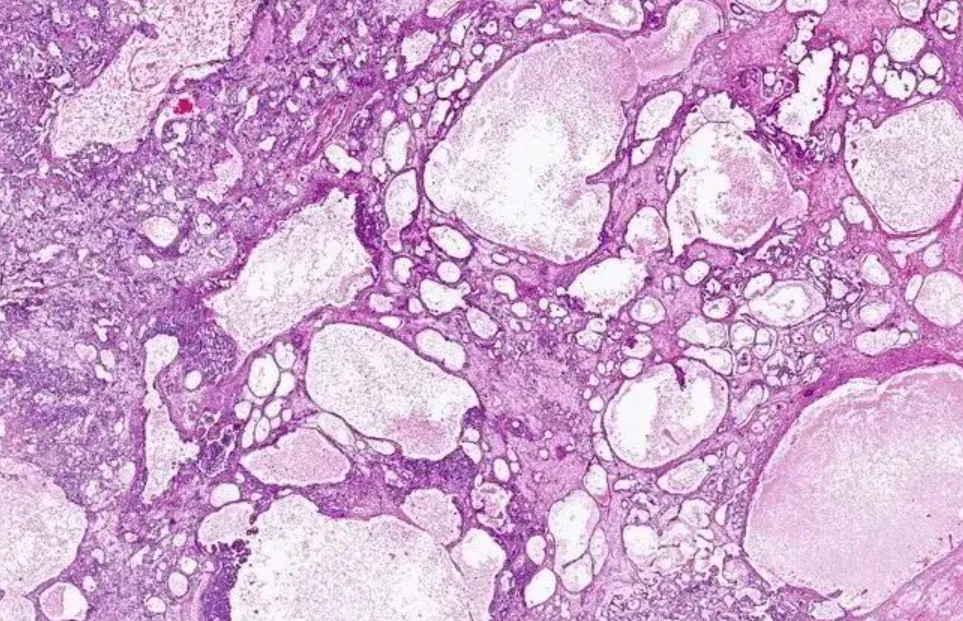
图3:大囊型,可见大的不规则囊腔(图片来源于网络)
3.内胚窦型,标志性结构为Schiller-Duval(S-D)小体,表现为乳头状结构,中央为纤维血管轴心,表面被覆单层立方或矮柱状、鞋钉样、核分裂活跃的上皮细胞(图4A,B)。S-D小体对卵黄囊瘤具有诊断价值,但并非所有病例都可见到,其典型结构仅见于1/3的肿瘤,因此当S-D小体不明显时,需注意肿瘤背景内是否存在由相互交通的腔隙和腺管组成的复杂迷宫样分支,即变异型S-D小体,也称为花彩型(festoon)S-D小体(图4C,D)。
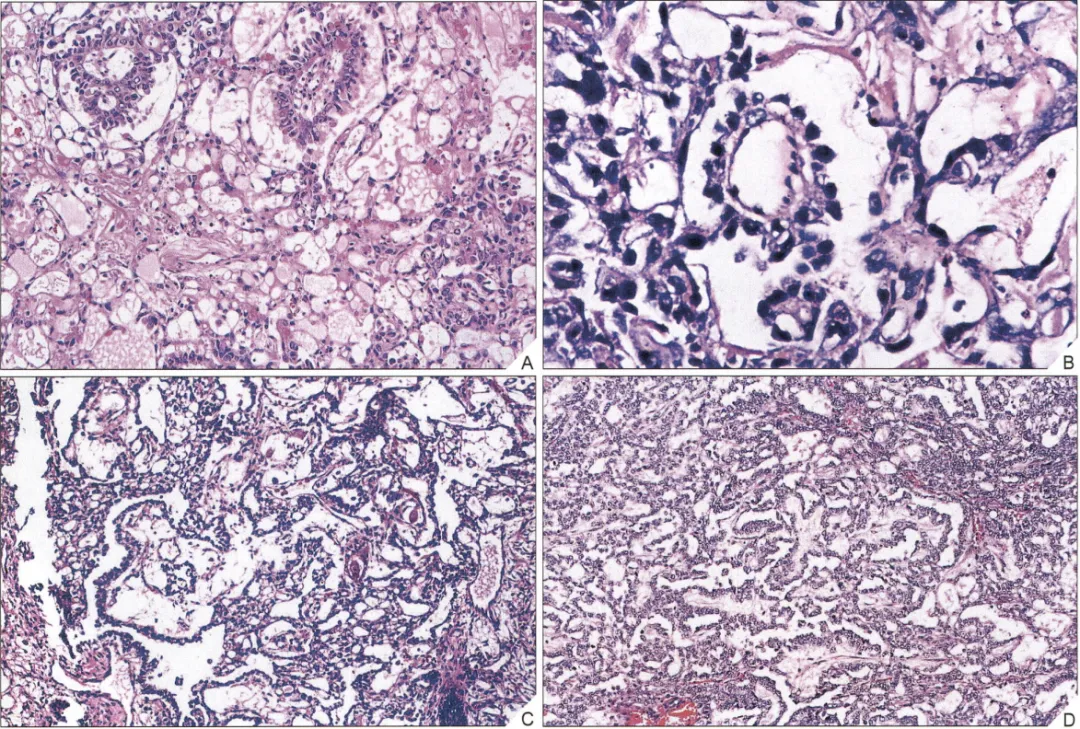
图4:内胚窦型,A、B为经典型S-D小体,C、D为变异型S-D小体(图片来自参考文献1)
4.黏液瘤样型,通常与微囊性型共存,可看到小的囊性间隙及腺样结构,衬扁平的肿瘤细胞,被丰富的黏液样基质包围,其中含有少量的星状、梭形、上皮样细胞(图5)。
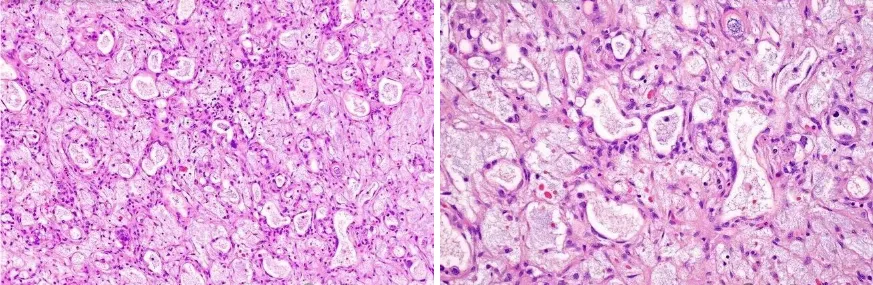
图5:黏液瘤样型,腺样结构和间质内有大量黏液样物质(图片来源于网络)
5.腺样/腺管型,肿瘤细胞主要有两种形态:一种呈子宫内膜样,常伴有明显的核下空泡,又称为内膜样型(图6A,B);另一种类似于早期发育的小肠或者肺泡,表现为单个腺体或相互吻合的腺体,偶尔可以出现筛状结构,甚至可见杯状细胞或潘氏细胞分化,周围间质有时可见类黏液样物质。
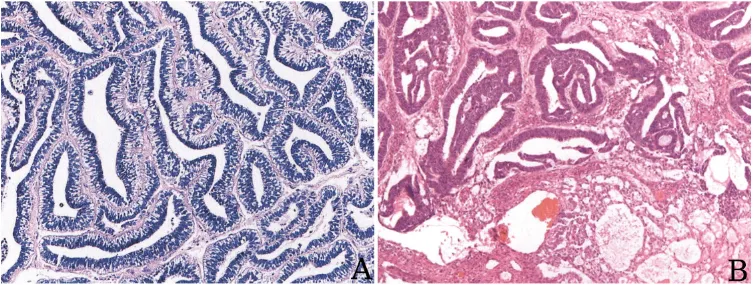
图6:腺样/腺管型,A,腺体呈分泌早期子宫内膜样改变,可见核下空泡;B,肿瘤由微囊型和腺样型混合组成(图片来源于参考文献1)。
6.多囊泡型,由许多大小不等的囊性结构组成,可见多个梨形、偏心或葫芦形的囊泡(与原始卵黄囊相似),囊泡内衬扁平细胞,周围围绕疏松或致密的梭形细胞间质(图7),肿瘤细胞呈扁平或柱状。
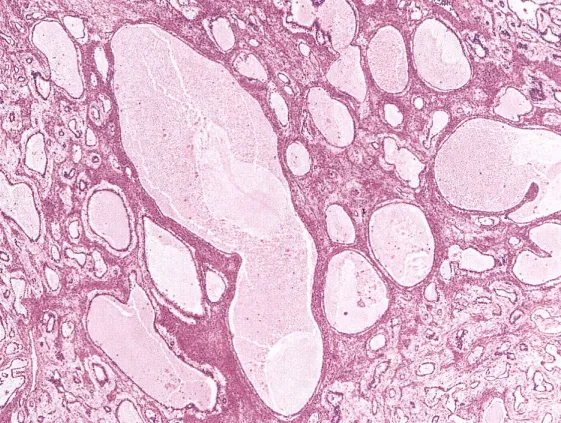
图7:多囊泡型,肿瘤具有大小不等的囊腔或囊泡(图片来源于参考文献1)
7.乳头型,乳头中央为纤维血管轴心,被覆于乳头表面的肿瘤细胞常有明显的异形性。(图8)。
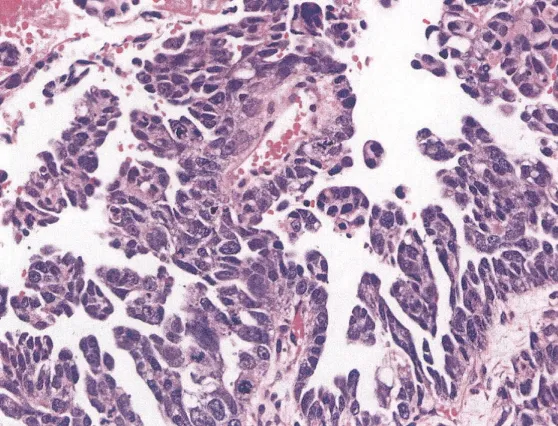
图8:乳头型,肿瘤具有显著的血管轴心,表面被覆有明显异型性的瘤细胞(图片来源于参考文献1)。
8.体壁型,很少见,但在转移或晚期复发化疗后的患者中相对常见,肿瘤细胞位于大量无定形的嗜酸性基底膜样物质中,这些基底膜样物PAS染色阳性,呈强折光性絮状、条索状或团块状物质,分布于瘤细胞或瘤巢外周及网状结构内(图9)。
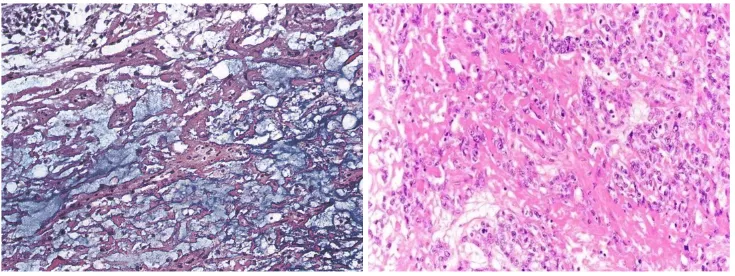
图9:体壁型,单个肿瘤细胞或肿瘤细胞群周围有大量的致密的嗜酸性基底膜物质(图片来源于参考文献1和网络)。
9.实性型,有胚芽样细胞和透明细胞两种,排列呈实性或片状(图10)。
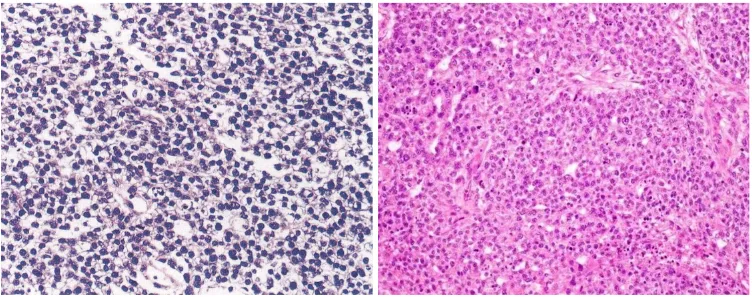
图10:实性型,肿瘤呈实性、片状生长,胞质透亮(图片来自参考文献1及网络)
10.肝样型,瘤细胞具有丰富的嗜酸性胞质,胞核呈空泡样,核仁明显,呈实性、巢状和片状分布,类似于肝细胞(图11)。
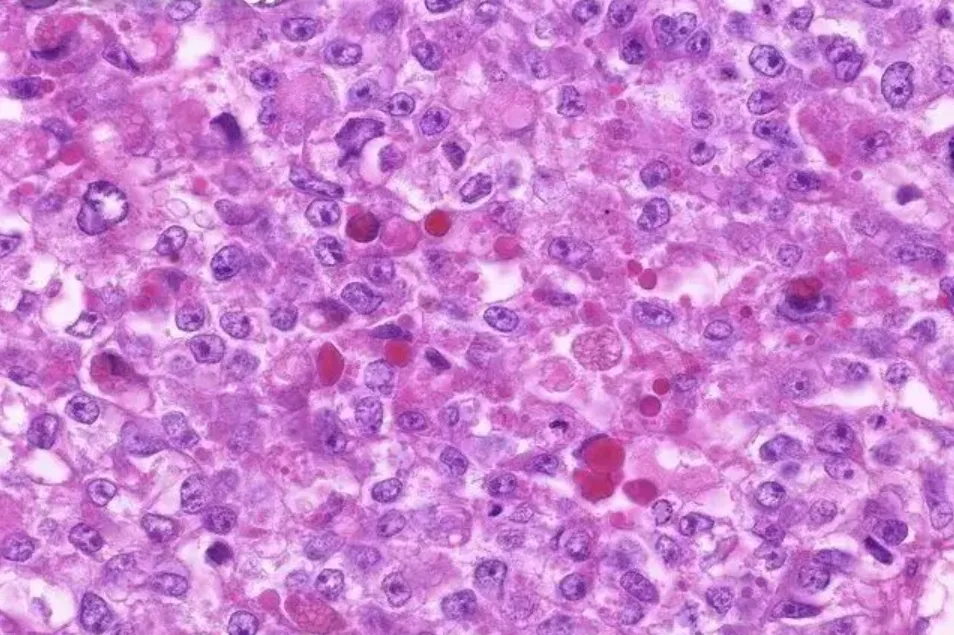
图11,肝样型,丰富的嗜酸性细胞质,空泡样核、突出的核仁,类似胎儿肝细胞
综合以上形态,S-D小体、基底膜样物质与透明(嗜酸)小体是卵黄囊瘤特征性的诊断线索。透明小体位于瘤细胞的胞质内或间质中,PAS及D-PAS染色均为阳性,且AFP及α1-抗胰蛋白酶免疫组化染色呈阳性反应。
【免疫组化】关于卵黄囊瘤的免疫组化见表1,
其中核心诊断组合:SALL4/LIN28 + AFP/GPC3 是诊断和确认卵黄囊瘤分化最常用、最可靠的免疫组化组合。
关键鉴别诊断:
vs. 胚胎性癌:卵黄囊瘤 OCT3/4阴性、CD30阴性,而胚胎性癌阳性。
vs. 透明细胞癌:卵黄囊瘤 EMA阴性、Napsin A阴性、GATA3阴性,而透明细胞癌常阳性;且卵黄囊瘤 SALL4、AFP、GPC3阳性。
vs. 间皮瘤:卵黄囊瘤 GATA3阴性、Calretinin阴性,而间皮瘤阳性;卵黄囊瘤生殖细胞标记(SALL4)阳性。
表1:卵黄囊瘤免疫组化标记物一览表
标记物名称 | 阳性表达部位 | 表达特点与诊断意义 | 备注/注意事项 |
AFP | 胞浆(弥漫或局灶) | 最经典、最特异的血清及组织学标记物。肝样细胞、内胚窦样结构(Schiller-Duval小体)、透明小体强阳性。阳性率>95%。 | 血清AFP水平常显著升高,是重要的临床监测指标。少数分化差的病例可能表达较弱。 |
SALL4 | 细胞核(弥漫强阳性) | 生殖细胞肿瘤广谱标记物。在卵黄囊瘤中几乎100%弥漫强阳性,敏感度极高。有助于确诊。 | 亦表达于无性细胞瘤、胚胎性癌等其他生殖细胞肿瘤,需结合其他标记物鉴别。 |
Glypican-3 | 胞浆/细胞膜 | 敏感且相对特异的标记物。在卵黄囊瘤中弥漫强阳性,阳性率约90-100%。在透明细胞癌中也可阳性。 | 与AFP相比,在实性、微囊等非典型结构中表达可能更稳定。 |
LIN28 | 胞浆(弥漫) | 与SALL4类似的广谱生殖细胞肿瘤标记物。在卵黄囊瘤中阳性率高,尤其在非典型形态中有价值。 | 表达模式与SALL4高度重叠,常联合使用以提高诊断可靠性。 |
CK(广谱) | 胞浆 | 阳性,提示上皮分化。在腺样、网状结构中表达明显。 | 特异性低,主要用于确认肿瘤的上皮特性。 |
OCT3/4 | 细胞核 | 通常为阴性。这是与胚胎性癌鉴别的关键点。胚胎性癌弥漫强阳性。 | 若阳性,需警惕混合有胚胎性癌成分。 |
CD30 | 细胞膜/高尔基区 | 通常为阴性。主要用于与胚胎性癌鉴别。胚胎性癌常阳性。 | 同上,是鉴别诊断的重要负向指标。 |
CD117 | 细胞膜 | 通常为阴性或局灶弱阳性。主要用于与无性细胞瘤鉴别。无性细胞瘤弥漫强阳性。 | 少数卵黄囊瘤可有局灶表达,需结合形态与其他标记。 |
hCG | 合体滋养层巨细胞 | 肿瘤内散在的合体滋养层巨细胞可阳性。 | 仅提示局灶滋养叶分化,不代表绒癌。卵黄囊瘤本身(体细胞)阴性。 |
GATA3 | 细胞核 | 通常阴性。有助于与 (卵巢/腹膜)间皮瘤 鉴别,后者常阳性。 | 在腺样卵黄囊瘤与间皮瘤形态相似时,此为关键鉴别点。 |
EMA | 细胞膜 | 通常为阴性。这是与各类癌(如子宫内膜样癌、透明细胞癌) 鉴别的关键。 | 绝大多数上皮性癌EMA阳性,而卵黄囊瘤阴性。此点非常重要。 |
Napsin A | 胞浆 | 通常为阴性。有助于与透明细胞癌鉴别,后者常阳性。 | 在透明细胞癌样形态的卵黄囊瘤中,此为关键鉴别标记。 |
【鉴别诊断】
1.透明细胞癌,这是最常见、最重要的鉴别诊断。透明细胞癌患者多为中年,常伴子宫内膜异位症,组织学主要表现为管囊状、乳头状、实性结构,胞浆透明或嗜酸,可见“靶样”透明小体。在免疫组化方面,透明细胞癌主要表现为EMA(膜+)、Napsin A(浆+)、HNF1β(核+)阳性,生殖细胞标记SALL4、AFP、GPC3阴性,EMA+强烈支持透明细胞癌,EMA-则需考虑卵黄囊瘤。
2.胚胎性癌,卵黄囊瘤和胚胎性癌常混合存在,二者均可呈实性生长和伴有透明的细胞质,但是胚胎性癌的细胞核较卵黄囊瘤细胞更大、核仁更明显,虽然卵黄囊瘤有时候细胞异型也会非常明显(如乳头型),胚胎性癌无S-D小体、嗜酸性基底膜样物质、肝样细胞及肠上皮分化。免疫组化,胚胎性癌OCT3/4(核+)、CD30(膜+)、SOX2(核+),AFP通常阴性或局灶+;卵黄囊瘤OCT3/4、CD30通常阴性,二者均可表达SALL4/LIN28,因此OCT3/4和CD30是鉴别核心。此外胚胎性癌血清HCG可轻度升高。
3.无性细胞瘤,无性细胞瘤的瘤细胞大、胞浆透明,细胞核位于中央,大而圆,核膜清楚,核染色质凝聚呈颗粒状,伴有1个或多个核仁,核分裂象易见,间质常见淋巴细胞浸润。肿瘤细胞与细胞核的大小及形态显著一致是无性细胞瘤的特点。实性生长的卵黄囊瘤可具有透明的细胞质,但卵黄囊瘤的细胞核缺乏多边形形态,很少为单一型生长方式且缺乏淋巴细胞浸润。免疫组化,无性细胞瘤OCT3/4(核+)、CD117(膜+)、D2-40(膜+),AFP、GPC3阴性。卵黄囊瘤OCT3/4、CD117通常阴性。
【治疗及预后】
卵黄囊瘤是可治愈的恶性肿瘤,治疗已非常标准化,核心是 “手术 + 以铂类为基础的联合化疗”。手术治疗的目标是全面确定分期(FIGO分期)并最大程度切除肿瘤,因患者绝大多数为年轻女性,强烈推荐并首选“保留生育功能的手术”,即仅切除患侧卵巢和输卵管,保留子宫及对侧正常卵巢。同时需进行大网膜切除、腹膜多点活检及淋巴结评估。除极少数完全切除的IA期患者可在严密监测下暂不化疗外,所有其他期别患者术后均必须接受辅助化疗。金标准方案为BEP方案(博来霉素+依托泊苷+顺铂),严密监测血清 AFP(甲胎蛋白) 水平,用于辅助诊断、评估化疗疗效以及监测是否复发。
卵巢卵黄囊瘤的总体预后极好,是妇科恶性肿瘤中治疗效果最显著的肿瘤之一,其5年生存率超过95%。其中,I期患者接近100%,即使是晚期(Ⅲ-IV期)患者,经过规范治疗,生存率也可达80-90%。
参考文献
1.郑文新、沈丹华、郭东辉等,《妇产科病理学第2版下卷》。
2.徐炼,王巍,何英等,四川大学学报,2018,49(4):680-682。
3.张娜,高燕,籍海虹等,卵巢卵黄囊瘤9例临床分析肿瘤预防与治疗2020年第5期。
4.佘祥东,卵巢卵黄囊瘤诊疗进展,国际妇产科学杂志2017年第2期。
审核:孙洁 教授 沈阳医学院附属中心医院病理科
编辑:远方

-END-
本公众号为非盈利性学术交流订阅号,大部分资料来源于大家自我创作、个人工作经验或学习体会,如涉及版权问题和学术问题请及时联系管理员处理;本公众号发布所有内容,版权均属本公众号所有。所有文章仅供公益交流。欢迎提供相关素材及资料或投稿等,投稿邮箱:1310214448@qq.com。欢迎个人形式转发或媒体、网站转载,后者请在文首注明「来源:金标准沙龙」。
