

第2课时 溶液的酸碱性与pH
[核心素养发展目标] 1.掌握溶液的酸碱性与pH的关系及检测溶液pH的方法。2.了解溶液pH调控的意义。3.能正确计算酸碱溶液的pH。
一、溶液的酸碱性与pH
1.25 ℃时,分析下列溶液中c(H+)和c(OH-)
| 纯水 | 0.1 mol·L-1 NaOH溶液 | 0.1 mol·L-1盐酸 |
c(H+)/ (mol·L-1) | | | |
c(OH-)/ (mol·L-1) | | | |
c(H+) 、c(OH-)的相对大小 | c(H+)c(OH-) | c(H+)c(OH-) | c(H+)c(OH-) |
溶液的酸碱性 | | | |
2.溶液的酸碱性与c(H+)、c(OH-)的关系
(1)任何水溶液中都有H+和OH-。
(2)溶液的酸碱性取决于溶液中c(H+)、c(OH-)的相对大小。
溶液的酸碱性(常温)酸性溶液:cH+ cOH- ,cH+>1×10-7 mol·L-1中性溶液:cH+ cOH-=1×10-7 mol·L-1碱性溶液:cH+ cOH-,cH+<1×10-7 mol·L-1
3.溶液的pH
(1)

(2)25 ℃时,溶液的pH与溶液酸碱性的关系:
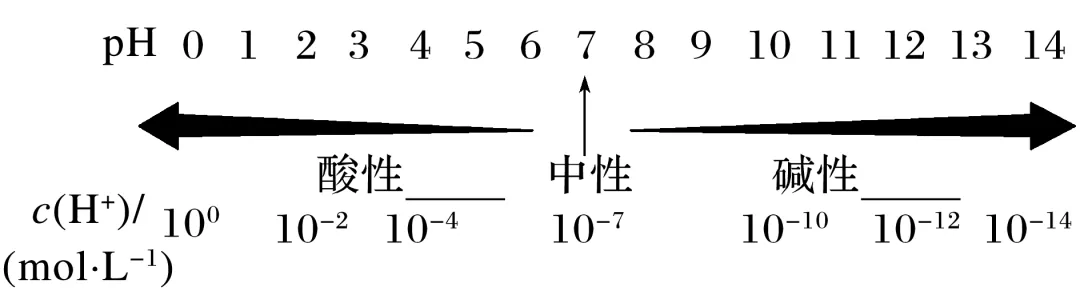
pH<7,为______溶液;pH=7,为______溶液;pH>7,为______溶液。

1.根据公式计算下列溶液的pH(常温),并比较其酸碱性的强弱。
(1)①c(H+)=1×10-5 mol·L-1溶液pH=________;
②0.001 mol·L-1的稀盐酸pH=______;
③0.005 mol·L-1的稀硫酸pH=______;
上述三种溶液酸性由强到弱的顺序:______________(填序号)。
(2)①c(H+)=1×10-9 mol·L-1的溶液pH=________;
②c(OH-)=1×10-4的溶液pH=______;
③0.001 mol·L-1的稀NaOH溶液pH=______;
上述三种溶液碱性由强到弱的顺序______________(填序号)。
2.pH=7的溶液一定呈中性吗?用pH判断溶液酸碱性时,要注意什么?
______________________________________________________________________________
______________________________________________________________________________
3.常温下pH=1的盐酸和pH=11的NaOH溶液由水电离出的c(H+)分别是多少?
______________________________________________________________________________
______________________________________________________________________________
4.25 ℃时,某溶液中由水电离出的c(H+)=1×10-12 mol·L-1,请探究该溶液的pH可能为多少?
______________________________________________________________________________
______________________________________________________________________________

计算酸碱溶液的pH
酸性:先求c(H+)―→pH(注意元数)
碱性:先求c(OH-)由Kwc(H+)―→pH
二、pH的测定和调控的意义
1.pH的测定
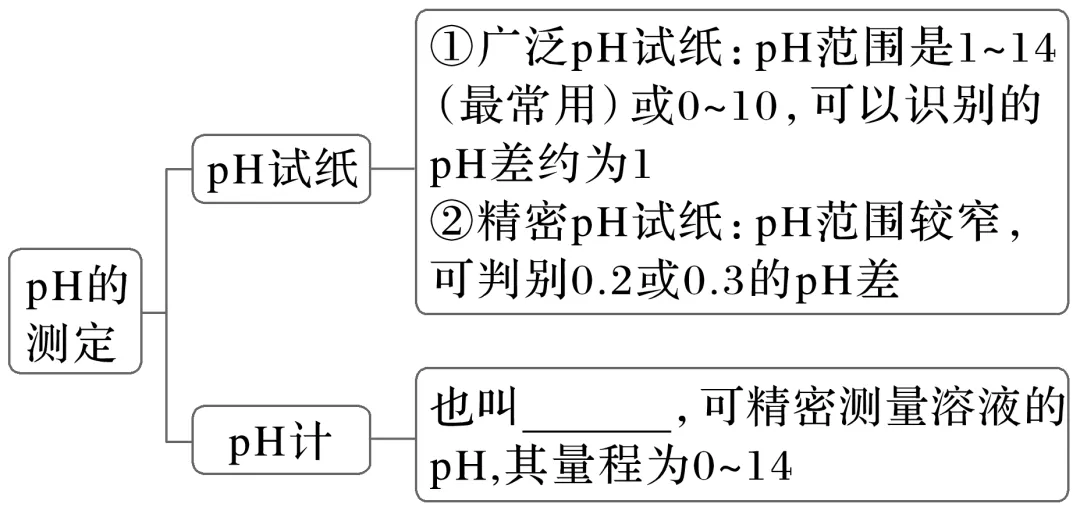
2.测定和调控溶液pH的应用
应用领域 | 实例 |
人体健康 | 人体各种体液都有一定的pH。当体内的酸碱平衡失调时,人体就表现出病变,因而可以利用检测血液的pH来诊断疾病 |
生活应用 | 利用护发素保护头发,就是通过调节头发的pH使之达到适宜的酸碱度 |
环保领域 | 酸性或碱性废水的处理,可以利用中和反应调节其pH |
农业生产 | 土壤的pH影响植物对不同形态养分的吸收及养分的有效性,不同作物生长对土壤的pH范围有不同的要求,因而应注意保持土壤的酸碱性 |
科学实验、 工业生产 | 溶液的pH控制常常是影响实验结果或产品质量、产量的一个重要因素 |

(1)使用pH试纸时应先将试纸润湿,然后再测定溶液的pH( )
(2)用广泛pH试纸测得某溶液的pH为3.4( )
(3)pH计是精确测定溶液pH的仪器( )

1.某同学为探究土壤的酸碱性做如下实验:常温下,向一定质量的土壤中加入一定体积的蒸馏水,充分搅拌后过滤,测量滤液的pH,再向滤液中滴加氨水,边滴加边测量溶液的pH,实验记录如表。下列说法不正确的是( )
加入氨水的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
溶液的pH | 4 | 4 | 4 | 4 | 6 | 8 | 10 | 10 | 10 |
A.滤液中由水电离出的c(H+)=1.0×10-10 mol·L-1
B.水的电离程度逐渐增大
C.所加氨水的pH=10
D.若Kb(NH3·H2O)=1.8×10-5,则氨水的浓度约为5.6×10-4 mol·L-1
2.(1)某盐酸由于长期放置,标签脱落,若确定其pH,用pH试纸测量的具体操作为________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
若使用时将试纸湿润,则测定结果如何变化?________。用湿润的pH试纸测量任何溶液一定有误差吗?______________________________________________________________
________________________________________________________________________。
(2)用广泛pH试纸测量溶液的pH时,记录的数据有何特点?
______________________________________________________________________________
______________________________________________________________________________
(3)是否可用pH试纸测定氯水的pH?简述理由。
______________________________________________________________________________
______________________________________________________________________________
三、溶液pH的简单计算
类型一 酸碱溶液的稀释
1.下列溶液被稀释后,计算所得溶液的pH(常温)
溶液稀释 | pH |
pH=3的稀盐酸加水稀释100倍 | |
pH=2的稀硫酸加水稀释100倍 | |
pH=11的NaOH溶液加水稀释10倍 | |
pH=12的Ba(OH)2溶液加水稀释10倍 | |
pH=5的稀盐酸加水稀释1 000倍 | |
pH=9的NaOH溶液加水稀释1 000倍 | |
2.(1)pH=3的醋酸加水稀释到原来的10倍,溶液的pH范围:________________。
(2)pH=12的氨水加水稀释到原来的10倍,溶液的pH范围:________________。

酸碱溶液稀释时pH变化规律(常温)
(1)强酸(或强碱)每稀释10倍,pH向7靠拢1个单位。
(2)弱酸(碱)每稀释10倍,pH向7靠拢不到1个单位。
(3)酸碱溶液无限稀释,pH只能接近7。
类型二 不同pH强酸与强酸(或强碱与强碱)混合
3.常温下,计算下列溶液混合后的pH。
(1)pH=3的盐酸与pH=5的硫酸溶液等体积混合后溶液的pH为________。
(2)pH=2的盐酸与pH=4的硫酸,若按1∶10的体积比混合(溶液体积变化忽略不计)。混合后溶液的pH为________。
(3)pH=10和pH=12的两种NaOH溶液等体积混合后溶液的pH为________。

(1)强酸与强酸混合(稀溶液体积变化忽略)
c混(H+)=c1H+·V1+c2H+·V2V1+V2,然后再求pH。
巧记:若pH之差≥2的两种强酸溶液等体积混合,可忽略较稀酸(pH较大者)提供的H+,相当于计算较浓的酸稀释1倍的pH。
(2)强碱与强碱混合(稀溶液体积变化忽略)
先计算c混(OH-)=c1OH-·V1+c2OH-·V2V1+V2,再求c混(H+)=Kwc混OH-,最后求pH。
巧记:若pH之差≥2的两种强碱溶液等体积混合,可忽略较稀碱(pH较小者)提供的OH-,相当于计算较浓的碱稀释1倍的pH。
类型三 中和反应后溶液的pH
4.0.015 mol·L-1的硫酸与0.01 mol·L-1的NaOH溶液等体积混合(体积变化忽略不计)后溶液的pH是____。
5.常温下,pH=12的NaOH溶液和pH=4的HCl溶液等体积混合(体积变化忽略不计)后溶液的pH为________。
6.常温下,将pH=3的盐酸与pH=12的氢氧化钠溶液按体积比为9∶1混合(体积变化忽略不计)后的pH=____________。

酸碱中和反应后pH计算的一般思路(常温)
恰好完全反应呈中性 | pH=7 |
酸过量 | c混(H+)=cH+V1-cOH-V2V1+V2⇒pH |

通过网盘分享的文件:同步PPT课件等3个文件
链接: https://pan.baidu.com/s/1WiBBQCVHpFgaci5JN4S3LA?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享