学习笔记 6-毒作用机制
- 2026-05-16 01:38:34
多数毒物发挥其对机体的毒作用至少经历4个过程:1. 从暴露部位转运到靶部位;2.终毒物与靶分子的反应;3.细胞功能障碍及导致的毒性;4.不适当的修复与适应。毒性机制涉及毒动学和毒效学各个阶段。
第一阶段-转运:从暴露部位到靶部位
1.1 吸收与毒物进入体循环前的排除
首过消除是毒物从暴露部位吸收进入体循环前的消除,涉及生物转化;主动转运;肝脏转化和排泄。
1.2 毒物分布及离开靶部位
从血循环进入靶部位(分布相)。多种因素促进和减少终毒物在其靶位点水平,如下表所示。
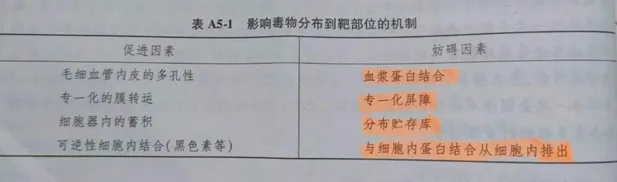
1.3. 排泄与重吸收
(1)排泄:肾,肾小球过滤,肾转运蛋白;肝:肝转运蛋白,肺:扩散
(2)重吸收:肾小管细胞重吸收,肠肝循环。
1.4 增毒和解毒
毒物在体内经生物转化为终毒物的过程称为增毒(toxication)作用。终毒物主要分为以下4类:亲电子剂、自由基、亲核剂和氧化还原反应物。
亲电子剂(electrophiles)
是指含一个缺电子原子的分子。亲电子剂带有部分或全部正电荷,容易与亲核物富含电子的原子共享电子对而发生反应。
亲电子代谢物的形成方式:
1.插入氧原子
2,形成共轭双键
3. 阳离子型亲电物通过键异裂形成
自由基(free radicals)
原子外轨道中含有一个或多个不成对电子的分子或分子片段。自由基通过接受或失去一个电子,或由化合物的共价键发生均裂而形成。
特点:顺磁性,化学性质十分活泼反应性极高,半减期极短。常见的自由基有:羟自由基、超氧阴离子自由基、过氧自由基等。
亲核剂 (nucleophiles)
亲核剂是毒物增毒作用较少见的机制。氰化物属于亲核剂。CO是二卤甲烷经过氧化脱卤作用形成的有毒代谢产物。
氧化还原反应物(redox-active reductants)
氧化还原反应物的生成有其特殊机制。比如能引起高铁血红蛋白的亚硝酸盐既可在小肠由硝酸盐经肠道细菌还原生成,也可由亚硝酸酯与谷胱甘肽反应生成。
解毒
消除或阻止终毒物生成的生物转化过程称为解毒(detoxication)。有时在毒物处置过程中,解毒代谢可与活化代谢竞争。毒物解毒作用通过多种途径实现,取决于毒物化学特征。
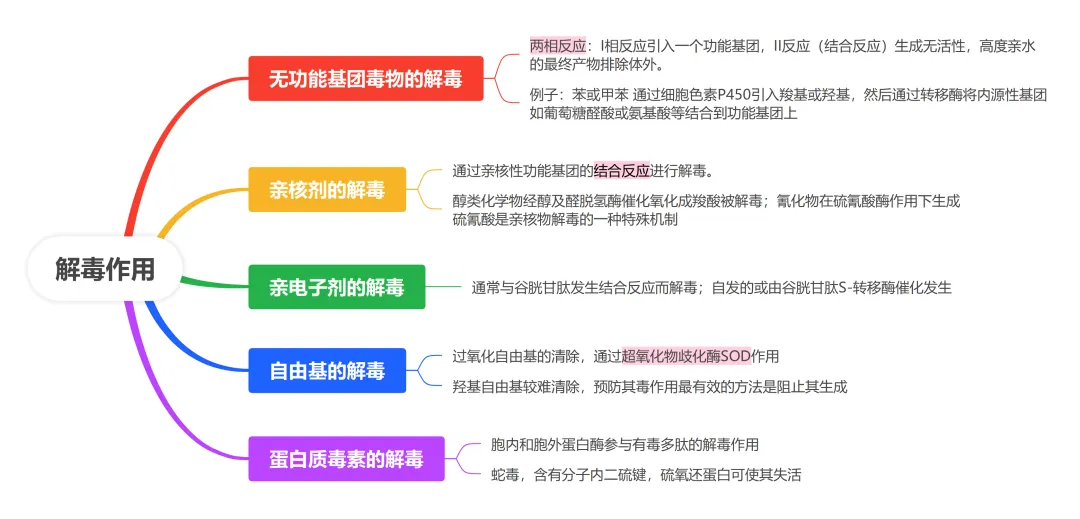
解毒过程失效原因有以下4种
1.毒物接触剂量超过机体解毒能力,引起解毒酶耗竭、共底物消耗或细胞抗氧化剂的耗竭
2.偶尔可见某种具有反应活性的毒物使解毒酶失活
3.某些结合反应可被逆转
4.解毒过程产生潜在有害副产物
第二阶段-终毒物与靶分子的反应
毒效应是终毒物与靶分子反应所介导的一系列继发生化事件,导致不同生物学水平(如靶分子本身、细胞器、细胞、组织和器官甚至整个机体)的结构损伤和功能异常。
2.1 靶分子属性
反应性、易接近性、关键功能。某种毒物引起毒性的靶分子,应证实满足3个标准:①终毒物与靶分子反应并对其功能产生不良影响;②终毒物在靶部位达到有效浓度(可达性);③
终毒物以所观察的毒性机制相关的方式改变靶分子。
2.2 终毒物与靶分子反应的5种类型
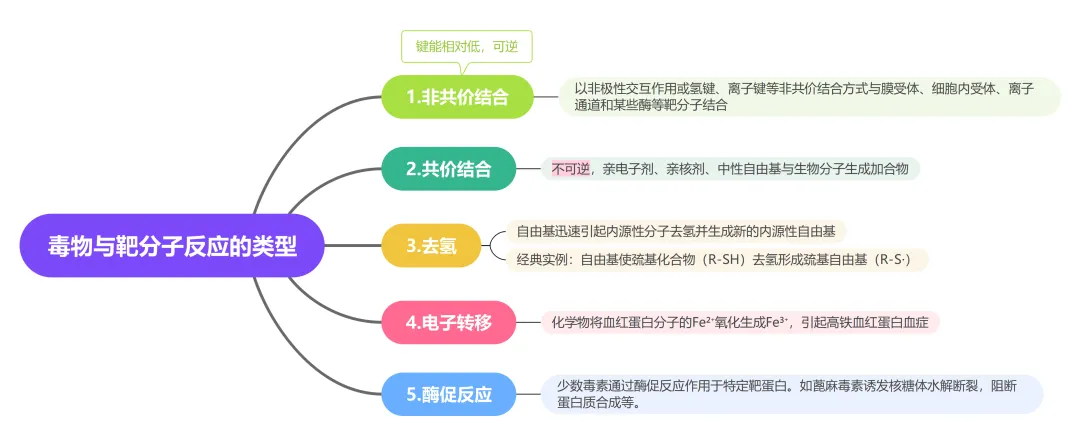
2.3 毒物对靶分子的影响
毒物对靶分子的影响主要包括两种机制:包括引起靶分子功能失调、破坏靶分子结构。
2.3.1 靶分子功能失调
有些毒物能模拟内源性配体并活化靶蛋白分子。比如吗啡能激活鸦片受体、河豚毒素能抑制神经元膜电压激活的钠通道开放等。一些毒物干扰DNA模板功能,如黄曲霉素氧化物与鸟嘌呤共价结合,导致G-A配对,诱发基因发生碱基置换突变
2.3.2 靶分子结构破坏
毒物通过与内源性分子形成加合物、发生交联和断裂而改变内源性分子的一级结构。
2.3.3新抗原形成
外源化学物及其代谢产物与生物大分子共价结合对多数个体免疫系统并不产生严重后果,单在少数个体可作为新抗原激发免疫应答。比如:青霉素本身可与蛋白质结合,引起免疫应答。
此外,还有非经靶分子反应引起的毒性:生物学环境的改变,①改变生物水相中H+离子浓度;②使细胞膜的脂质相发生物理化学改变;③占据位置或空间引起危害。
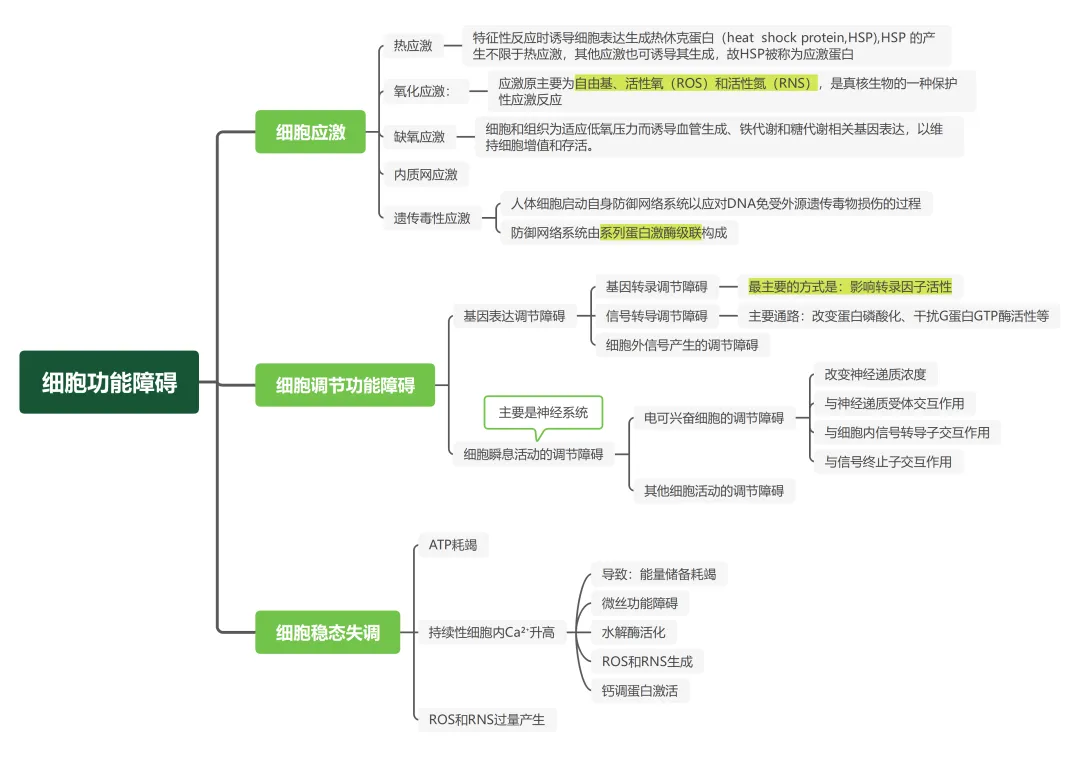
第三阶段-细胞调节功能障碍及导致的毒性
细胞功能障碍的发生也遵循一定的先后次序。通常细胞在受到外界有害刺激的情况下,首先会发生细胞应激;如果细胞损伤进一步加重,则引起细胞调节功能障碍,最终发展为细胞稳态失调,甚至出现细胞死亡。
如下图 细胞调节或维持功能的改变导致的毒效应
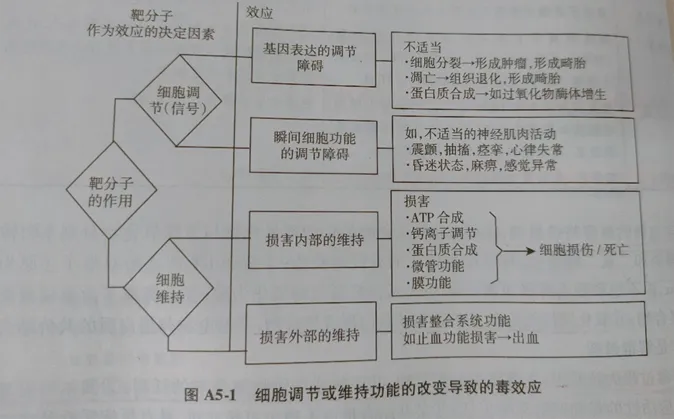
3.1细胞应激(cellular stress)
是细胞处于不利环境或遇到有害刺激时所产生的适应性反应,根据引起细胞应激的原因不同及应激反应的差异,分为热应激、缺氧应激、氧化应激、内质网应激和遗传毒性应激。
能导致细胞应激的物理、化学和生物因素称为应激原,包括DNA损伤性应激原和非DNA损伤性应激原。

3.2 细胞调节功能障碍
细胞受信号分子调节。信号分子通过受体将信号传递给基因调节区域和功能蛋白。受体包括细胞表面受体和核受体。细胞受体激活可导致①改变基因表达,增加或减少特定蛋白的功能;②特定蛋白发生化学修饰(如磷酸化、甲基化、乙酰化等),从而激活或抑制蛋白功能。
3.3 细胞维持的毒性改变(细胞稳态失调)
细胞稳态(cellular homeostasis)是指在神经、内分泌核免疫系统共同调节下,细胞内各种成分核生理功能保持相对稳定状态。生物膜完整性是维持细胞稳态的关键。
毒物通过启动如下三种机制引起细胞稳态失调:1.ATP耗竭;2.持续性细胞内Ca²⁺升高;3.ROS和RNS过量产生。
并非各自孤立事件,而是以多种方式相互作用,彼此放大。细胞稳态失调的后果是细胞损伤。
细胞损伤即由化学物或其他因素干扰正常细胞自稳态机制而产生的病理性过程。
在致死性损伤作用下,细胞经历致死前时相→不可复时点→死亡时相,细胞可发生凋亡、自噬和胀亡改变,病理学可统称为“坏死”。
自噬是经溶酶体介导对细胞内蛋白质和细胞器降解的过程,以稳定细胞内环境,维持细胞的存活。
细胞死亡的不同模式

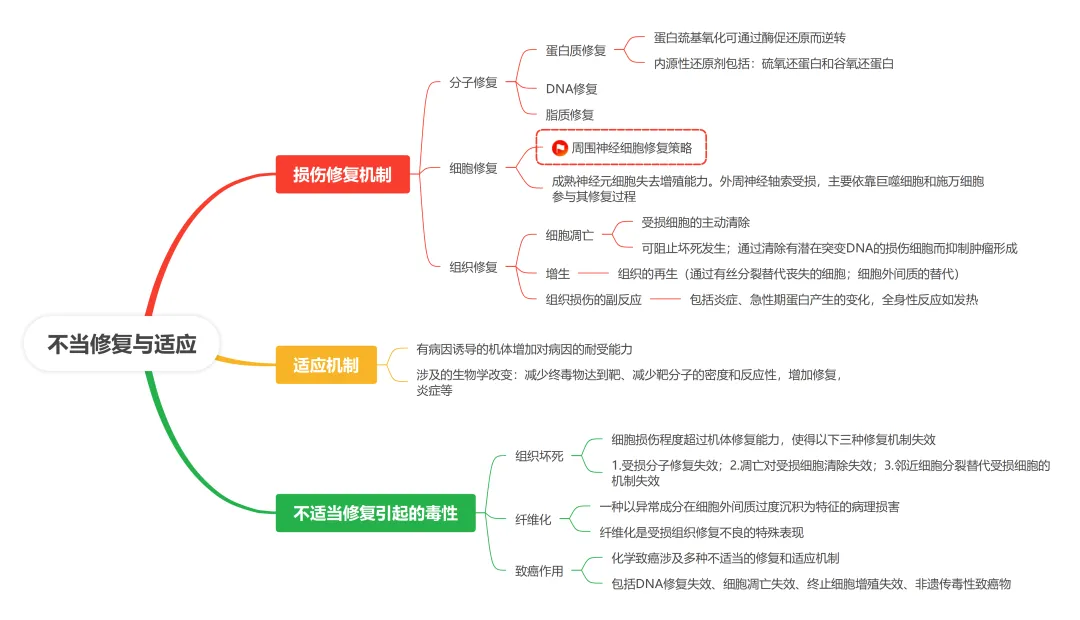
第四阶段 不当修复与适应

1.《现代毒理学简明教程》,周宗灿,付立杰,2012;
2.《毒理学基础》第7版,王心如,孙志伟,2017;
3.《毒理学教程》第三版,周宗灿,2006.
