
[核心素养发展目标]1.理解化学键的概念及化学反应的本质,培养“宏观辨识与微观探析”的核心素养。2.会识别微粒间作用力的类型,能判断物质变化过程中化学键的变化,培养“证据推理与模型认知”的核心素养。
一、化学键与分子间作用力
1.化学键
(1)概念:__________的原子之间__________的相互作用。
(2)分类
(3)化学反应的本质
①表象:反应物中的原子重新组合为产物分子。
②本质:__________的断裂和__________的形成。
③解释H2和Cl2反应过程
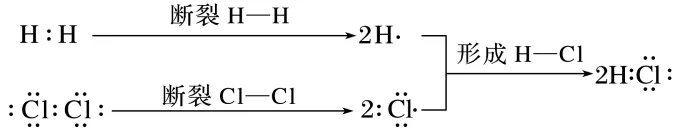
 思考1
思考1 有化学键断裂的过程一定是化学反应吗?有化学键形成的过程一定有新物质生成吗?
有化学键断裂的过程一定是化学反应吗?有化学键形成的过程一定有新物质生成吗?
2.分子间作用力
(1)分子间存在一种把__________在一起的作用力,叫做分子间作用力,最初又称__________。由分子构成的物质,其__________等物理性质主要由分子间作用力大小决定。
(2)分类:分子间作用力分为__________和__________。其中范德华力比化学键弱得多;氢键不是化学键,比化学键__________,比范德华力__________。
(3)分子间形成的氢键会使物质的熔点和沸点__________,水分子间的氢键可使其密度在固态时__________液态时的密度。
 思考2
思考2 “因为H2O分子间存在氢键,故H2O的稳定性强于H2S”这句话对吗?为什么?
“因为H2O分子间存在氢键,故H2O的稳定性强于H2S”这句话对吗?为什么?

1.判断正误
(1)NaHSO4中含有离子键、极性共价键与非极性共价键( )
(2)化学键既可存在于分子内的原子间,又可存在于分子之间( )
(3)稀有气体中不存在化学键( )
(4)两原子之间的相互作用叫做化学键( )
2.下列叙述正确的是( )
A.化学键是一种作用力
B.氯气中含离子键
C.离子键、共价键、分子间作用力均属于化学键
D.所有物质一定含有化学键
3.关于氢键及范德华力,下列说法正确的是( )
A.氢键比范德华力强,所以它属于化学键
B.分子间形成的氢键使物质的熔、沸点升高
C.沸点:HI>HBr>HCl>HF
D.H2O是一种稳定的化合物,这是由H2O之间形成氢键所致
4.下列各组物质中,含有的化学键类型完全相同的是( )
A.HI和NaIB.NaF和KOH
C.CO2和HClD.F2和NaBr
化学键与物质类型的关系
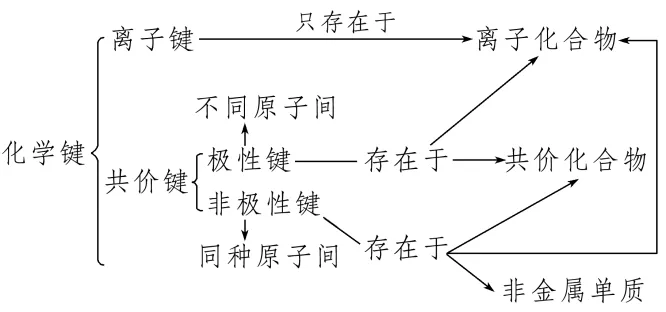
二、物质变化过程中化学键的变化
1.化学反应过程
(1)化学键的变化:化学反应过程包含反应物中化学键的断裂和生成物中化学键的形成,如H2+Cl2 2HCl。
2HCl。
(2)实质: 两过程不可分割
两过程不可分割
2.物质的溶解或熔化过程
(1)离子化合物的溶解或熔化的过程
离子化合物 电离
电离 阴、阳离子
阴、阳离子
如NaCl在水中或熔化时的电离:____________________。
注:一些特殊的离子化合物,可以和水发生反应,如Na2O2溶于水既有离子键又有共价键被破坏。
(2)共价化合物的溶解或熔化过程
①溶解过程
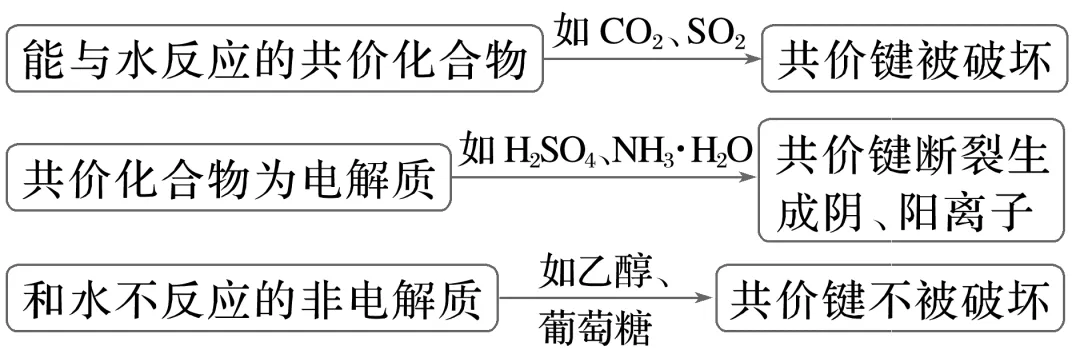
②熔化过程
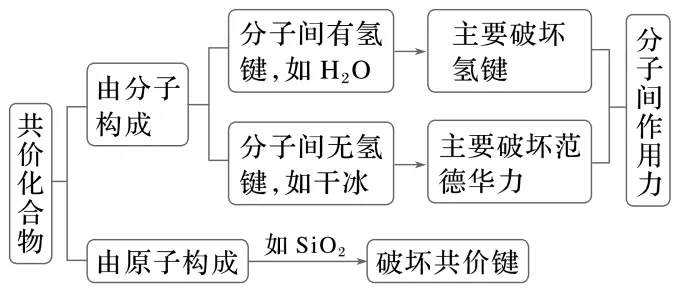
(3)单质的熔化或溶解过程
单质的特点 | 化学键变化 | 举例 |
由分子构成的固体单质 | 熔化或升华时只破坏范德华力,不破坏化学键 | P4的熔化,I2的升华等 |
由原子构成的单质 | 熔化时破坏共价键 | 金刚石、晶体硅等 |
能与水反应的某些活泼非金属单质 | 溶于水后,分子内共价键被破坏 | Cl2、F2等 |

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享