
[核心素养发展目标]1.依据化合价理论,结合实验探究,掌握Fe、Fe2+、Fe3+相互转化的途径,强化变化观念。
2.通过实验探究学会Fe2+、Fe3+的检验方法,培养证据推理意识,提升实验探究能力与创新意识。3.Fe2+与Fe3+的相互转化及鉴别。
一、铁盐、亚铁盐的性质与检验
常见的铁盐有___________、___________等,常见的亚铁盐有___________、___________等。
1.与KSCN溶液的反应——Fe3+的检验
(1)操作:
①FeCl3溶液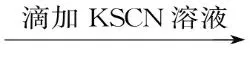 溶液变成___________色。
溶液变成___________色。
②FeCl2溶液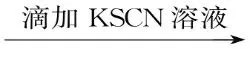 溶液___________色。
溶液___________色。
(2)原理:反应①的离子方程式为Fe3++3SCN- Fe(SCN)3。
Fe(SCN)3。
(3)结论:含有Fe3+的盐溶液遇到KSCN溶液时变成红色,利用这一反应检验Fe3+的存在。
2.实验探究Fe2+、Fe3+的性质
(1)从化合价角度预测Fe2+和Fe3+的性质
①Fe3+——能降低到___________价或___________价,具有___________。
②
(2)实验探究
①实验操作:
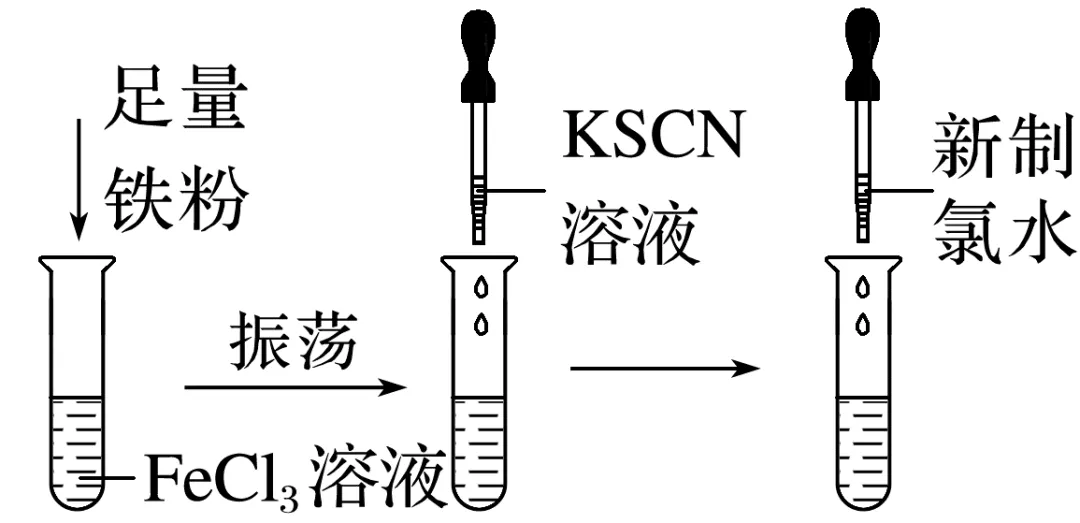
②实验现象:向FeCl3溶液中加入足量铁粉后溶液显___________色,试管中有黑色固体,再滴加KSCN溶液,溶液___________,向上层溶液中滴加新制氯水,溶液变___________色。
③离子方程式:______________________、______________________、______________________。
④实验结论:a.Fe3+具有氧化性,能被还原剂(如Fe)还原为Fe2+;b.Fe2+具有还原性,能被氧化剂(如氯气、过氧化氢等)氧化为Fe3+。
3.Fe2+、Fe3+的性质总结
 思考
思考 (1)实验室中久置的硫酸亚铁溶液会变黄的原因是。
(1)实验室中久置的硫酸亚铁溶液会变黄的原因是。
(2)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:。
(3)某化学小组检验铁的氧化物中是否有+2价铁时,设计思路为
少量固体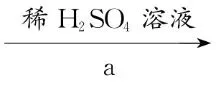 溶液
溶液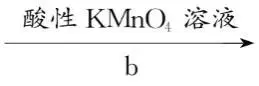 紫红色褪去。
紫红色褪去。
其中一位同学认为可以将步骤a中的稀硫酸换为稀盐酸,是否可以?
Fe2+、Fe3+的检验
(1)单一溶液中F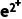 、F
、F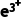 的检验
的检验
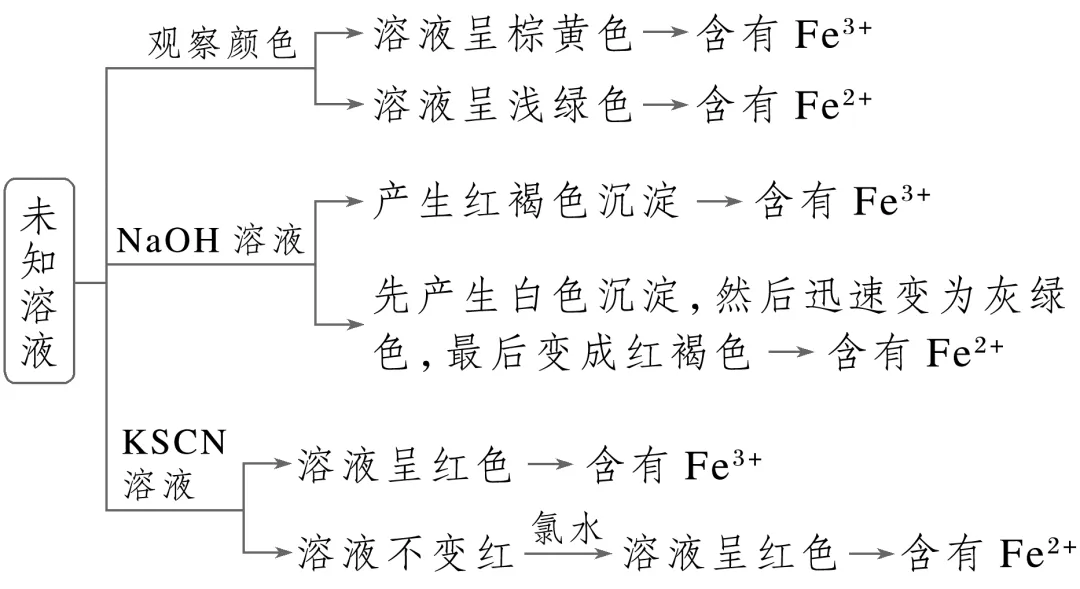
(2)混合溶液中Fe2+、Fe3+的检验
①检验Fe2+的方法
方法一:通常向溶液中滴加适量酸性KMnO4溶液,溶液紫红色褪去,说明含有Fe2+(注意:Cl-等还原性的离子对Fe2+的检验有干扰)。
方法二:向溶液中加入K3[Fe(CN)6]溶液,产生蓝色沉淀,说明含有Fe2+。
②检验Fe3+,可用KSCN试剂,现象为溶液变红。

1.判断正误
(1)向某溶液中先滴加氯水,后滴加KSCN溶液,溶液变红色,则原溶液中有Fe3+( )
(2)向FeCl3溶液中滴加KSCN溶液,出现红色沉淀( )
(3)向MCl2溶液中加入酸性KMnO4溶液,溶液褪色,则M2+为Fe2+( )
(4)向含有Fe2+的溶液中,滴加几滴H2O2溶液后溶液变成红色,说明溶液中一定有SCN-( )
2.现欲探究铁及其化合物的氧化性或还原性,可供选用的试剂有铁粉、FeCl3溶液、FeCl2溶液、氯水、H2O2溶液、锌片。下列叙述不正确的是( )
A.在FeCl2溶液中加入锌片,溶液逐渐由浅绿色变为无色
B.向FeCl2溶液中滴加氯水,溶液变为棕黄色,则Fe2+具有还原性
C.向FeCl2溶液中滴加少量酸化的H2O2溶液,溶液变为棕黄色,并产生大量无色气体
D.向FeCl3溶液中加入足量铁粉,溶液由棕黄色变为浅绿色,则Fe具有还原性
3.某同学为了检验家中的两种补铁药(成分均为FeSO4)是否变质,查阅了有关资料,得知SCN-、Fe2+能被酸性KMnO4溶液氧化而使酸性KMnO4溶液褪色,并结合已学的知识设计了如下实验:
①将药片除去糖衣研细后溶解、过滤。
②取滤液分别加入两支试管中,在一支试管中加入酸性KMnO4溶液,在另一支试管中加入KSCN溶液。
请回答下列问题:
(1)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液后不变红,结论是。
(2)若滴入酸性KMnO4溶液后不褪色,滴入KSCN溶液变红,结论是。
(3)若滴入酸性KMnO4溶液后褪色,滴入KSCN溶液变红,结论是。
(4)能不能将酸性KMnO4溶液和KSCN溶液滴入同一支试管中进行验证,原因是。
二、Fe及其化合物的“价—类”二维图及应用
1.铁元素的“价—类”二维图
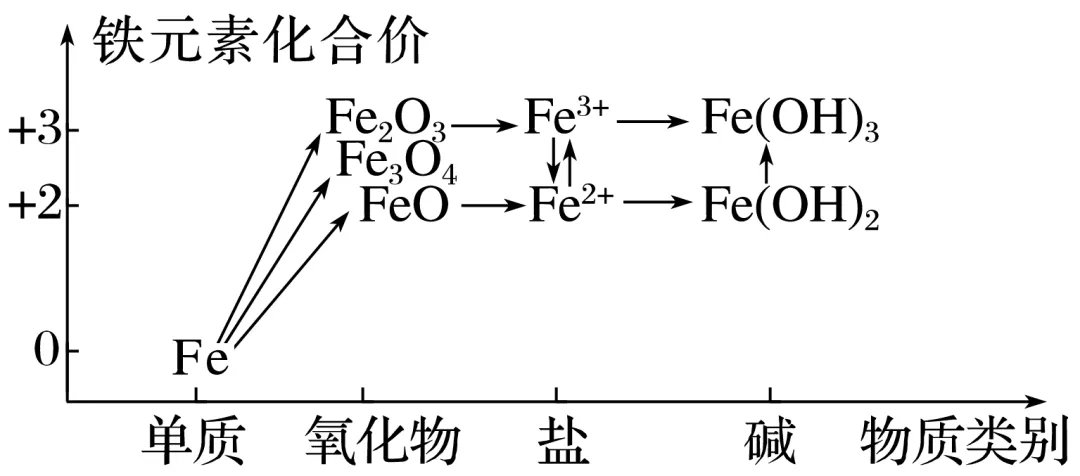
铁元素不同价态之间的转化需要通过氧化还原反应来实现,氧化剂、还原剂的强弱不同,转化产物也不同。

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享