
第1课时 物质的量 摩尔质量
[核心素养发展目标]1.了解物质的量及其单位、阿伏加德罗常数、摩尔质量的含义与应用,利用物质的量将宏观物理量与微观粒子的个数联系起来,并能从宏观和微观结合的视角分析解决问题。2.能从物质的量的角度认识物质的组成及变化,建立物质的量、物质的质量和微观粒子数之间计算的思维模型。
一、物质的量的单位——摩尔
1.物质的量
(1)物质的量是表示含有__________的集合体的物理量,用符号n表示。
(2)物质的量的单位——摩尔
(3)表示方法及含义
明确物质的量的规范表示
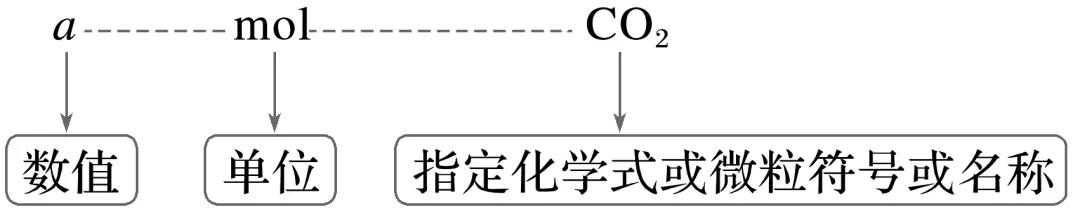
如1 mol H指1 mol__________,1 mol H2(氢气)指1 mol__________,不能说1 mol氢,指代不明确。
2.阿伏加德罗常数(NA)
特别提醒阿伏加德罗常数的单位为mol-1。
3.物质的量、阿伏加德罗常数与粒子数之间的关系
(1)关系式:n=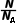 。
。
 思考1
思考1 通过下图可进一步认识水的组成,并理解物质的量与微粒数目的关系。
通过下图可进一步认识水的组成,并理解物质的量与微粒数目的关系。
 思考2
思考2 运用物质的量与微粒数目的关系,分析下列问题。
运用物质的量与微粒数目的关系,分析下列问题。
(1)1molCO2中有__________molC和__________molO,0.5molCO2中有__________molC和__________molO。__________molCO2含有0.5mol氧原子。
(2)1molNa2SO4中含有Na+的数目是__________,与__________molNaCl含有相同Na+数目。
(3)0.2molNH3与__________H2O中所含H原子数一样多。若用NA表示阿伏加德罗常数的值,0.3molH2O中含__________个电子。
(2)结论:微粒之间的物质的量之比等于微粒的__________之比。

1.判断正误
(1)物质的量可以理解为物质的数量( )
(2)1 mol任何粒子所含有的粒子数相等( )
(3)阿伏加德罗常数就是6.02×1023( )
(4)1 mol水中含有2 mol氢和1 mol氧( )
2.下列叙述正确的是( )
A.摩尔是表示物质所含微粒数量以及物质质量的具有双重意义的单位
B.摩尔是国际单位制中7个基本物理量之一
C.含有6.02×1023个氧原子的H3PO4的物质的量是0.25 mol
D.2H既可以表示2个氢原子又可以表示2 mol氢原子
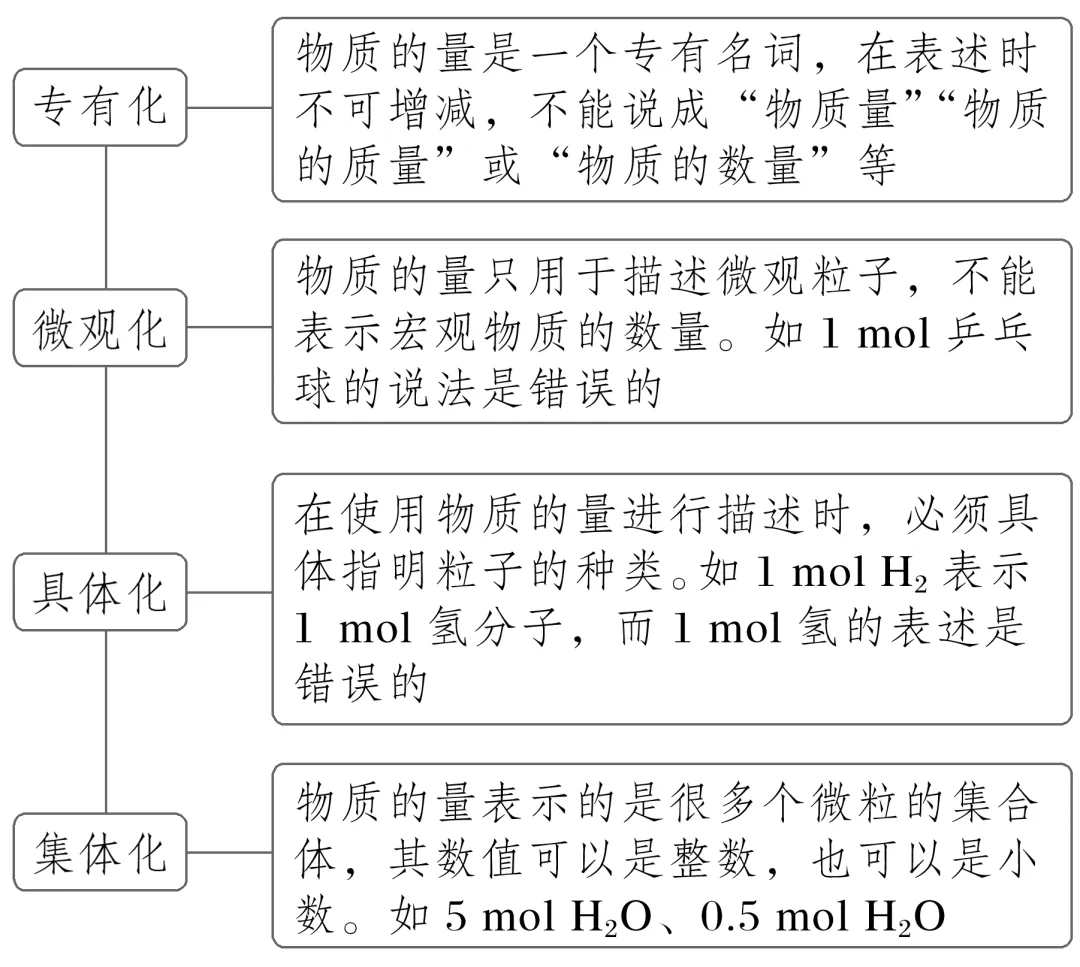
物质的量的理解——“四化”
二、摩尔质量
1.摩尔质量
2.物质的量(n)、质量(m)和摩尔质量(M)之间的关系
n=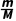 =__________。
=__________。
 思考1
思考1 摩尔质量与相对分子质量(或相对原子质量)是否等同,为什么?
摩尔质量与相对分子质量(或相对原子质量)是否等同,为什么?
 思考2
思考2 结合下列问题,总结摩尔质量的计算方法。
结合下列问题,总结摩尔质量的计算方法。
(1)已知氨气的相对分子质量为17,则氨气的摩尔质量为__________。
(2)1.28g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为__________。
(3)已知一个铁原子的质量为bg,则铁的摩尔质量为__________(用NA表示阿伏加德罗常数的值)。
(4)已知一个碳原子(12C)的质量为ag,1个某分子的质量为bg,则该分子的摩尔质量为__________。
前提条件 | 公式 |
任意状态的任意物质 | M=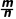 (定义式) (定义式) |

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享