化妆品大讲堂(花都):学习笔记
- 2026-05-02 07:29:01


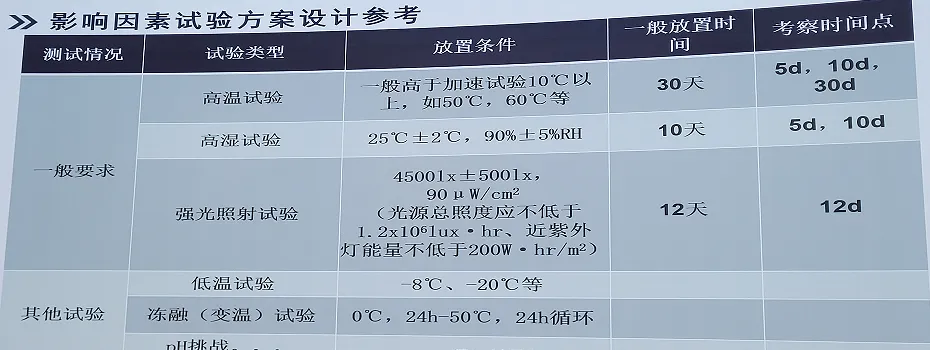
2. 影响因素试验方案设计参考
一般要求:
高温试验:一般高于加速试验10℃以上,如50℃、60℃等,一般放置30天,考察时间点5d、10d、30d。
高湿试验:25℃±2℃,90%±5%RH,一般放置10天,考察时间点5d、10d。
照光照射试验:4500 lx±500 lx,90 uW/cm2(光源总照度应不低于1.2×106 lux●hr,近紫外灯能量不低于200w●hr/m2),一般放置12天,考察时间点12d。

其它试验:
低温试验:-8℃、-20℃等
冻融(变温)试验:0℃,24h —— 50°C,24h循环。
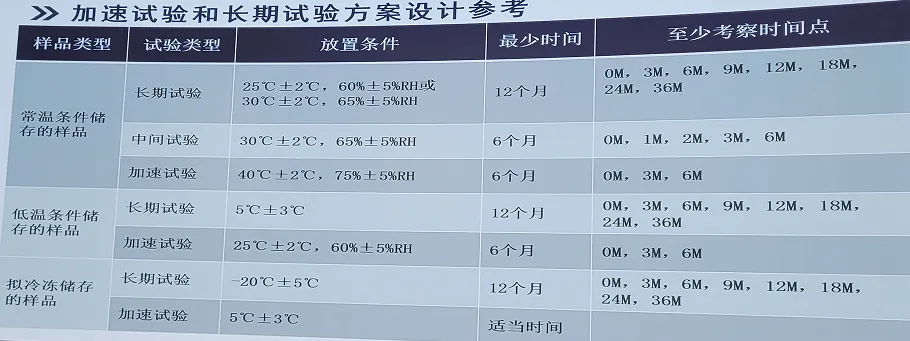
3. 加速试验和长期试验设计方案参考
常温条件储存的样品:
长期试验:25℃±2℃,60%±5%RH 或 30℃±2℃,65%±5%RH,最少时间12个月,至少考察时间点:0M,3M, 6M,9M,12M,18M,24M,36M。
中间试验:30℃±2℃,65%±5%RH,最少时间6个月,至少考察时间点:0M,1M, 2M,3M,6M。
加速试验:40℃±2℃,75%±5%RH,最少时间6个月,至少考察时间点:0M,3M,6M。
低温条件储存的样品:
长期试验:5℃±3℃,最少时间12个月,至少考察时间点:0M,3M, 6M,9M,12M,18M,24M,36M。
加速试验:25℃±2℃,60%±5%RH,最少时间6个月,至少考察时间点:0M,3M,6M。
拟冷冻储存的样品:
长期试验:-20℃±5℃,最少时间12个月,至少考察时间点:0M,3M, 6M,9M,12M,18M,24M,36M。
加速试验:5℃±3℃,适当时间。
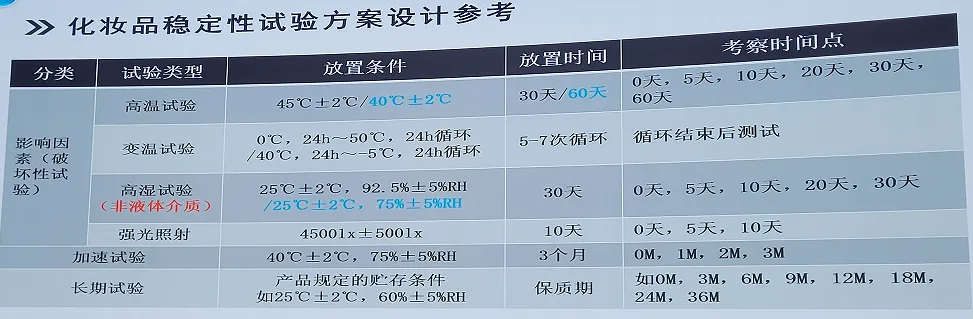
3. 化妆品稳定性试验设计方案参考
影响因素(破坏性试验):
高温试验:45℃±2℃/40℃±2℃,30天/60天,考察时间点:0天,5天,10天,20天,30天,60天。
变温试验:0℃,24h ~50℃,24h循环 或 40℃,24h~-5℃,24h循环,5~7次循环,循环结束后测试。
高湿试验(非液体介质):25℃±2℃,92.5%±5%RH 或 25℃±2℃,75%±5%RH,30天,考察时间点:0天,5天,10天,20天,30天。
强光照射:4500 lx±500 lx,10天,考察时间点:0天,5天,10天。
加速试验:40℃±2℃,75%±5%RH,3个月,考察时间点:0M,1M,2M,3M。
长期试验:产品规定的贮存条件,如25℃±2℃,60%±5%RH,放置时间为保质期,考察时间点:如0M,3M,6M,9M,12M, 18M,24M,36M。
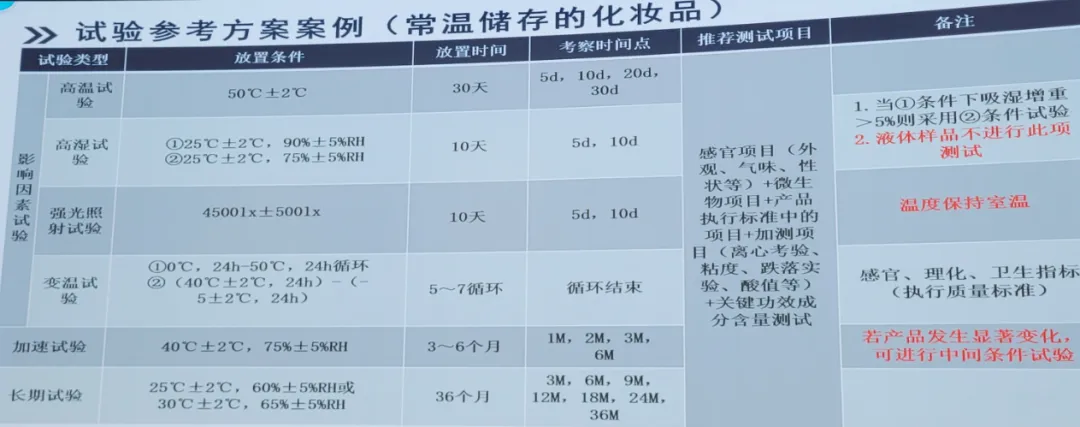
4. 常温储存化妆品试验方案案例
影响因素(破坏性试验):
高温试验:50℃±2℃,30天,考察时间点:0天,5天,10天,20天,30天。
高湿试验:25℃±2℃,90%±5%RH 或 25℃±2℃,75%±5%RH,10天,考察时间点:0天,5天,10天。
强光照射试验:4500 lx±500 lx,10天,考察时间点:0天,5天,10天。
变温试验:0℃,24h ~50℃,24h循环 或 40℃±2℃,24h~-5℃±2℃,24h循环,5~7次循环,循环结束后测试。
加速试验:40℃±2℃,75%±5%RH,3个月~6个月,考察时间点:0M,1M,2M,3M,6M。
长期试验:产品规定的贮存条件,如25℃±2℃,60%±5%RH 或 30±2℃,65%±5%RH,36个月,考察时间点:如0M,3M,6M,9M,12M, 18M,24M,36M。
5. 开启后使用期限测定(PAO)
目前可采用参考依据GB 27950-2020 《手消毒剂通用要求》
模拟场景:将成品样品开封,模拟日常使用(如每日开盖、用洁净勺取用两次)
监测节点:0天、1、3、6、9、12月等,按预设时间定方案。
关键项目:0天按照执行标准测试。其余时间点重点关注外观、气味及微生物指标,建议监测功效活性物含量变化。

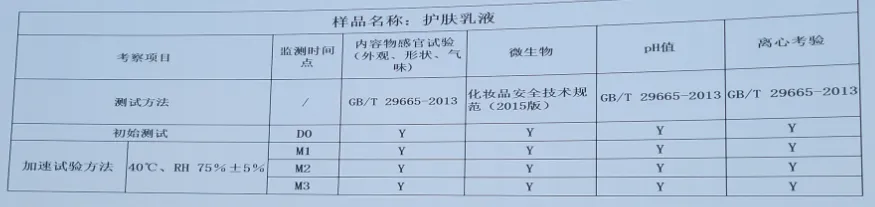
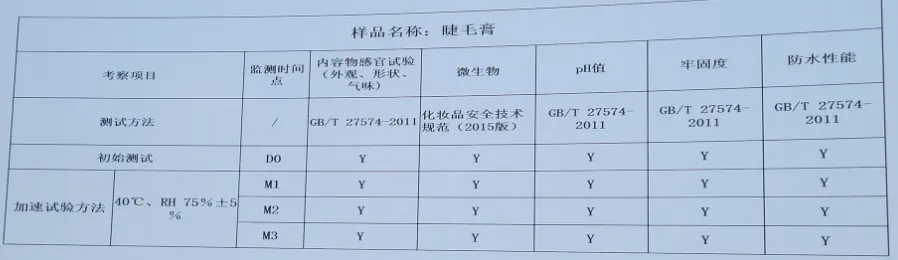
6. 包材相溶性测试案例
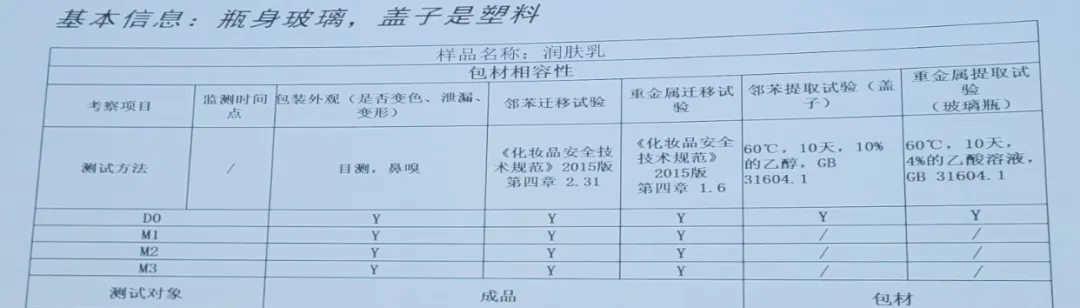
附:GB 27950-2020 《手消毒剂通用要求》之附录A (规范性附录) 产品启用后使用有效期检测方法
A.1 目的
观察手消毒剂产品启用后的使用有效期。
A.2适用范围
本检测方法适用于手消毒剂产品启用后使用有效期的检测。
A.3 试验器材
生物安全柜或洁净实验室(洁净度1000 级以上)、刻度吸管(1.0 mL、2.0 mL、5.0 mL)、稀释液、营养琼脂培养基、平皿、中和剂、电动混合器、含量检测仪器见相应的标准方法或《消毒技术规范》(2002年版)。
A.4 试验方法
A.4.1 选择有代表性房间(在医院或模拟医院条件)为试验房间。取3批次、每批3瓶共9瓶定型包装的消毒剂,置于试验房间内。每天按5个时间段使用5 次手消毒剂,每次时间间隔为1h左右,使用量与使用方法按产品使用说明书(当消毒剂余量不到10%时,停止采取样品),在0天、(T一30)天和T天(T为使用说明书的最长启用后的使用有效期)分别用2支灭菌试管进行无菌操作采取2mL,编号并填写采样记录,在4h 内送实验室检测。1 支样品用于检测细菌总数,另一支样品检测消毒剂有效成分含量。
A.4.2 在生物安全柜或洁净实验室内按GB15982规定检测细菌总数,结果取平均值;按消毒产品相应的标准或《消毒技术规范》(2002年版)检测有效成分含量,结果取平均值,计算有效成分下降率。
A.5 评价标准
A.5.1 手消毒剂启用后在使用有效期内有效成分含量下降率≤10%,且有效成分含量不低于说明书标示量的下限值,细菌总数≤100 CFU/mL,符合GB15982要求。
A.5.2 符合A.5.1 者为手消毒剂启用使用有效期合格,但在T 天时段以内任何一瓶样品的有效成分含量低于标示量的下限值或细菌总数>100CFU/mL时,即终止试验并判定使用有效期不合格,T天不合格而(T一30)天合格,该产品启用后使用有效期为(T一30)天。
A.6 注意事项
A.6.1 当试验样品余量少于 10%时,不再采取样品检测。
A.6.2 采样要注意无菌操作;试验应使用经检定和校准的仪器设备及灭菌合格的试剂和器材。
A.6.3 应避免样品暴晒;使用时应避免手触摸消毒剂出液口处、拧开消毒剂出液头和暴露消毒液。
关联阅读:
GB/T 16294-2025医药工业洁净室(区)沉降菌的测试方法 学习笔记
《化妆品监管协作区域实施化妆品生产质量管理规范若干问题共识(征求意见稿)学习笔记
蜗牛声明:
1. 引用信息来源为公开资料,如有侵权,请联系删除。
2. 文章观点仅为行业学术交流,不作经营决策等用。
3.未经同意,请勿转载。

