学习笔记(21):子宫内膜癌免疫治疗全景图
- 2026-06-01 20:04:40


子宫内膜癌是全球发病率持续上升的妇科恶性肿瘤之一,尤其在绝经后女性中更为常见。尽管分子分型和免疫检查点抑制剂的应用已显著改变晚期和复发患者的治疗格局,但不同分子亚型对免疫治疗的反应差异、联合策略的选择及耐药机制仍是亟待解决的临床难题。
2026年1月,Frontiers in Immunology 1发表综述Immunotherapy in endometrial cancer: mechanisms, clinical evidence, and future directions 2,系统梳理了子宫内膜癌免疫治疗的分子机制、关键临床证据及未来发展方向,为优化治疗策略和推动精准免疫治疗提供了重要参考。

分子分型及其对内膜癌免疫治疗的影响
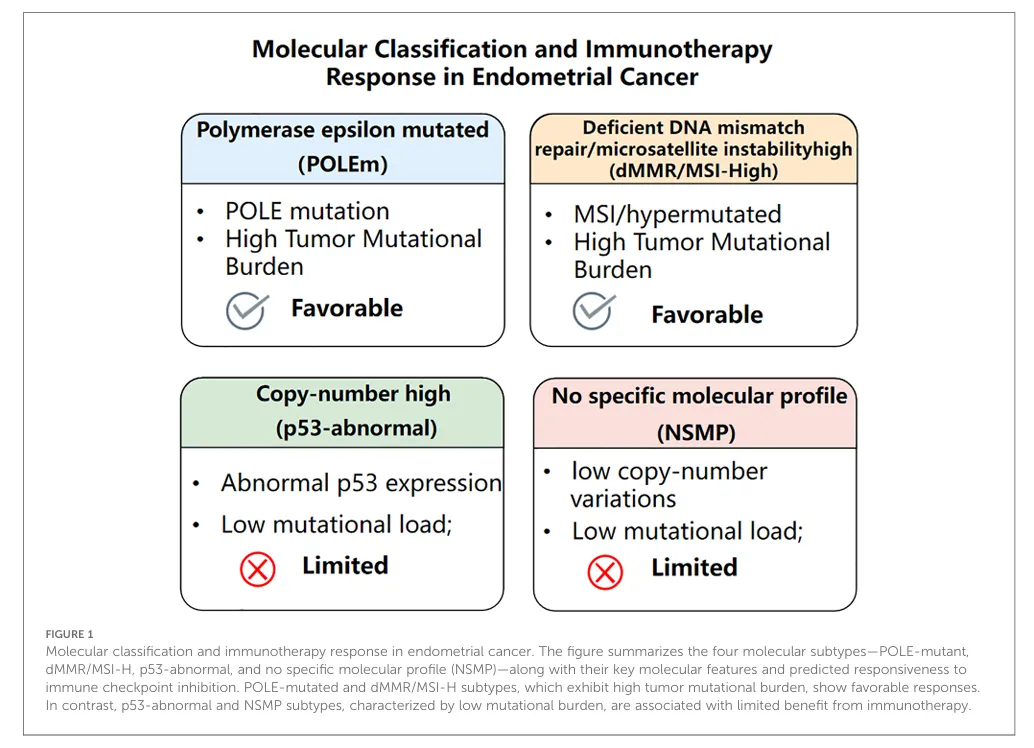
TCGA建立的子宫内膜癌分子分型为免疫治疗提供了重要的精准分层依据。
POLE突变型和 dMMR/MSI‑H 型肿瘤具有高突变负荷和显著免疫激活特征,对免疫检查点抑制剂最为敏感;
而 p53异常型和 NSMP 型通常呈免疫“冷”状态,对单药免疫治疗反应有限,更可能受益于联合策略。
总体而言,分子分型不仅揭示了不同亚型的免疫生物学差异,也为患者筛选和个体化免疫治疗方案的制定奠定了基础。
子宫内膜癌的免疫治疗:作用机制与治疗策略
免疫治疗已成为子宫内膜癌治疗的重要方向,当前策略涵盖免疫检查点抑制、免疫联合靶向治疗及新兴细胞治疗。不同治疗方式针对肿瘤免疫逃逸的不同环节,在特定分子亚型中展现出差异化疗效。
1.PD‑1/PD‑L1 通路阻断
PD‑1/PD‑L1抑制剂通过解除T细胞抑制恢复抗肿瘤免疫,是目前子宫内膜癌免疫治疗的核心手段。
dMMR/MSI‑H肿瘤因高突变负荷和免疫活化,对PD‑1抑制剂高度敏感。多项Ⅲ期研究(RUBY、NRG‑GY018)证实,PD‑1抑制剂联合化疗在一线治疗中显著改善无进展生存期,确立了该策略在dMMR/MSI‑H人群中的标准地位;而在pMMR肿瘤中,单药疗效有限。
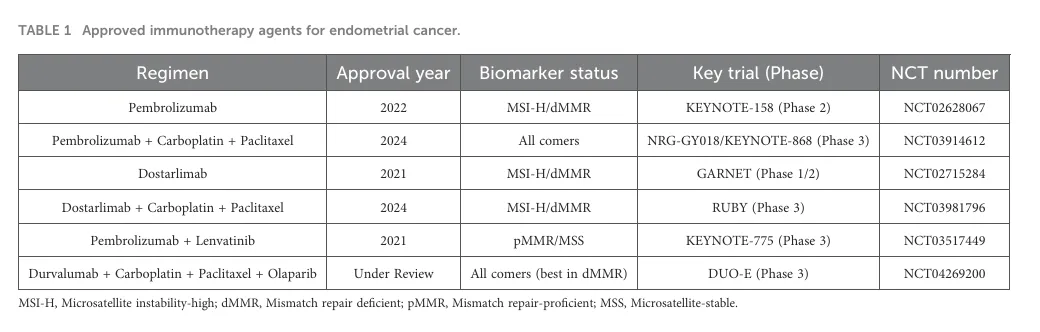
表1总结了支持这些药物获批的关键注册性临床试验。
2. 免疫检查点抑制剂与靶向治疗的联合
针对pMMR子宫内膜癌免疫耐受的问题,免疫治疗与靶向药物联合成为关键突破方向。帕博利珠单抗联合仑伐替尼在复发/转移期显著改善生存结局,尤其惠及pMMR患者。
此外,靶向DNA损伤修复通路、EphA2等分子并联合免疫治疗,有望通过增强免疫原性和抑制肿瘤生存信号,实现协同抗肿瘤效应。
3. 细胞治疗策略
细胞免疫治疗为晚期或耐药子宫内膜癌提供了新的探索方向。CAR‑T、CAR‑巨噬细胞、TIL治疗、NK细胞及TCR工程化T细胞等策略正在早期研究或临床试验阶段。
尽管面临抗原异质性和免疫抑制微环境等挑战,通过多靶点设计、结构优化及与免疫检查点抑制剂联合,细胞治疗在未来子宫内膜癌治疗中的角色值得期待。
临床证据与已获批治疗方案
免疫检查点抑制剂凭借明确的临床获益,已被正式纳入晚期子宫内膜癌的标准治疗体系。除已获批方案外,双免疫检查点阻断、免疫联合靶向治疗、抗体‑药物偶联物以及治疗性疫苗和细胞治疗等新策略正在快速推进,多项Ⅲ期研究正在进行,标志着子宫内膜癌免疫治疗正迈向更加多元化和个体化的阶段。
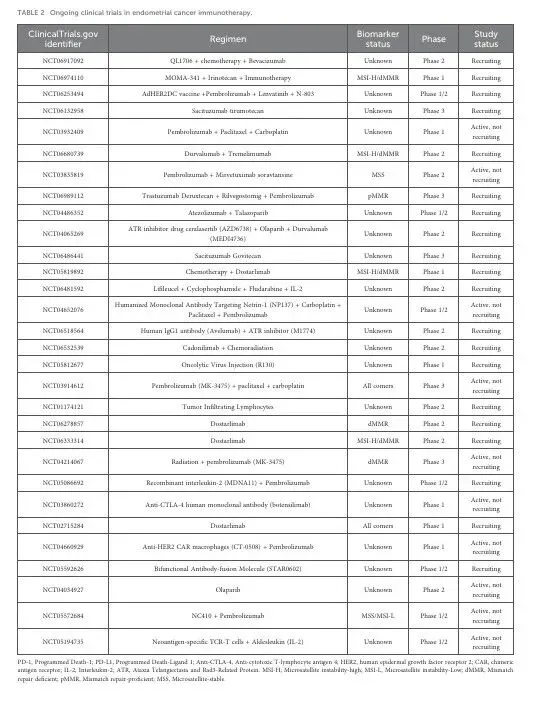
表2.子宫内膜癌免疫治疗的在研临床试验
子宫内膜癌免疫治疗的转化进展与未来方向
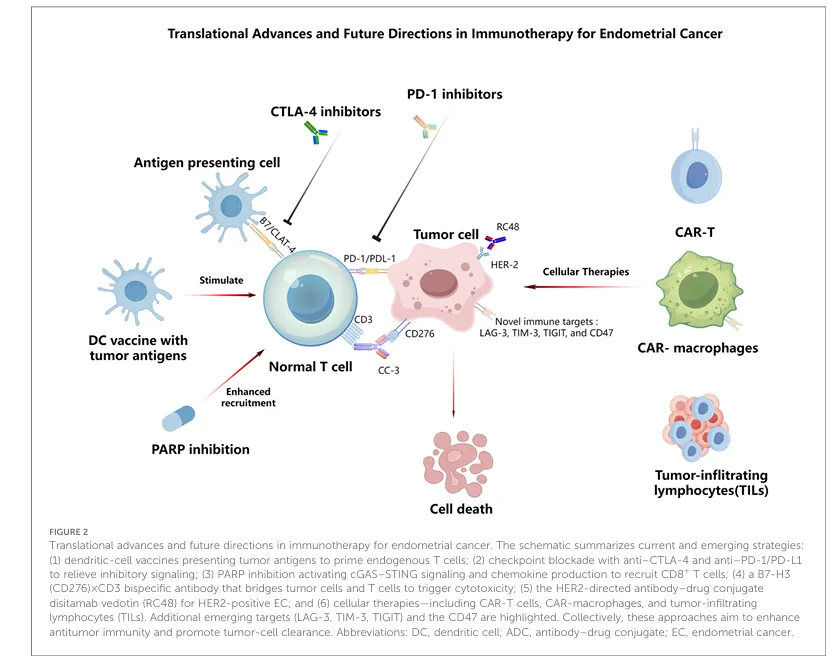
图2.子宫内膜癌免疫治疗的转化进展与未来方向。该示意图总结了当前及新兴的治疗策略:(1)树突状细胞疫苗,通过呈递肿瘤抗原以启动内源性T细胞反应;(2)免疫检查点阻断,采用抗CTLA‑4及抗PD‑1/PD‑L1抗体解除抑制性信号;(3)PARP抑制剂,通过激活cGAS–STING信号通路并增加CD8⁺ T细胞浸润,增强抗肿瘤免疫;(4)B7‑H3(CD276)×CD3双特异性抗体,将T细胞与肿瘤细胞连接;(5)针对HER2过表达子宫内膜癌的抗体‑药物偶联物,如曲妥珠单抗德鲁司坦(RC48);以及(6)细胞治疗策略,包括CAR‑T细胞、CAR‑巨噬细胞和肿瘤浸润淋巴细胞(TILs)。此外,新兴靶点还包括LAG‑3、TIM‑3、TIGIT和CD47。总体而言,这些策略旨在增强抗肿瘤免疫并促进肿瘤清除。
1.从免疫治疗耐药机制到靶向干预策略
子宫内膜癌对免疫治疗的耐药源于多层次的肿瘤‑免疫互作障碍,包括抗原呈递缺陷、PD‑L1持续高表达、代谢性免疫抑制及翻译后修饰介导的免疫逃逸。上述机制在 pMMR 和 p53 异常型肿瘤中尤为突出,解释了免疫检查点抑制剂疗效受限的原因。
图3.系统展示了驱动子宫内膜癌免疫耐药的关键通路。
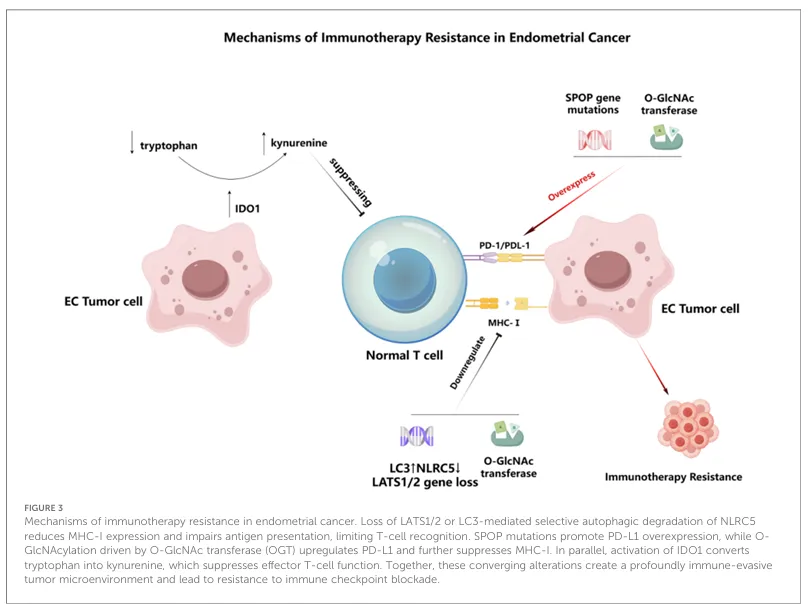
基于这些机制,B7‑H3 等新型免疫调节靶点受到关注,相关双特异性抗体和抗体‑药物偶联物正推动免疫治疗向更精准的方向发展。
2. 细胞治疗与肿瘤微环境调控
细胞治疗通过不依赖 MHC 的杀伤机制,为免疫耐药肿瘤提供新思路。CAR‑T、CAR‑巨噬细胞、肿瘤浸润淋巴细胞治疗及 TCR 工程化 T 细胞等策略正在探索中,并可通过联合微环境调控药物、溶瘤病毒或清除衰老细胞等手段,改善肿瘤浸润和治疗持久性,拓展免疫治疗的适用范围。
3. 未来方向:联合策略与精准治疗
未来免疫治疗的核心是理性联合与精准分层。免疫检查点抑制剂联合 PARP 抑制剂、HER2 靶向药物、抗血管生成治疗或免疫抑制通路抑制剂显示出良好前景;
新型免疫靶点、生物标志物(TCR克隆性、干扰素信号和循环肿瘤DNA动态变化)及个体化策略(如新抗原疫苗、树突状细胞疫苗和TCR工程化治疗)不断涌现。此外,免疫治疗与放疗及先天免疫通路激活剂的结合,为增强系统性抗肿瘤免疫提供了新的可能。

参考资料

