子宫内膜癌是最常见的妇科恶性肿瘤,美国2025年预计新发病例超6.9万,死亡近1.4万,且死亡率呈上升趋势。多数患者在早期即可通过手术治愈,但约9–14%在诊断时已出现远处转移,预后极差,5年生存率仅18.4%。原发性EC的分子特征已明确,分为POLE超突变型、MSI-H型、CN-low/NSMP型和CN-high/TP53异常型,其中CN-high/TP53异常型预后最差。然而,远处转移的分子机制仍不清楚。2025年3月在Gynecologic Oncology发表《The genomic landscape of distant metastatic endometrial cancer》,主要通过对137例远处转移性EC和711例原发性EC进行大规模基因组测序,发现转移性EC更具染色体不稳定性,而非突变负荷增加,且在CN-low/NSMP亚型中AKT1和CTNNB1突变显著富集,而PTEN突变减少,提示这些差异可能成为未来靶向治疗的重要突破口。
研究方法
一.样本来源与筛选
1. 研究基于 MSK-IMPACT 测序平台(检测505个癌症相关基因),时间范围为2015/4-2020/6;
2. 从1888例子宫内膜癌中筛选出 137例远处转移性EC和 711例原发性EC(肿瘤纯度>15%)用于后续分析;
3. 所有转移性样本均经病理专家复核,确认组织学类型、转移部位及MMR、p53状态;
二.基因组分析
1. 提取体细胞突变、拷贝数(CN)改变、结构变异、肿瘤突变负荷(TMB)、MSIsensor评分。
2. 计算基因组改变比例(FGA) 以评估染色体不稳定性。分子亚型定义:
1)POLE:POLE热点突变
2)MSI-H/MMRd:MSI sensor≥10或MMR蛋白缺失
3)CN-H/TP53异常:TP53致病突变或纯合缺失
4)CN-L/NSMP:不符合上述特征的肿瘤
3. 可操作基因与通路分析
1) 使用 OncoKB 标准定义临床可操作突变(Level 1–3)
2) 分析12个致癌通路,若样本中至少一个相关基因改变则认为该通路受影响
3) 染色体臂水平CN改变通过ASCETS工具计算

研究方法
一. 远处转移性EC的临床病理特征
远处转移性EC主要为复发(84%),最常见转移部位是肺(48%),组织学以子宫内膜样癌(43%)和浆液性癌(20%)为主,分子亚型主要为CN-H/TP53异常(42%)和CN-L/NSMP(39%),低级别子宫内膜样癌转移多为CN-L/NSMP(63%)和MSI-H/MMRd(32%)。
EC远处转移特征总览

二.临床特征:原发灶 vs 远处转移灶
1. 年龄差异:转移性患者年龄更大(中位数67岁 vs 64岁,p<0.001)。
2. 组织学差异:转移性EC低级别子宫内膜样癌比例更低(30% vs 51%,p=0.001),近肾样类型比例更高(6% vs <1%,p<0.001)。
3. 分子亚型:CN-H/TP53异常、CN-L/NSMP和MSI-H/MMRd分布无显著差异,但POLE型在转移灶中极少见(1例 vs 9%,p=0.002),符合其低复发风险。
4. 基因组特征:两者整体突变谱相似,常见突变包括 PI3K通路基因(PTEN、PIK3CA、PIK3R1)、TP53、CTNNB1、ARID1A。
5. 临床可操作突变:原发性EC更常见(37% vs 27%,p=0.025),包括MSI-H和高TMB。
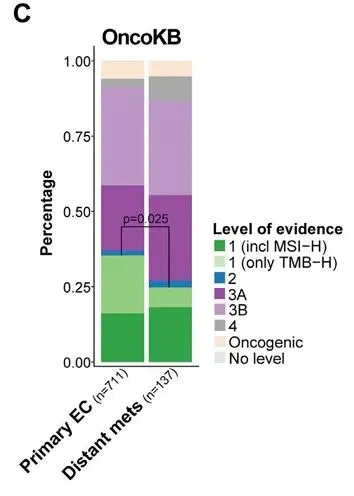
三.子宫内膜癌原发灶 vs 远处转移灶的基因组特征
1.原发灶&转移灶组织学类型比例

2.TMB比较:原发灶与转移灶相似;
染色体不稳定性(FGA)比较:转移灶显著高于原发灶;

3.转移部位分析:
1)肺是最常见转移部位:癌肉瘤57.9%,子宫内膜样癌52.5%,浆液性癌35.7%
2)浆液性癌更易转移至软组织(17.9%)
3)子宫内膜样癌更易转移至肝(22%)和胃肠道(10.2%)
4)在 CN-L/NSMP亚型中,肺转移比例更高,软组织转移比例更低,提示不同分子亚型可能影响远处转移模式
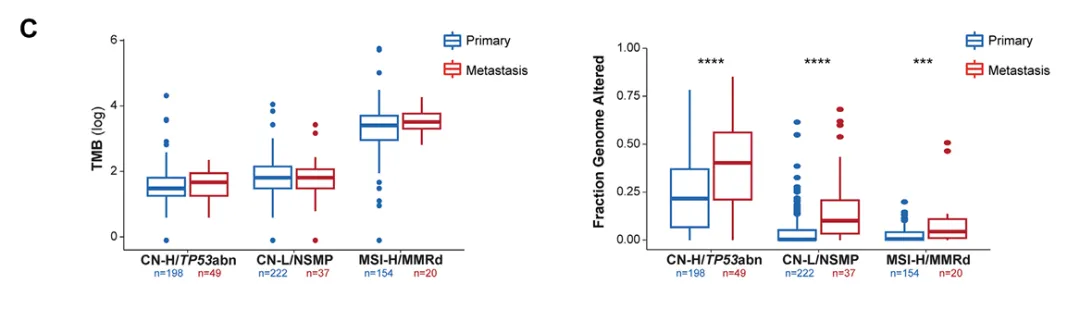
4.分子亚型与TMB的关系:TMB在各分子亚型中原发与转移性相似;
1)CN-H/TP53异常:4.4 vs 5.3 Mut/Mb(p=0.13)
2)CN-L/NSMP:6.1 vs 6.1 Mut/Mb(p=0.90)
3)MSI-H/MMRd:30.15 vs 33.45 Mut/Mb(p=0.22)
5.分子亚型与FGA的关系:转移灶的 FGA 显著高于原发灶;总体水平上 CN-H/TP53abn 最高、CN-L/NSMP 次之、MSI-H/MMRd 最低;
1)CN-H/TP53异常:40% vs 22%(p<0.0001)
2)CN-L/NSMP:10% vs 0%(p<0.0001)
3)MSI-H/MMRd:4% vs 1%(p=0.0009)
6.拷贝数变化细节:
1) CN-H/TP53异常型转移灶显著增加多个染色体臂的增加和丢失(如1p、6q、8q、11q、19p、20增益,2q、5p、12、21q丢失)。
2) CN-L/NSMP型转移灶更常见1q、7q增加及13q、6p丢失。
3) MSI-H/MMRd型转移灶也出现显著差异,尤其是染色体10增加。
7.基因突变差异:
1) 整体基因组在原发灶与转移灶CN-H/TP53异常型的癌肉瘤、浆液性癌和子宫内膜样癌之间无显著差异。
2) 但在CN-L/NSMP和MSI-H/MMRd亚型中,转移灶显著富集:
a. CTNNB1突变:CN-L/NSMP(59% vs 36%,q<0.1),MSI-H/MMRd(40% vs 9%,q<0.1)
b. AKT1突变:CN-L/NSMP转移灶显著增加(28% vs 0%,q<0.1)
c. PTEN突变:CN-L/NSMP原发灶更常见(83% vs 50%,q<0.01)
1.根据不同转移部位,分析了致癌体细胞突变及拷贝数(CN)改变所影响的基因和相关信号通路。
2.CNS 转移几乎全部携带 TP53 突变,而 GI 转移仅少数有 TP53 突变,骨转移则完全缺失该突变。
1)CNS 转移:p53 通路主导,TP53 突变普遍(100%)。
2)骨转移:PI3K 通路主导,PTEN(100%) 和 PIK3R1(100%) 突变普遍,TP53 缺失。
3)GI 转移:PTEN(70%)、BCOR(50%)、JAK1(40%) 突变常见,细胞周期通路改变。
4)肺转移:KRAS (30%)突变显著,RTK/RAS 通路活跃(56%)。
5)跨部位共同通路:表观遗传、PI3K、p53 是最常见的三条通路。
4.信号通路在不同转移部位的改变
1)骨转移:PI3K 通路在所有骨转移中均发生改变。
2)CNS 转移:p53 通路在所有 CNS 转移中均发生改变。
3)跨部位最常见通路:表观遗传调控、PI3K 和 p53。
4)其他显著通路:
a.细胞周期通路:CNS(40%)、GI(50%)转移常见。
b.RTK和RAS通路:CNS(40%)、肺(56%)、软组织(60%)转移常见。
总结
一.主要发现
1. 远处转移 EC 最常见分子亚型:CN-H/TP53abn 和 CN-L/NSMP。
2. 转移灶 不增加突变负荷(TMB),但 染色体不稳定性显著升高,即 CN 改变是进展驱动因素。
3. MSI-H/MMRd 转移也出现 CN 改变,尽管原发通常缺乏此类改变。
二.关键突变
1. AKT1热点突变:在远处CN-L/NSMP转移中显著富集 → 支持 AKT 抑制剂治疗。
2. CTNNB1热点突变:在远处CN-L/NSMP和MSI-H/MMRd转移中富集 → 可能与复发风险相关。
三. 转移部位特点
1. CNS 转移:均为 CN-H/TP53abn,TP53 突变必需,预后差。
2. 骨转移:无 TP53 突变,PI3K 通路改变显著。
3. 肺/肝转移:最常见,PI3K 通路改变频繁。
四. 临床意义
1. 转移进展主要由 CN 改变驱动,而非突变负荷。
2. AKT1 和 CTNNB1 突变可能成为治疗靶点。
3. 需进一步研究分子特征与转移部位的关联。
[1]. Gynecologic Oncology(期刊简称:Gynecol Oncol)的最新影响因子如下:2024年 JCR 报告显示,影响因子为 4.1,2023年为 4.5,五年影响因子接近 4.4。2026–2027年度预估影响因子约为 4.7,显示其学术影响力持续走强。[2].The genomic landscape of distant metastatic endometrial cancer;Gynecologic Oncology 195 (2025) 89–97。