学习笔记(16):看似“低调”的 NSMP 子宫内膜癌,其实最复杂?
- 2026-05-10 16:44:34
近期发表在 Gynecologic Oncology1 的系统综述《The challenge of molecular stratification in No Specific Molecular Profile endometrial cancer》2,正试图回答这个关键问题——NSMP 内部是否存在被忽视的分子标志物,可以帮助我们实现更精准的风险分层?


本研究遵循 PRISMA 标准系统检索 2013–2024 年文献,最终从 1699 条记录中纳入 19 项观察性研究,系统评估 ProMisE 之外分子改变在整体子宫内膜癌及 NSMP 亚组中的预后价值,并通过偏倚及异质性分析确保方法学严谨性。纳入研究以早期子宫内膜样癌为主,其中 5 项提供 NSMP 的独立生存分析,为后续整合 NSMP 内部分子标志物奠定基础。
纳入研究评估的分子改变包括:
ARID1A 突变
CTNNB1 突变/β-catenin 核表达
L1CAM 高表达
PIK3CA/PTEN 突变
雌激素受体(ER)缺失
检测方法主要包括:
免疫组化(IHC):15 项研究
下一代测序(NGS):4 项研究,三项用于 CTNNB1,一项用于 ARID1A)
因此 Meta 分析仅纳入了生存结局(PFS、OS)的 HR 值,并将结果按总体人群与 NSMP 亚组分别呈现,同时区分单变量和多变量分析。
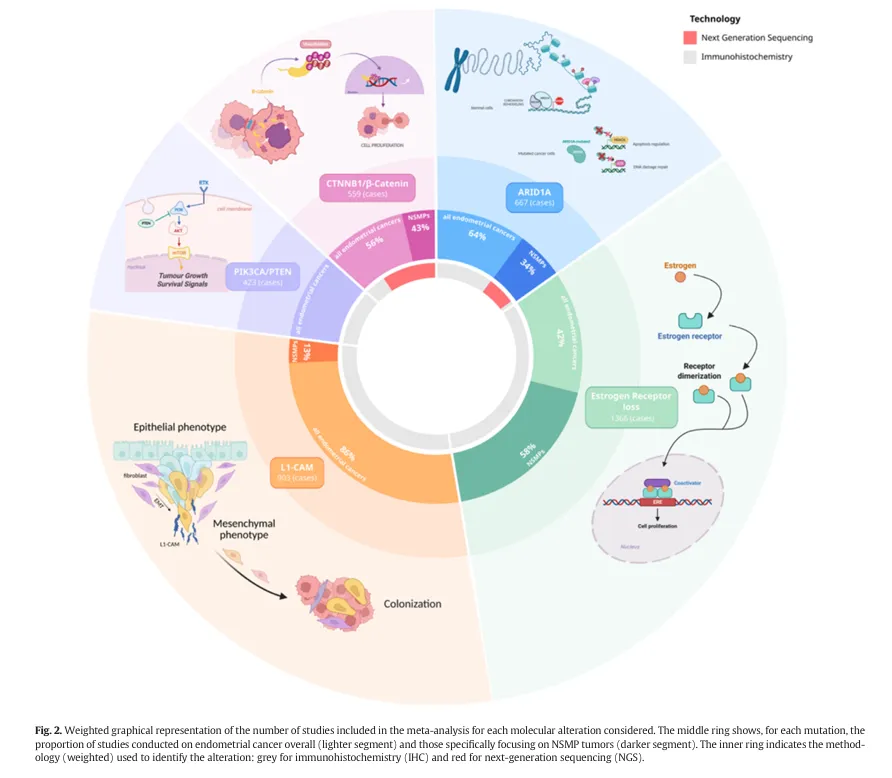
图2. 各类分子改变纳入 Meta 分析研究数量的加权图示。外环展示了每一种分子改变所对应的研究数量;中环区分了研究对象为整体子宫内膜癌人群(浅色部分)与专门针对NSMP亚组(深色部分)的比例;内环则标示用于检测该分子改变的技术类型:灰色代表免疫组化(IHC),红色代表二代测序(NGS)。
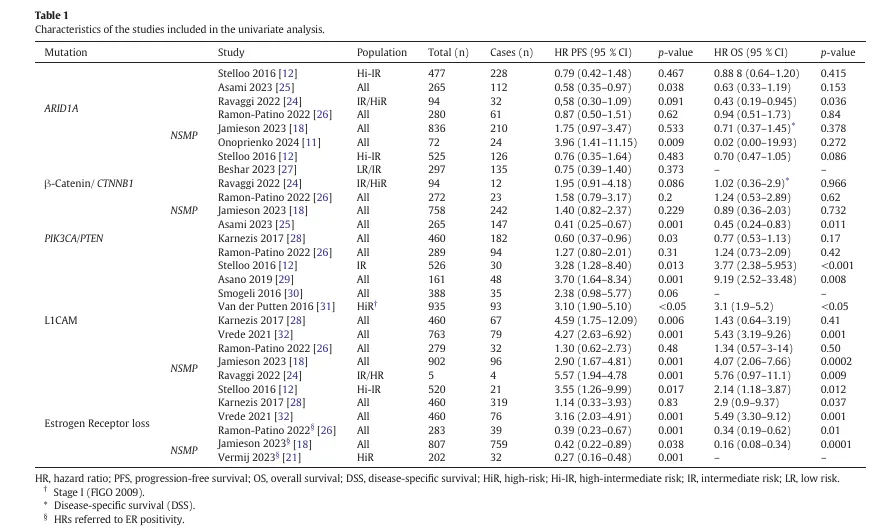
表 1. 纳入单变量分析的研究基本信息
ARID1A 突变
共有 4 项研究在单变量分析中探讨 ARID1A 突变的预后意义,其中 2 项在 NSMP 亚组进行了独立分析;另有 2 项提供了多变量结果。
总体人群→ ARID1A 突变对预后无显著影响
PFS:HR 0.97(95% CI 0.62–1.52)
OS:HR 0.79(95% CI 0.62–1.00)
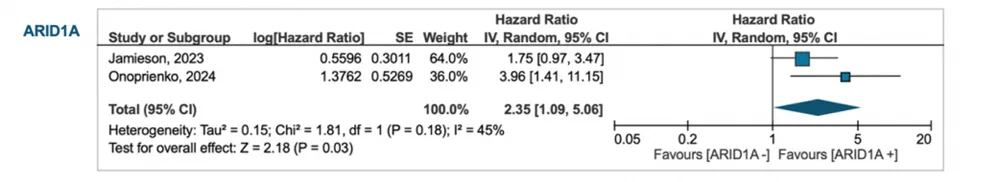
NSMP 亚组→ 在 NSMP中ARID1A突变与复发风险升高显著相关
PFS:HR 2.35(95% CI 1.09–5.06)
OS:影响并无统计学意义
多变量分析→ 结果亦未达到统计学显著
PFS:HR 1.27(95% CI 0.24–6.73)
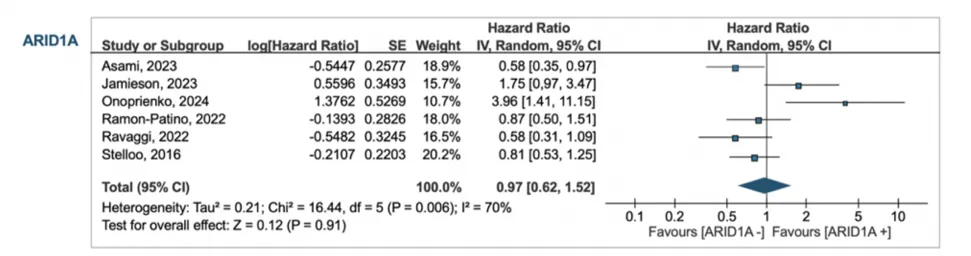
全部人群PFS
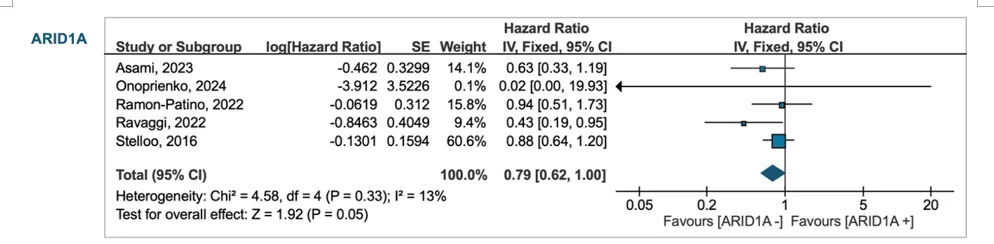
全部人群OS
NSMP人群PFS
β-catenin 核表达 / CTNNB1 突变
共有 4 项单变量研究,其中仅 1 项对 NSMP 提供独立生存分析;另有 1 项提供多变量结果。
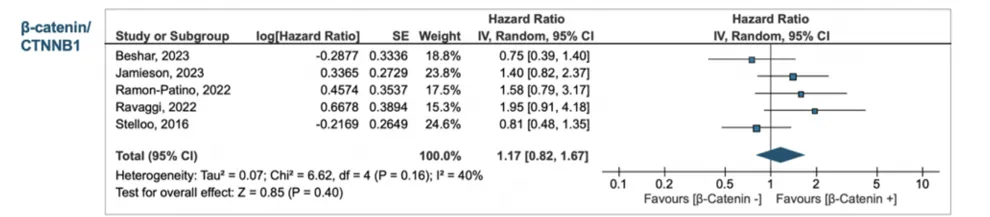
总体人群→未显示显著预后意义
PFS:HR 1.17(95% CI 0.82–1.67)
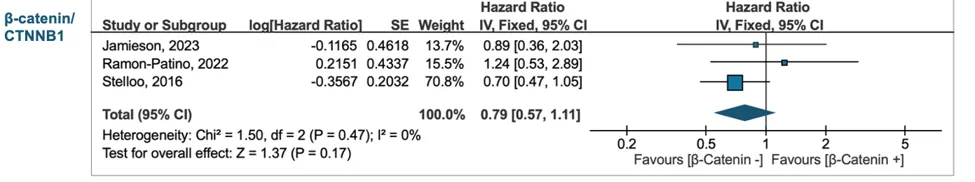
OS:HR 0.79(95% CI 0.57–1.11)
NSMP→在NSMP中也未显示显著影响
PFS:HR 1.4(95% CI 0.82–2.37)
DSS:HR 0.89(95% CI 0.36–2.03)
多变量分析数量有限,无法得出明确结论
全部人群PFS
全部人群OS
L1CAM 高表达
共有 7 项研究提供单变量分析,其中 2 项对 NSMP 进行了亚组分析;12 项研究提供了多变量数据。
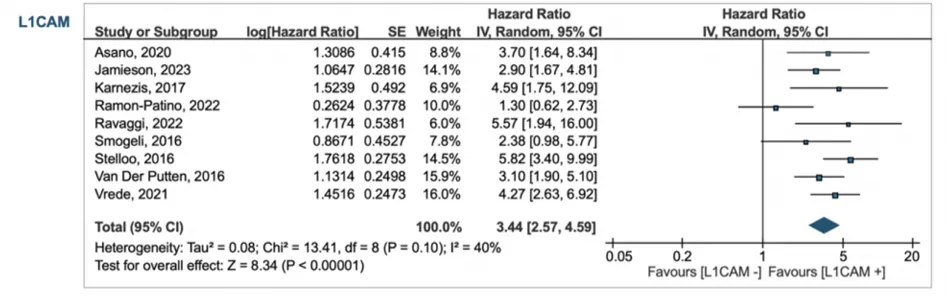
总体人群→ L1CAM 高表达与明显更差的生存结局相关
PFS:HR 3.44(95% CI 2.57–4.59)
OS:HR 3.29(95% CI 2.41–4.50)
DSS:HR 3.26(95% CI 1.27–8.90)
NSMP 亚组→ 在 NSMP 中亦为显著不良预后标志物
PFS:HR 3.34(95% CI 2.05–5.44)
OS:HR 3.69(95% CI 1.87–7.30)
多变量分析→L1CAM 过表达也显示显著的不良影响
PFS:HR 3.42(95% CI 1.94–6.01)
OS:HR 2.77(95% CI 1.68–4.59)
DSS:HR 1.80(95% CI 0.75–4.30)(未达显著性)
漏斗图分析显示不存在明显的发表偏倚
全部人群PFS
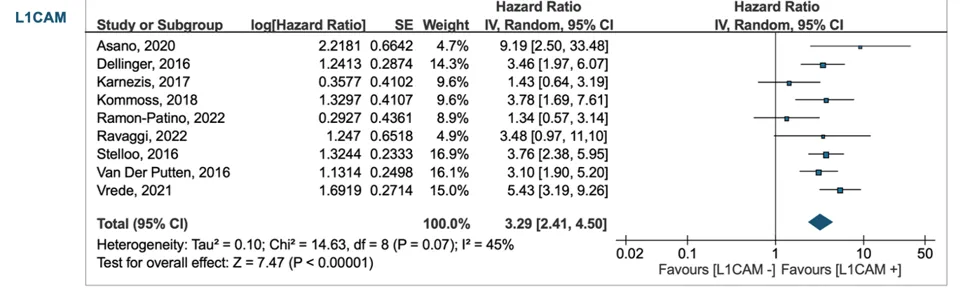
全部人群OS
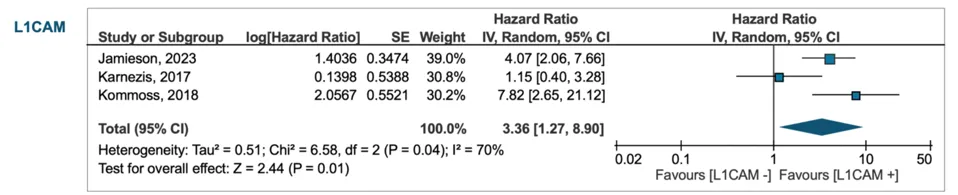
全部人群DFS
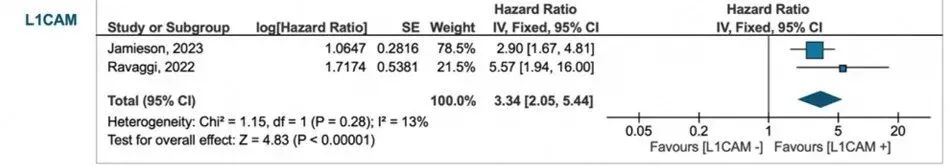
NSMP人群PFS
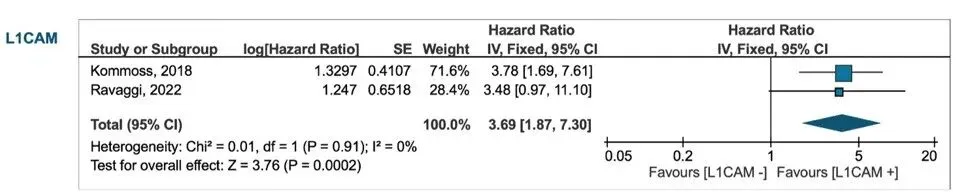
NSMP人群OS
PIK3CA / PTEN 突变
共有 3 项研究提供单变量分析,均未专门分析 NSMP;2 项提供多变量结果。PIK3CA/PTEN 突变在子宫内膜癌中的预后价值有限,未显示显著的不良或保护趋势。
总体人群→ 总体人群中无预后影响
PFS:HR 0.68(95% CI 0.35–1.32)
OS:HR 0.77(95% CI 0.47–1.27)
多变量分析进一步支持其缺乏显著预后价值
PFS:HR 0.62(95% CI 0.28–1.37) OS:HR 0.77(95% CI 0.31–1.95)
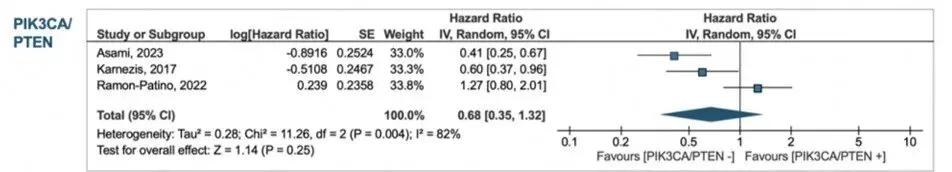
全部人群PFS
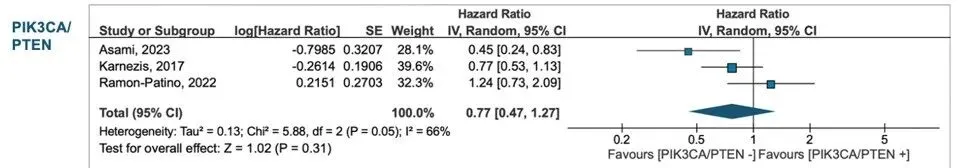
全部人群OS
雌激素受体(ER)缺失
4 项单变量研究评估 ER 缺失,含2项NSMP 研究;3 项提供多变量结果。
总体人群→ ER缺失显著不良预后
PFS:HR 3.13(95% CI 2.45–4.00)
OS:HR 3.28(95% CI 2.05–5.23)
DSS:HR 5.27(95% CI 2.70–10.27)
NSMP 亚组→ 在NSMP中同样为显著不良预后标志物
PFS:HR 3.14(95% CI 2.00–4.91)
多变量结果亦保持显著性
PFS:HR 1.50
OS:HR 2.96
DSS:HR 2.36
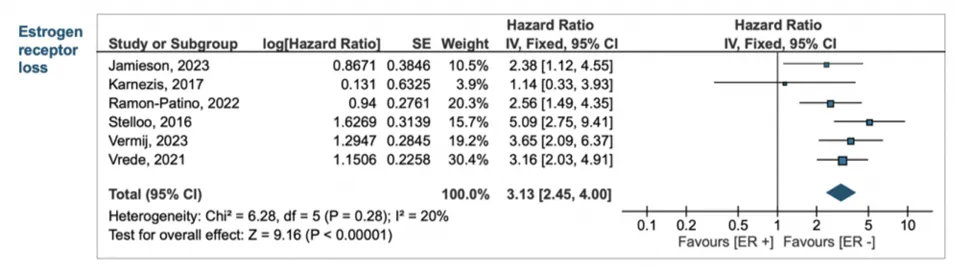
全部人群PFS
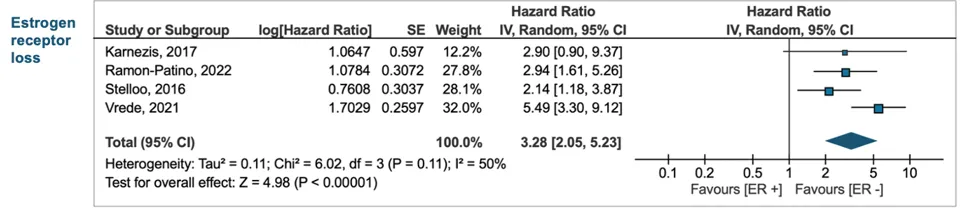
全部人群OS
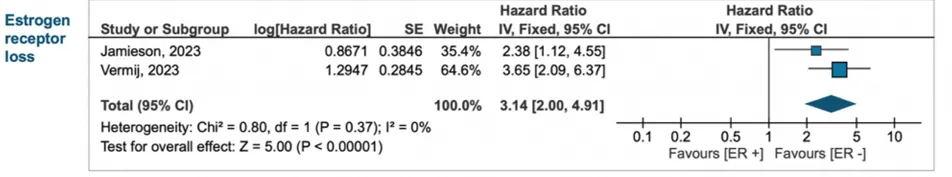
NSMP人群PFS
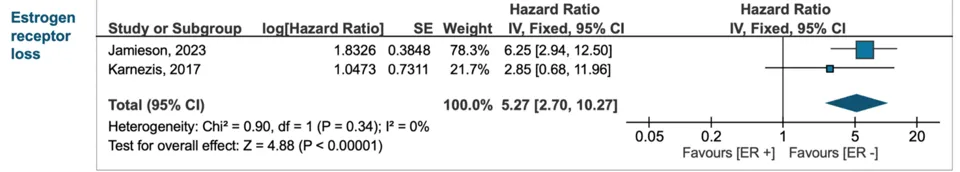
NSMP人群OS
研究的异质性
由于专门针对 NSMP 或单一FIGO 分期的研究数量有限,因此纳入所有可用数据,并通过亚组及敏感性分析处理异质性。
CTNNB1/β‑catenin:I² 较低 → 异质性中等,可接受
ER 缺失:I² 极低 → 各研究结果高度一致
L1CAM:存在一定变异,但总体效应方向一致
ARID1A 与 PIK3CA:异质性较高 → 需谨慎解读结果
本次 Meta 分析显示,L1CAM过表达与ER缺失是整体子宫内膜癌及NSMP 亚组中最稳定、最明确的不良预后因素;而 ARID1A、β‑catenin/CTNNB1、PIK3CA/PTEN 等分子改变的预后价值有限且证据不一致,提示 NSMP 内部亟需更多专门研究来明确其分子标志物及指导未来临床试验设计。

结合文献的讨论、临床意义与未来方向
现有研究中,仅少量文献在 NSMP 亚组中探索 ProMisE 体系之外的分子改变,其证据总体有限,尤其缺乏 OS 数据。
然而既有研究一致显示 L1CAM 过表达与 ER 缺失显著提高 NSMP 的复发风险,而 β‑catenin/CTNNB1 与 ARID1A 的预后价值仍不明确,可能仅在特定分子亚群中起作用。PORTEC‑4a 试验基于 CTNNB1 与 L1CAM 的风险意义进一步推动了 NSMP 的分层策略,其中 CTNNB1 exon 3 突变用于区分低/中风险 NSMP,而 L1CAM 高表达被视为高侵袭性特征。
ER 缺失同样显示出稳定的不良预后意义,已被建议与肿瘤分级结合用于将 NSMP 进一步划分为高低风险组。
准确识别真正低风险的 NSMP 有助于:明确可降阶治疗的亚组(类似 POLE‑mut)/甚至可能采用随访替代辅助治疗;
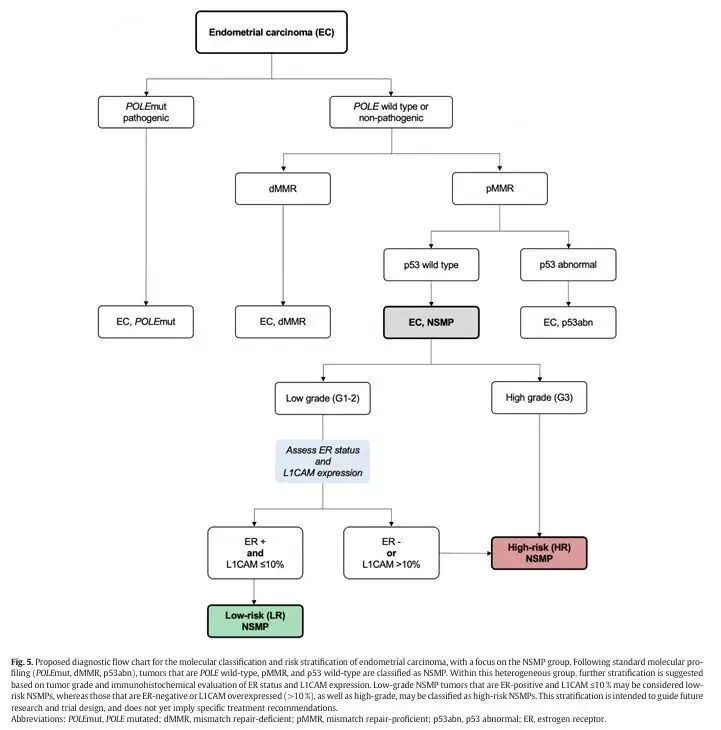
基于当前证据,ER 与 L1CAM 是最具潜力的 NSMP 风险分层标志物,可通过 IHC 进一步细化随访与研究策略;而 ARID1A、CTNNB1、PIK3CA 等标志物尚缺乏足够证据支持临床应用,仍需更多专门针对 NSMP 的研究来明确其预后价值。下图是建议的诊断流程图:

Take Home Message
1️⃣ 在 NSMP 子宫内膜癌中,L1CAM 过表达与 ER 缺失是最稳定、最明确的不良预后标志物,可用于进一步分层 NSMP 风险。
2️⃣ ARID1A、CTNNB1、PIK3CA 等分子改变的预后价值仍不确定,且可能仅在特定亚组中有意义,亟需更多专门研究。
3️⃣ 引入 ER/L1CAM 的 NSMP 分层思路正进入临床试验阶段,并可能成为未来实现治疗升级或降阶的重要基础。



