学习笔记(15):MMR‑d子宫内膜癌不再“一视同仁”:一项大数据研究告诉我们什么?
- 2026-05-10 16:52:18

 研究设计
研究设计1. 入组人群
时间范围:2017年7月—2022年4月
疾病类型:原发子宫内膜癌
FIGO 2009 分期:IA–IVB
治疗要求:均接受了初次手术治疗(未接受新辅助治疗)
必须具备:完整的手术标本病理与 IHC 检测(MMR、p53、激素受体状态),最终将 IHC 中至少 1 个 MMR 蛋白缺失者定义为 MMRd 人群并进一步分型。
2. 研究计划
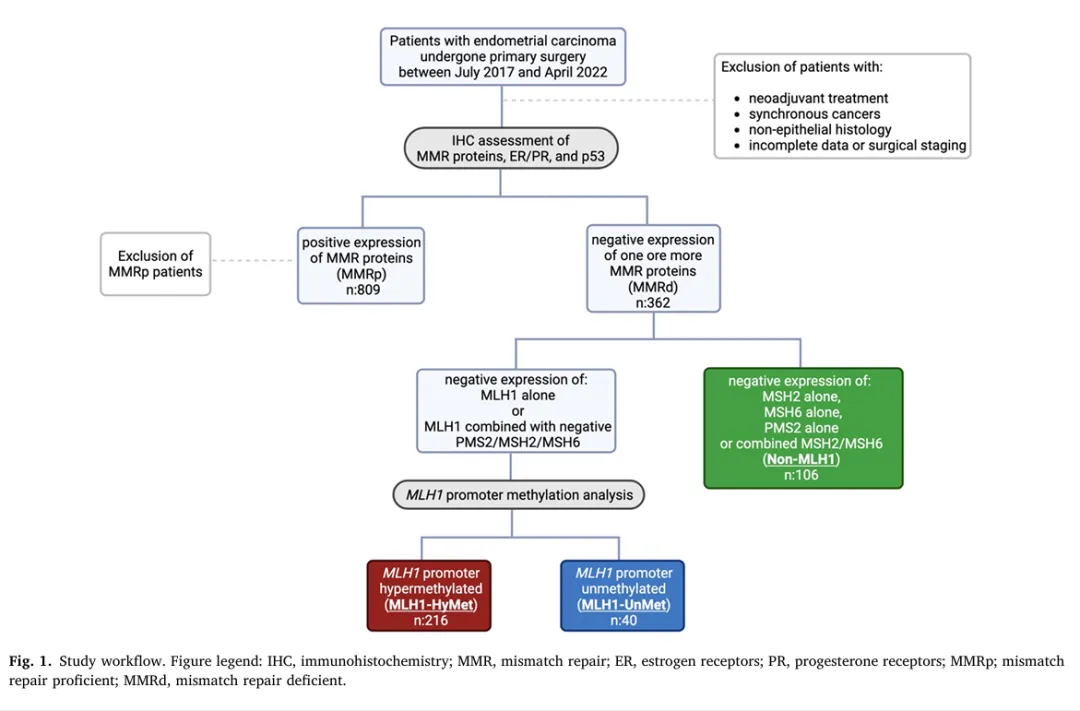
IHC 检测 MMR 蛋白(MLH1、PMS2、MSH2、MSH6)
对 MLH1 缺失者进一步进行 MLH1 启动子甲基化检测
基于 IHC + 甲基化状态,将 MMRd 分为三组:
MLH1-HyMet(MLH1启动子高甲基化)
MLH1-UnMet(MLH1启动子未甲基化)
non‑MLH1(MSH2/MSH6/PMS2缺失)
3. 主要终点/次要终点
主要终点:
肿瘤临床病理特征
5 年无事件生存(EFS)
次要终点:
早期阶段 vs. 晚期/转移性阶段 的 EFS 差异
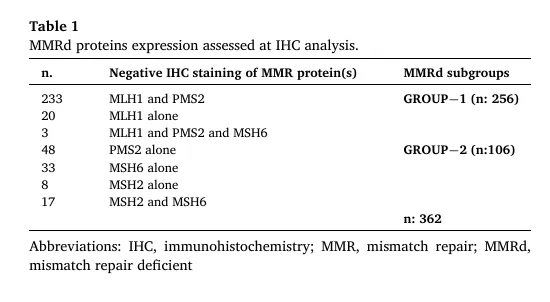
MLH1-HyMet(高甲基化):216 例,占 59.7%
MLH1-UnMet(未甲基化):40 例,占 11%
non-MLH1(非 MLH1 缺陷):106 例,占 29.3%
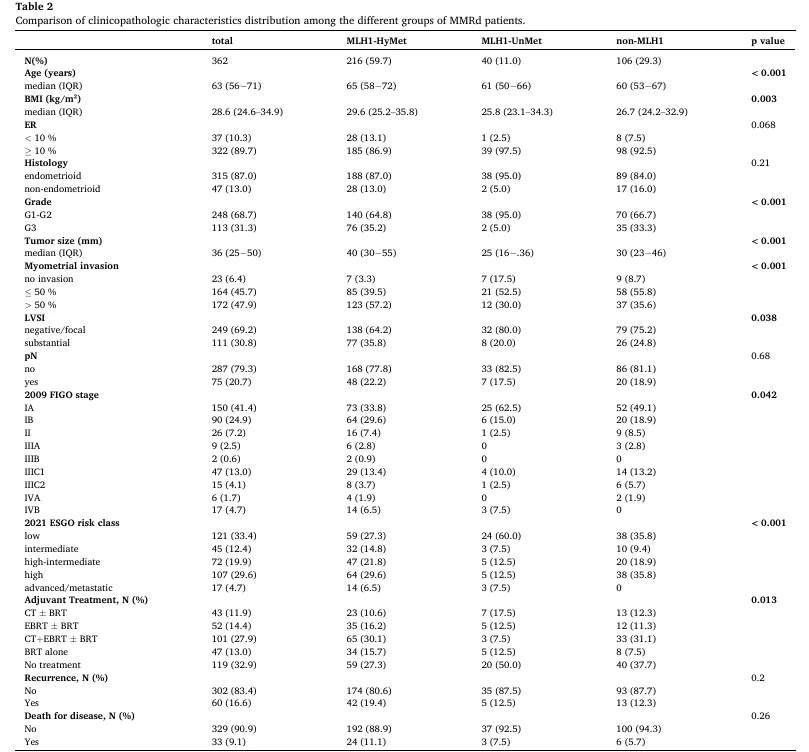
在不同 MMRd 亚型中,MLH1-HyMet 组整体呈现更不良的临床病理特征:
年龄最大(p < 0.001)
BMI 最高(p = 0.003)
肿瘤体积最大(p < 0.001)
肌层浸润最深(p < 0.001)
明显 LVSI 比例最高(p = 0.038)
肿瘤分级:
MLH1-HyMet 与 non-MLH1 中 3 级肿瘤比例更高
MLH1-UnMet 中仅有 5% 为 3 级(p < 0.001)
分期与风险:MLH1-HyMet FIGO IA 期比例最低(p = 0.042),低风险肿瘤比例最低(p < 0.001)
辅助治疗:MLH1-HyMet 更常需要辅助治疗,未接受辅助治疗的比例仅 27.3%,低于 MLH1-UnMet(50%)和 non-MLH1(37.7%)(p = 0.013)
3.EFS的结果分析
在单因素Cox回归分析中,多项临床病理特征都与无事件生存期(EFS)相关,包括:
肿瘤组织学类型(子宫内膜样 vs 非子宫内膜样)
肿瘤分级(G1/G2 vs G3)
肿瘤大小
LVSI(阴性/局灶性 vs 明显性)
2009 FIGO 分期(I–II vs III–IV)
2021 ESGO-ESTRO-ESP 风险分类(从低风险到晚期/转移性)
但在多因素Cox回归模型中,只有“肿瘤大小”和“LVSI”是dMMR人群中独立影响 EFS 的因素;

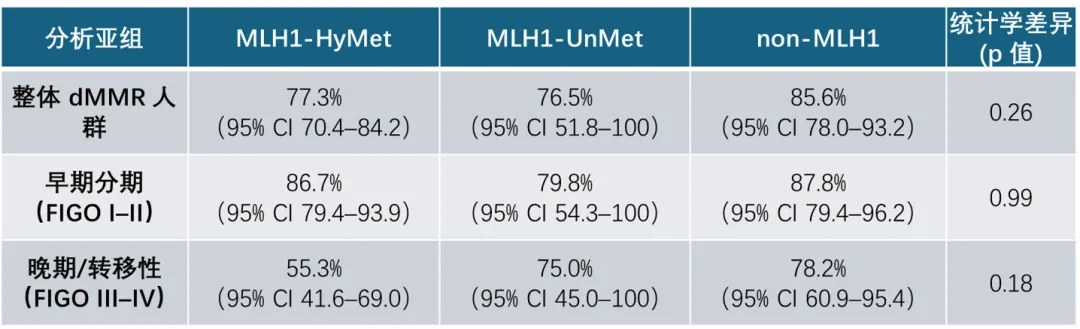
dMMR各亚型5年EFS 汇总表:
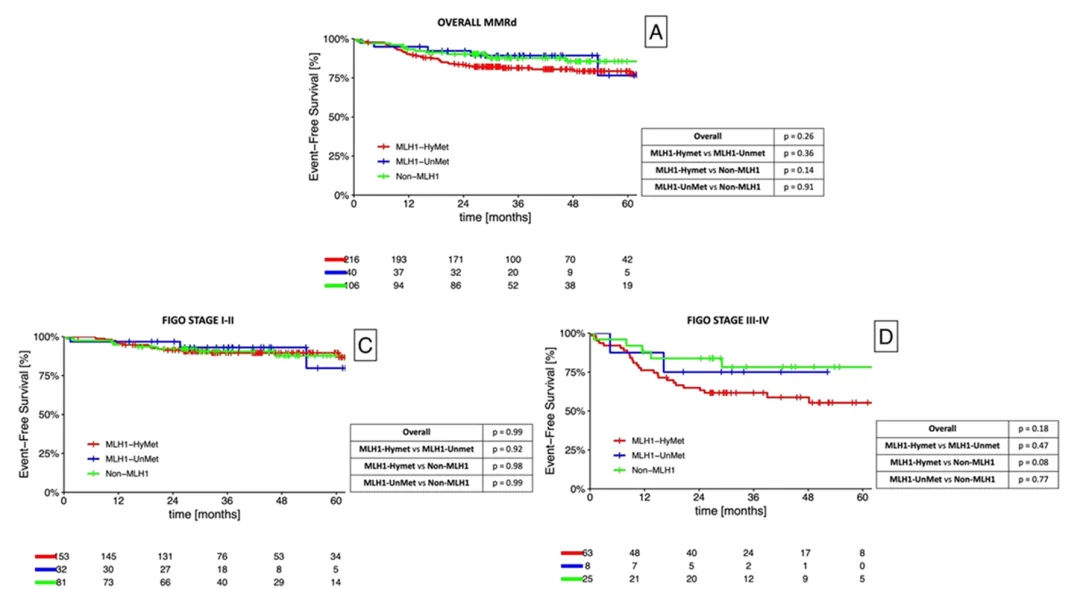
4. 对子宫内膜样亚型(n=315)进行了亚组分析
子宫内膜样(Endometrioid)MMRd 亚型 5 年;
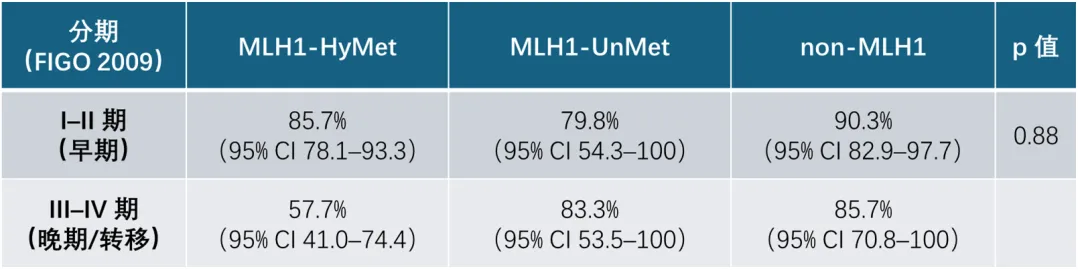
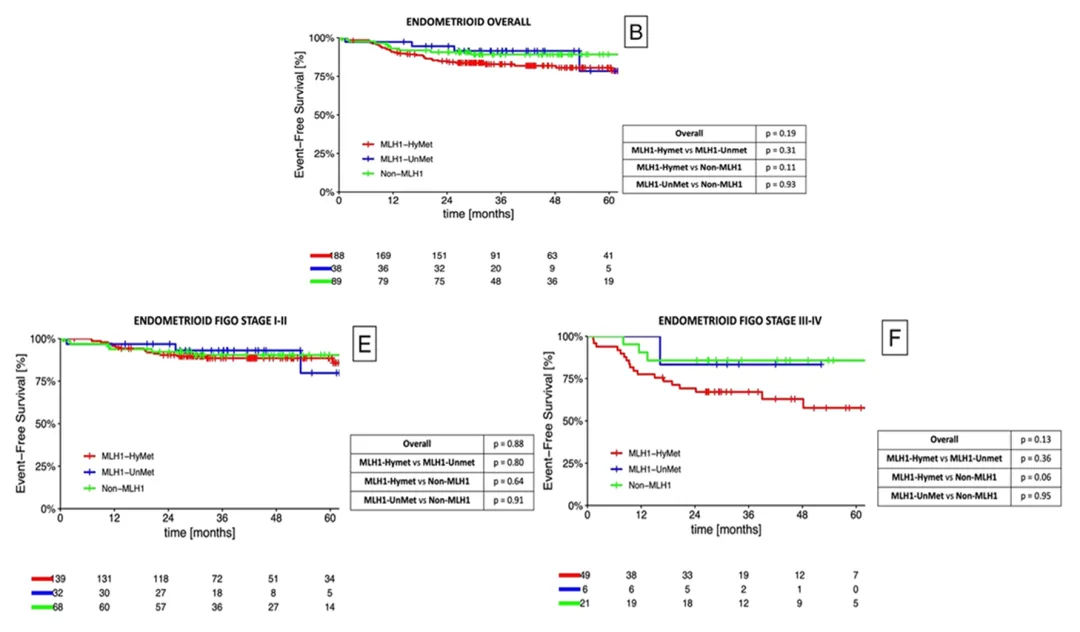
在多因素分析中,诊断年龄、肿瘤体积、LVSI 存在情况以及晚期/转移性(2021 ESGO 风险分类)均与 EFS 独立相关。
5.非子宫内膜样(non-endometrioid)亚型
本研究人群中有 13.0%(n=47)的 MMRd EC 属于非子宫内膜样组织学类型,该亚组中:
40.4%(n=19)为去分化型
36.2%(n=17)为混合型
12.8%(n=6)为浆液性
4.3%(n=2)为透明细胞型
2.1%(n=1)为癌肉瘤
2.1%(n=1)为未分化型
在不同 MMRd 亚型中:
59.6%(n=28)为 MLH1-HyMet
36.2%(n=17)为 non-MLH1
4.3%(n=2)为 MLH1-UnMet
34.0%(n=16)的非子宫内膜样MMRd也是多重分类,且全部浆液性(n=6)或混合型(内膜样-浆液性,n=1)病例均为 p53 异常(p53abn),即多重分类。
6. 多重分类 MMRd-p53abn
纳入分析的 MMRd 患者中,5.5%(n=20)为多重分类,其中 80%(n=16)为非子宫内膜样类型;
25%(n=5)为 MLH1-HyMet
10%(n=2)为 MLH1-UnMet
65%(n=13)为 non-MLH1
绝大多数多重分类患者接受了辅助治疗(85%,n=17)。其中 2 名患者(10%)出现疾病复发:
一名因临床状况差未接受辅助治疗
一名拒绝化疗,仅接受放疗
研究讨论
1.文献比较与一致性
MLH1‑HyMet 在文献中占比 40–80%,本研究为 59.7%,结果一致。
生物学侵袭性趋势(更晚分期、更多 LVSI、更大肿瘤)与既往研究一致。
与 Post 等研究类似,均提示 MLH1‑HyMet 预后更差,但本研究未达统计学显著性,差异可能由于:
其他研究中 LS 患者更年轻、更早分期
随访时间更长,本研究随访时间(中位 42 个月)有限
2. 关于免疫治疗(ICIs)
dMMR的EC对ICIs(如帕博利珠单抗等)的疗效优于pMMR;
预后方面,高甲基化 MMRd 通常较差,但各 MMRd 亚组对 ICIs 的反应差异在文献中不一致:
小规模研究:Lynch/Lynch-like 反应更佳,MLH1‑HyMet 反应率低
大型试验(NRG GY018、GARNET、RUBY):MMR 缺陷机制不影响疗效
3.潜在机制:
MLH1 高甲基化 MMRd 肿瘤通常呈现更“免疫冷”的肿瘤微环境,表现为较低的 PD‑L1 表达、较少的 B/T 细胞浸润和较低的免疫活化评分。
前临床机制研究支持“免疫冷”微环境可能与 ICI 低应答相关,为高甲基化 MMRd 预后较差和治疗反应差异提供潜在生物学解释。
本研究中无患者在晚期/转移性阶段接受一线 ICIs,可能导致未观察到更大差异。
4. 研究优劣势
优势
样本量大,为文献中最大 MMRd 队列之一
罕见亚型(多分类、非子宫内膜样 MMRd)数据详尽
研究流程与关键文献一致
局限
回顾性设计
随访不足
部分亚型样本数少
缺乏 POLE、SWI/SNF、LS 生殖系检测(对结论影响有限)
5. 临床意义及未来方向
随着 EC 分子治疗发展,MMRd 作为重要亚组,需要进一步细分以指导治疗;
正在进行的重要试验(RAINBO、PORTEC‑4a、EUGENIE)将推动分子分型指导治疗;
最新 LEAP‑001 显示:仑伐替尼 + 帕博利珠单抗显著延长生存;
对于生物学上更侵袭的 MLH1‑HyMet 需重点探索:免疫+多靶点联合方案是否可显著弥补 ICIs 效果较弱的问题;
Take Home Message
在 1171 名接受手术分期和 IHC 评估的子宫内膜癌患者中,30.9%(362例)被诊断为dMMR,其中 59.7%(216 例)为 MLH1‑HyMet、11%(40 例)为 MLH1‑UnMet、29.3%(106 例)为 non‑MLH1。
相比另外两个亚组,MLH1‑HyMet 患者年龄更大、BMI 更高,且表现出更具侵袭性的病理特征(更大的肿瘤体积、更深的肌层浸润、明显的 LVSI 以及更低比例的早期与低风险疾病)。
dMMR亚组的EFS整体无显著差异,且在调整分期和组织学后仍然一致,但在晚期/转移性患者中,MLH1‑HyMet 显示出更差预后的趋势。
总体而言,MLH1 高甲基化 MMRd EC 的临床病理特征更具侵袭性,但三亚组之间的预后差异尚未达到统计学显著性。



