
[核心素养发展目标]掌握氧化还原反应方程式的配平。
一、氧化还原反应方程式的配平
1.配平原则
(1)得失电子守恒:氧化剂和还原剂得失电子总数相等,化合价升高总数=化合价降低总数。
(2)质量守恒:反应前后原子的种类和个数不变。
(3)电荷守恒:离子反应前后,阴、阳离子所带电荷总数相等。
2.配平的一般步骤
以碳与浓硫酸反应生成二氧化碳、二氧化硫和水为例
(1)标变价:写出反应物、生成物的化学式,并在化学方程式中标出化合价发生变化的元素的化合价。
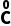 +H2
+H2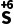 O4(浓)——
O4(浓)——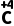 O2+
O2+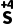 O2+H2O
O2+H2O
(2)列得失:根据化合价的变化标出电子转移的方向和数目。
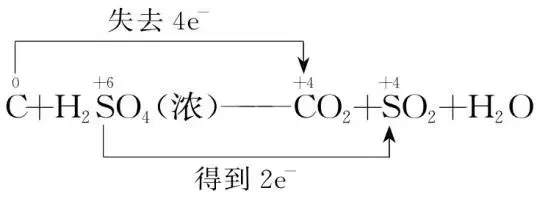
(3)求总数:使得失电子的总数相等。
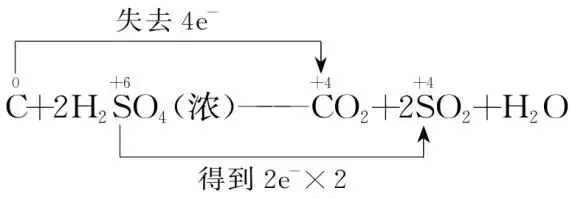
(4)配系数:根据质量守恒定律配平其他物质的化学计量数,并添加气体符号,注明反应条件,将单线改为双线。
C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
(5)查守恒:利用守恒三原则,检查是否配平。
1.配平下列化学方程式。
(1)Mg+CO2 C+MgO
C+MgO
(2)Na2SO3+KIO3+H2SO4===Na2SO4+K2SO4+I2+H2O
2.(2024·福建泉州高一段考)储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为
C+K2Cr2O7+H2SO4===CO2↑+K2SO4+Cr2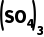 +H2O。
+H2O。
(1)配平上述化学方程式。
(2)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为 L。
二、配平氧化还原反应方程式的常用技巧
题型1 逆向配平法
分解反应、歧化反应、部分氧化还原反应,一般使用逆向配平的方法,即先从氧化产物和还原产物开始配平。
例1 S+KOHK2S+K2SO3+H2O
分析
硫单质既是氧化剂又是还原剂,K2S是产物,K2SO3是产物。
(1)化合价的变化,生成“1个K2S”化合价价,生成“1个K2SO3”化合价价,化合价变化的最小公倍数为,因而K2S化学计量数为,K2SO3的化学计量数为。
(2)根据S原子守恒确定单质硫的化学计量数为。
(3)再根据K原子守恒配出KOH的化学计量数为。
(4)最后定H2O的化学计量数为。
1. (2024·河北衡水高一段考)以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2,其过程如下:
过程Ⅰ:Fe3O4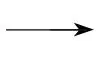 2(未配平);
2(未配平);
过程Ⅱ:FeO+H2OH2+Fe3O4(未配平)。下列说法错误的是( )
A.过程Ⅰ的反应中还原产物是FeO
B.过程Ⅰ的反应中每生成12个FeO转移8个电子
C.该方法制H2具有成本低、产物易分离等优点
D.过程Ⅱ的反应中FeO和H2O的化学计量数之比为2∶1
题型2 离子方程式的配平
首先根据得失电子守恒和质量守恒配平氧化剂、还原剂和氧化产物、还原产物,根据电荷守恒配平离子方程式两边电荷数,最后根据原子守恒配平未变价元素的原子。
例2 Mn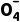 +H++H2O2===Mn2++O2↑+H2O
+H++H2O2===Mn2++O2↑+H2O
分析
先根据得失电子守恒确定氧化剂Mn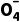 、还原剂H2O2、还原产物Mn2+、氧化产物O2的化学计量数分别是、、、; 根据电荷守恒确定H+的化学计量数为,根据H原子守恒确定H2O的化学计量数为,最后用O原子守恒检验。
、还原剂H2O2、还原产物Mn2+、氧化产物O2的化学计量数分别是、、、; 根据电荷守恒确定H+的化学计量数为,根据H原子守恒确定H2O的化学计量数为,最后用O原子守恒检验。
2.(2023·湖北孝感一中高一期中)已知在碱性条件下,发生反应:Fe3++ClO-+OH-
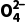 +Cl-+H2O(未配平)。
+Cl-+H2O(未配平)。
(1)Fe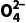 中铁元素化合价为。
中铁元素化合价为。
(2)Fe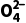 是(填“氧化”或“还原”)产物。
是(填“氧化”或“还原”)产物。
(3)配平该离子方程式:___________________________________________________。
题型3 缺项配平类[一般缺的为酸(H+)、碱(OH-)、水]
(1)先将得失电子数配平,再观察两边电荷。若反应物这边缺正电荷,一般加H+,生成物一般加水;若反应物这边缺负电荷,一般加OH-,生成物一般加水,然后根据两边电荷数进行配平。
(2)当化学方程式中有多个缺项时,应根据化合价的变化找准氧化剂、还原剂、氧化产物、还原产物。
例3 Mn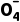 +I-+
+I-+ Mn2++I2+H2O
Mn2++I2+H2O
3.NaNO2是一种食品添加剂,能致癌。酸性高锰酸钾溶液与亚硝酸钠反应的离子方程式是Mn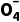 +N
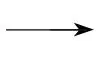
+N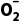 +
+
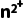 +N
+N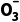 +H2O。下列叙述正确的是( )
+H2O。下列叙述正确的是( )
A.该反应中N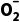 被还原
被还原
B.反应过程中溶液的pH变小
C.生成1 mol NaNO3需要消耗0.4 mol KMnO4

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/1PNDK7_UY-I6aOdOvfo5O5Q?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享