
[核心素养发展目标]1.熟练以物质的量为中心的计算与转换。2.利用化学方程式找出各物质的量的关系并进行计算。
一、以物质的量为中心的计算
1.物质的量是联系宏观量(如质量、体积)与微观量(如粒子数目)的桥梁和纽带:
2.要紧紧抓住“物质的量”这个计算的核心。牢固建立把“其他物理量转化为物质的量”的这一思维模式,充分利用下列“万能恒等式”及其变形,进行各物理量的相互求算:
n=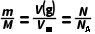 =c·V(aq)
=c·V(aq)
3.在解题的过程中,根据条件找出已知量与未知量之间的物质的量关系,就可使复杂的问题简单化、技巧化。其解题方法是依据变化前后某一粒子物质的量保持不变,列出守恒关系求解。
1.(2024·江苏南通海门中学高一期末)过氧乙酸消毒液是一种常见的消毒剂。如图为实验室中过氧乙酸消毒液试剂瓶标签上的有关数据,下列说法不正确的是( )
A.3.01×1023个过氧乙酸分子中所含碳原子的物质的量约为1 mol
B.过氧乙酸中C、H、O三种元素的质量之比为6∶1∶12
C.过氧乙酸消毒液的物质的量浓度为2.28 mol·L-1
D.该消毒液中过氧乙酸的物质的量为11.4 mol
2.(2024·江苏南通高一上段考)(1)在标准状况下,①6.72 L CH4;②3.01×1023个HCl分子;③13.6 g H2S;④0.2 mol NH3。下列关系表达正确的是(填字母)。
a.体积:②>①>③>④
b.密度:②>③>④>①
c.质量:②>①>③>④
d.氢原子个数:①>③>④>②
(2)8.4 g N2与9.6 g Rx的分子数目之比为3∶2,原子数目相同。则9.6 g Rx的物质的量为 mol。x值为,R的相对原子质量是。
二、依据化学方程式的计算
1.化学反应计算的方法
2CO + O2 2CO2
2CO2
化学计量数2
物质的量2 mol
(1)同一个化学方程式中各物质的化学计量数之比等于其之比。
(2)对于有气体参加的反应,在同温同压下各气体的化学计量数之比等于其之比。
例1实验室为确定一瓶稀盐酸的浓度,用0.100 mol·L-1 NaOH溶液中和25.00 mL该盐酸,当酸与碱恰好完全反应时,消耗NaOH溶液24.50 mL,试求该盐酸的物质的量浓度。
_______________________________________________________________________________________
_______________________________________________________________________________________
2.依据化学方程式列方程组法
方程组法用于解决两种物质的混合物计算,读题时找到两个已知量时,利用各物质的关系建立二元一次方程组求算未知量。
例2(2024·河北唐山高一检测)氧气与碳在一定条件下发生反应可以生成CO和CO2。在标准状况下,18.8 g CO与CO2的混合气体体积为11.2 L。则:
(1)CO和CO2的物质的量之比是。
(2)CO的质量是 g。
3.依据反应前后的差量计算
根据化学反应前后物质的有关物理量发生的变化,找出所谓的“理论差量”,如反应前后的质量差、物质的量差、气体体积差等,该差量与反应物的有关量成正比。差量法就是借助这种比例关系求解的方法。
例3把铁棒插入CuSO4溶液,一段时间后取出,铁棒质量增加了4 g,参加反应的Fe的质量为。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/1PNDK7_UY-I6aOdOvfo5O5Q?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享