
[核心素养发展目标] 1.掌握从海水中提取镁的原理和过程,了解镁的性质及用途。2.掌握从海带中提取碘的原理和过程,掌握加碘盐中碘元素的检验方法,了解碘在生活中的应用。
一、从海水中提取镁
1.镁的存在
自然界中的镁主要以的形式存在于和中。
2.镁的提取
(1)工艺流程
(2)相关反应的化学方程式
①分解贝壳制取氢氧化钙:________________________________________________________;
________________________________________________________。
②沉淀镁离子:________________________________________________________。
③制备氯化镁:________________________________________________________。
MgCl2·6H2OMgCl2+6H2O。
④制取金属镁:________________________________________________________。
3.镁的原子结构与性质
(1)原子结构
(2)物理性质
镁是色金属,密度,易传热,导电,能与铜、铝等金属形成合金。
(3)化学性质
镁是活泼金属,能在O2、N2、CO2中燃烧,可以和酸(如HCl、HNO3等)发生反应。写出下列反应的化学方程式:
4.镁的用途
(1)镁能与铜、铝等金属形成合金。镁合金的密度、硬度和强度,被广泛用于制造火箭、导弹和飞机的部件等。
(2)氧化镁是难溶于水的固体,熔点,常用作材料。
1.正误判断
(1)镁在空气中燃烧只能生成MgO( )
(2)镁着火时能用干冰灭火器灭火( )
(3)沉淀海水中的Mg2+宜选用廉价的熟石灰( )
(4)海水中提取Mg既涉及复分解反应又涉及置换反应( )
2.镁粉可用来制造焰火,工业上制取镁粉的方法是将镁的蒸气进行冷却,其中最适宜的方法是( )
A.在氮气的容器内冷却
B.在空气中冷却
C.在氦气的环境里冷却
D.在二氧化碳气体里冷却
3.海水提取镁的主要流程如下:
下列说法正确的是( )
①试剂M是盐酸 ②流程中的反应全部都是非氧化还原反应 ③操作b只是过滤 ④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2⑤电解熔融MgCl2比电解熔融的MgO制金属镁更节约能量
A.①②③④⑤B.②③
C.④⑤D.①④⑤
二、从海带中提取碘
1.从海带中提取碘的原理
(1)目前工业上并不直接通过海水提取碘(海水中I-的),而是以具有富集碘能力的海藻(如海带等)为原料获取碘。
(2)海带中所含的碘元素在浸泡时以碘离子(I-)的形式进入水中,可选择、等氧化剂把浸出液中的碘离子氧化成碘单质,离子方程式分别为、。
(3)现代工业上也用处理含碘离子的溶液以提高碘的提取率。
2.从海带中提取碘的工艺流程
3.加碘盐中碘元素的检验
(1)加碘盐中碘元素的存在形式:________________________________________________________。
(2)检验原理
在酸性条件下,I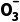 与I-反应的离子方程式:I
与I-反应的离子方程式:I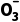 +5I-+6H+===3I2+3H2O,生成的单质碘用淀粉溶液检验,现象是。
+5I-+6H+===3I2+3H2O,生成的单质碘用淀粉溶液检验,现象是。
(3)用试纸和生活中常见的物质检验加碘盐中碘元素存在的方案:
食盐酸性溶液试纸变蓝,证明有碘元素存在。
特别提醒碘是维持人体甲状腺正常功能所必需的元素,缺碘会导致甲状腺肿大,食用过多的碘盐或含碘食品,对健康也不利。
1.正误判断
(1)工业上是把海水中的碘用氧化剂氧化提取I2( )
(2)海带中含有碘,能使淀粉变蓝( )
(3)加碘盐中的碘元素被氧化为碘单质后,才能检验( )
(4)医用碘酒可用于人体补碘( )
(5)用Cl2、H2O2等氧化I-前需先用酸酸化( )

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/1PNDK7_UY-I6aOdOvfo5O5Q?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享