
[核心素养发展目标]1.能从宏观和微观相结合的角度理解影响物质体积大小的因素。2.理解气体摩尔体积的含义,能进行标准状况下气体体积、物质的量及微粒数目、质量等的换算。3.理解阿伏加德罗定律及其推论,并能运用阿伏加德罗定律及其推论解决简单问题。
一、决定物质体积大小的因素
1.不同聚集状态物质的微观结构与宏观性质
聚集状态 | 微观结构 | 微粒的运动方式 | 宏观性质 |
固态 | 微粒排列,微粒间的空隙 | 在固定的位置上 | 有的形状,被压缩 |
液态 | 微粒排列,微粒间的空隙 | 可以自由 | 没有固定的形状,被压缩 |
气态 | 微粒间的距离 | 可以自由 | 没有固定的形状,被压缩 |
思考讨论不同宏观物质的物理性质可能存在哪些差异?可能的原因是什么?
_______________________________________________________________________________________
_______________________________________________________________________________________
2.分析不同聚集状态物质的体积
已知下列物质的密度,试计算1 mol这些物质的体积,将结果填入下表(说明:固体、液体密度均为293 K时的测定值,气体密度为1.01×105 Pa、273 K时的测定值)。
1 mol不同物质的体积
物质 | 摩尔质量/(g·mol-1) | 密度 | 1 mol物质的体积 |
Al | 26.98 | 2.70 g·cm-3 | |
Fe | 55.85 | 7.86 g·cm-3 | |
H2O | 18.02 | 0.988 g·cm-3 | |
C2H5OH | 46.07 | 0.789 g·cm-3 | |
H2 | 2.016 | 0.089 9 g·L-1 | |
N2 | 28.02 | 1.25 g·L-1 | |
CO | 28.01 | 1.25 g·L-1 | |
结论:(1)相同条件下1 mol固体、液体的体积。
(2)同温同压下,1 mol气体的体积 。
3.影响物质体积大小的因素
气态物质中微粒间的距离与外界温度、压强有关。因此,当温度、压强一定时,任何具有相同的气体都具有大致相同的。
1.正误判断
(1)一定温度、压强下,气体体积由其分子的大小和数目决定( )
(2)当压强一定时,温度越高,气体分子间的距离越大;温度一定时,压强越大,气体分子的距离越大( )
(3)1 mol一氧化碳和1 mol氧气所含的分子数相同,体积也相同( )
2.(2023·福建泉州高一期中)同温同压下,两种气体的体积不相同,其主要原因是( )
A.分子大小不同B.分子间距离不同
C.性质不同D.分子数不同
二、气体摩尔体积
思考1对一定量气体体积的探究。已知1mol不同气体在不同条件下的体积:
化学式 | 条件 | 1mol气体体积/L |
H2 | 0℃,101kPa | 22.4 |
O2 | 0℃,101kPa | 22.4 |
CO | 0℃,101kPa | 22.4 |
H2 | 0℃,202kPa | 11.2 |
CO2 | 0℃,202kPa | 11.2 |
N2 | 273℃,202kPa | 22.4 |
NH3 | 273℃,202kPa | 22.4 |
(1)从上表分析得出结论:
①1mol任何气体,在标准状况下的体积都约为。
②1mol不同的气体,在不同的条件下,体积(填“一定”“一定不”或“可能”)相等。
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是① ,②。
1.气体摩尔体积
2.标准状况下的气体摩尔体积
即在标准状况下,气体摩尔体积约为。
思考2(1)标准状况下,1mol任何物质的体积都约是22.4L吗?
_______________________________________________________________________________________
_______________________________________________________________________________________
(2)当1mol气体的体积为22.4L时,能否说明该气体一定处于标准状况下?
_______________________________________________________________________________________
_______________________________________________________________________________________
(3)气体摩尔体积适用范围是气体,是否必须为纯净气体?
_______________________________________________________________________________________
_______________________________________________________________________________________
3.理解气体摩尔体积应注意的几个问题
(1)标准状况下的气体摩尔体积Vm=22.4 L·mol-1,非标准状况时不能使用。
(2)n=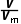 ,只适用于气态物质(单一或者混合气体),对于固态物质(如碳、三氧化硫等)或液态物质(如水、酒精等)均不适用。
,只适用于气态物质(单一或者混合气体),对于固态物质(如碳、三氧化硫等)或液态物质(如水、酒精等)均不适用。

通过网盘分享的文件:word讲义
链接: https://pan.baidu.com/s/1PNDK7_UY-I6aOdOvfo5O5Q?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享