
第一节 原子结构与元素周期表
第1课时 原子结构
[核心素养发展目标]1.了解原子的表示方法,掌握有关质量数、质子数、中子数、电子数的相关计算。2.能从微观角度认识原子的构成,掌握原子核外电子排布规律,能画出1~20号元素的原子结构示意图。
一、原子的构成
1.构成原子的微粒及其性质
原子
2.质量数
(1)概念:将原子核内所有__________和__________的相对质量取近似__________,所得的数值叫做质量数,常用__________表示。
(2)构成原子的粒子间的两个关系
①质量数(A)=__________+__________。
②质子数=核电荷数=__________。
 思考1
思考1 原子的质量数是否就是原子的相对原子质量?请举例说明。
原子的质量数是否就是原子的相对原子质量?请举例说明。
3.原子的表示方法
原子 | 质子数(Z) | 中子数(N) | 表示方法 |
F | 9 | 10 | |
Na | 11 | 12 | |
Al | 13 | 14 | |
 思考2
思考2 填写下列表格并思考离子的核外电子数、质子数、电荷数之间的关系。
填写下列表格并思考离子的核外电子数、质子数、电荷数之间的关系。
粒子 符号 | 质子 数(Z) | 质量 数(A) | 中子 数(N) | 电荷数 | 核外电 子数 |
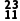 Na+ Na+
| 11 | 23 | | | |
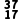 Cl- Cl-
| 17 | 37 | | | |
结论:阳离子中核外电子数=__________-__________;
阴离子中核外电子数=__________+__________。

1.判断正误
(1)原子呈电中性是因为中子不带电( )
(2)质子数和中子数决定原子的质量( )
(3)微粒中的质子数与核外电子数一定相等( )
(4)某种氯原子的中子数是18,则其质量数是35,核外电子数是17( )
2.(2024·福建泉州十六中高一月考)下列关于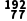 Ir的说法不正确的是( )
Ir的说法不正确的是( )
A.核内质子数是77B.核内中子数是192
C.核外电子数是77D.质量数是192
3.带有2个单位正电荷的粒子X2+,它的质量数等于137,中子数是81,则其核外电子数为( )
A.56 B.54 C.58 D.137
(1)一个信息丰富的符号解读

(2)粒子中的电性关系
①分子或原子:质子数=核外电子数
②阳离子Xn+:质子数=核外电子数+n
③阴离子Xn-:质子数=核外电子数-n
二、原子核外电子排布
1.电子层
(1)概念:在含有多个电子的原子里,电子分别在__________的区域内运动。我们把不同的区域简化为__________,也称作电子层。
如图为电子层模型示意图:
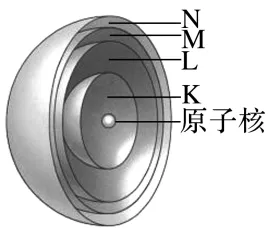
(2)不同电子层的表示及能量关系
各电子层由内到外 | 电子层数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
字母代号 | | | | | | | |
离核远近 | 由__________到__________ |
能量高低 | 由__________到__________ |
2.电子分层排布
阅读教材思考与讨论中稀有气体元素原子的电子层排布规律
(1)能量最低原理
核外电子总是优先排布在能量最低的电子层里,然后再由里往外排布在能量逐步升高的电子层里,即按K→L→M→N……顺序排列。
(2)电子层最多容纳的电子数
①第n层最多容纳__________个电子。如K、L、M、N层最多容纳的电子数分别为__________。

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享