
第1课时 元素性质的周期性变化规律
[核心素养发展目标]1.了解元素原子核外电子排布、原子半径、主要化合价的周期性变化,认识元素周期律并理解其实质。2.会设计实验探究同周期元素性质的变化规律,会比较元素的金属性或非金属性的强弱,促进“证据推理与模型认知”化学核心素养的发展。
一、核外电子排布、原子半径和主要化合价的变化
1.原子核外电子排布的周期性变化
以原子序数为1~18的元素为例,探究原子最外层电子数的变化,图示如下:
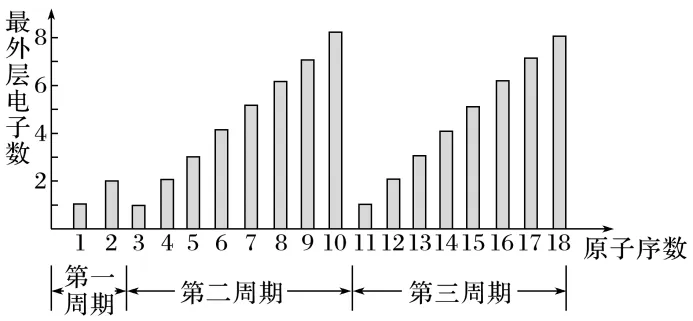
规律:随着原子序数的递增,元素原子的最外层电子排布呈现______的周期性变化(第一周期除外)。
2.原子半径的周期性变化
以第二、三周期元素为例,探究元素的原子半径的变化,图示如下:
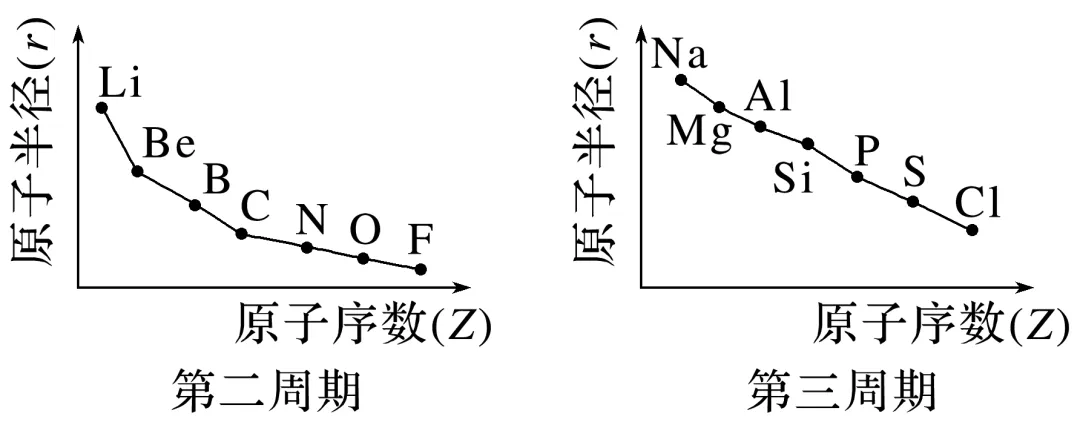
规律:随着原子序数的递增,元素的原子半径呈现__________的周期性变化。
 思考1
思考1 试比较下列微粒的半径大小(填“>”“<”或“=”)。
试比较下列微粒的半径大小(填“>”“<”或“=”)。
(1)Mg__________Ca__________K;
(2)PSCl;
(3)Fe3+Fe2+Fe;
(4)S2-Cl-Na+Mg2+。
“三看法”比较微粒半径的大小
一看层,层多径大;
二看核,层同核多径小;
三看电子,层同核同电子多径大,如Cl->Cl、Fe2+>Fe3+。
3.元素化合价的周期性变化
以原子序数为1~18的元素为例,探究元素化合价的变化,图示如下:
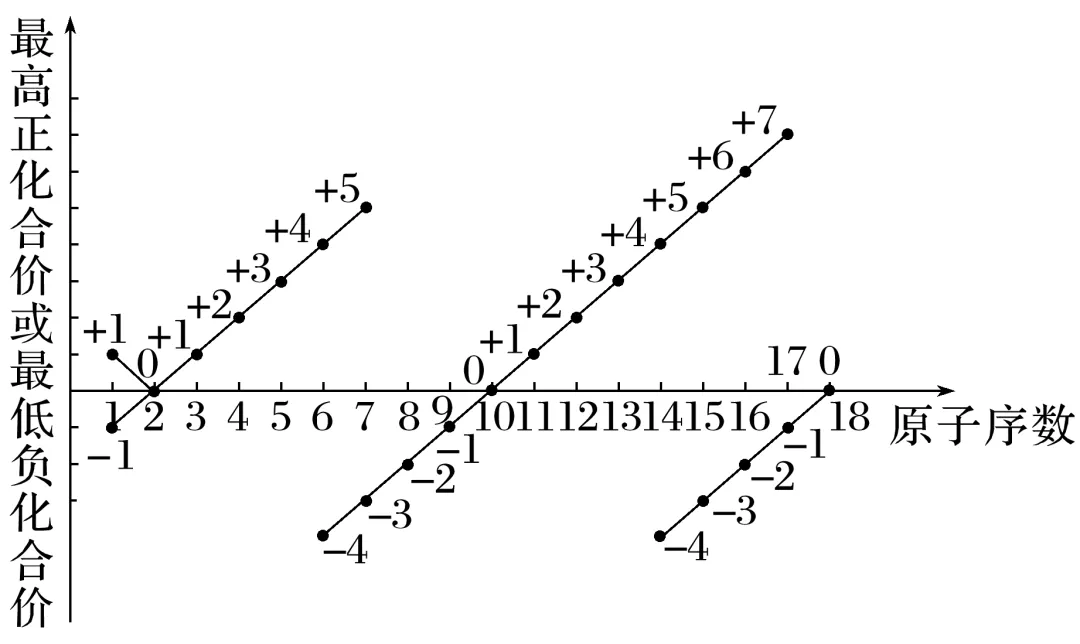
规律:随着原子序数的递增,元素的化合价呈__________变化,即每周期,最高正价为__________(O无最高正价、F无正价),负价为__________。
 思考2
思考2 主族元素的最高化合价等于其族序数,这句话对吗?为什么?
主族元素的最高化合价等于其族序数,这句话对吗?为什么?
主族元素主要化合价的确定方法
(1)最高正价=主族序数=最外层电子数(O、F除外)。
(2)最低负价=最高正价-8(H、O、F除外)。
(3)H的最高价为+1,最低价为-1。

1.判断正误
(1)第二周期元素从左至右,最高正价从+1递增到+7( )
(2)原子半径最小的元素是氢元素( )
(3)氢元素除了有+1价外,也可以有-1价,如NaH( )
(4)主族元素的最低负价等于其族序数-8( )
(5)第三周期原子半径最大的元素为钠( )
2.下列说法正确的是( )
A.原子序数越大,原子半径一定越大
B.电子层数多的原子半径一定比电子层数少的原子半径大
C.元素性质的周期性变化不是元素性质的简单重复
D.按C、N、O、F的顺序,元素的最高正化合价依次升高
3.(2024·海口长流中学高一月考)若某非金属元素X的最高价氧化物对应的水化物的化学式为HnXOm,则X元素的族序数为,它的最高价氧化物的化学式为,氢化物的化学式为。
二、同周期元素金属性和非金属性的递变规律
以第三周期元素为例探究元素性质的递变规律。
1.预测:元素性质的递变规律
第三周期元素电子层数__________,由左向右核电荷数依次增多,原子半径依次__________,失电子的能力依次__________,得电子的能力依次__________,预测它们的金属性依次__________,非金属性依次__________。
2.实验探究:金属性的递变规律
(1)Na、Mg元素金属性强弱比较
原理 | 金属与水反应置换出H2的难易程度 |
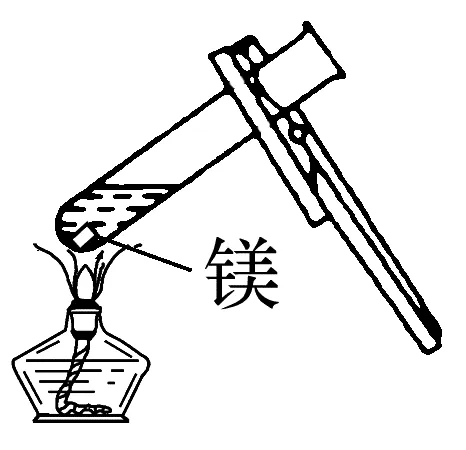
操作 | 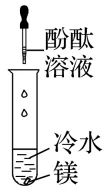
| 
|
现象 | 镁条表面附着__________ | 剧烈反应,溶液变成浅红色 |
化学反应 | - | Mg+2H2O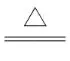 Mg(OH)2+H2↑ Mg(OH)2+H2↑ |
结论 | 结合Na与水的反应的现象,Na与水反应置换H2比Mg__________,则金属性:__________ |
(2)Mg、Al元素金属性强弱比较
原理 | 金属的最高价氧化物对应的水化物的碱性强弱 |
物质 | Al(OH)3 | Mg(OH)2 |

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享