
[核心素养发展目标]1.了解容量瓶的特点、用途及使用注意事项。2.掌握配制一定物质的量浓度的溶液的方法及操作,建立实验误差分析思维模型,并能应用模型解决实际问题。
一、一定物质的量浓度溶液的配制
1.主要仪器
托盘天平(或分析天平)、烧杯、__________、__________、__________、量筒。
2.容量瓶
 思考1
思考1 容量瓶使用前需要检验是否漏水吗,应该如何操作?
容量瓶使用前需要检验是否漏水吗,应该如何操作?
3.配制过程
以配制100 mL 1.00 mol·L-1 氯化钠溶液为例
 思考2
思考2 实验室需要配制480mL1.00mol·L-1的氢氧化钠溶液,则用托盘天平称量多少克氢氧化钠固体?
实验室需要配制480mL1.00mol·L-1的氢氧化钠溶液,则用托盘天平称量多少克氢氧化钠固体?
 思考3
思考3 现用98%的浓H2SO4(ρ=1.84g·cm-3)配制浓度为0.5mol·L-1的稀硫酸500mL。
现用98%的浓H2SO4(ρ=1.84g·cm-3)配制浓度为0.5mol·L-1的稀硫酸500mL。
(1)配制该溶液的步骤应该为计算、__________、__________、__________、移液、洗涤、定容、摇匀、装瓶。
(2)配制该溶液应选用的玻璃仪器有烧杯、玻璃棒、__________、胶头滴管和__________。
(3)所需浓H2SO4的体积为__________mL。

1.判断正误
(1)配制溶液时,可以用托盘天平称取10 g固体溶质( )
(2)要配制230 mL溶液,必须选择250 mL容量瓶( )
(3)配制一定物质的量浓度的稀盐酸时,用量筒量取9.82 mL浓盐酸( )
(4)在使用容量瓶配制NaOH溶液或稀H2SO4时,必须要等溶液恢复至室温再转移到容量瓶中( )
(5)配制好的溶液保存在容量瓶中备用( )
2.下列有关一定物质的量浓度溶液的配制说法不正确的是__________(填序号)。
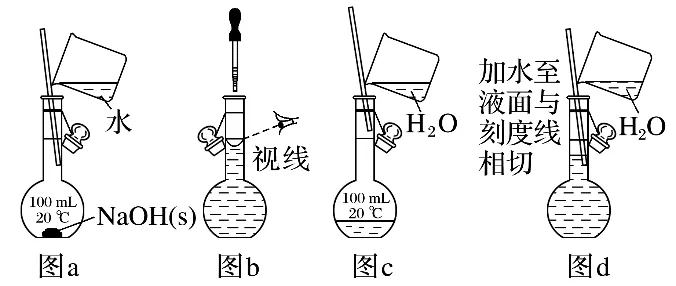
(1)为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至液面离刻度线1~2 cm时,改用胶头滴管滴加蒸馏水至刻度线;
(2)利用图a配制一定物质的量浓度的NaOH 溶液;
(3)利用图b配制一定物质的量浓度的NaCl溶液;
(4)利用图c配制一定物质的量浓度的NaNO3溶液;
(5)用容量瓶配制溶液时,若加水超过刻度线,立即用胶头滴管吸出多余液体;
(6)配制溶液的定容操作可以用图d表示。
二、配制一定物质的量浓度的溶液的误差分析
1.误差分析的原理依据
根据cB=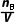 =
=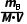 判断。其他条件不变时:
判断。其他条件不变时:
(1)使nB、mB增大(或减小)的因素,导致cB__________(或__________)。
(2)使V增大(或减小)的因素,导致cB__________(或__________)。
2.配制100mL1.00mol·L-1的氯化钠溶液常出现的误差
能引起误差的操作 | 因变量 | c |
n | V |
称量 | ①少量氯化钠粘在称量纸上 | | 不变 | |
②使用游码,且药品砝码位置颠倒 | | 不变 | |
移液 | ③有少量液体溅出 | | 不变 | |
④容量瓶内有少量水 | | | |

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享