
[核心素养发展目标]1.通过实验认识Na2CO3、NaHCO3的性质,培养科学探究意识。2.了解焰色试验的操作与应用。
一、碳酸钠和碳酸氢钠
1.Na2CO3、NaHCO3性质探究
(1)探究Na2CO3、NaHCO3的溶解性及水溶液的酸碱性
在两支试管中分别加入少量Na2CO3和NaHCO3(各约1 g),完成下列实验,并将实验现象和相应的结论填入表中。
盐 | Na2CO3 | NaHCO3 |
①观察两支试管中碳酸钠、碳酸氢钠的形态 | __________ | 细小的白色晶体 |
②加几滴水并将温度计伸入其中 | 加水后__________,温度计示数__________ | 加水后__________溶解,温度计示数__________ |
③继续向②的试管中分别加5 mL水,用力振荡 | 振荡一段时间后可溶解 | 固体量减少 |
④分别向③所得溶液中滴加1~2滴酚酞溶液 | 溶液__________,溶液碱性较强 | 溶液__________,溶液碱性较弱 |
初步结论 | 碳酸钠、碳酸氢钠均__________溶于水,水溶液均呈__________性,但Na2CO3的溶解度更__________,碱性更__________ |
 思考1
思考1 Na2CO3粉末遇水生成碳酸钠晶体(Na2CO3·xH2O),且在干燥空气中失去结晶水变成碳酸钠粉末,那么钠露置在空气中,最终会完全转变成什么?
Na2CO3粉末遇水生成碳酸钠晶体(Na2CO3·xH2O),且在干燥空气中失去结晶水变成碳酸钠粉末,那么钠露置在空气中,最终会完全转变成什么?
 思考2
思考2 向饱和的Na2CO3溶液中通入过量的CO2,会有什么现象?试分析其原因?
向饱和的Na2CO3溶液中通入过量的CO2,会有什么现象?试分析其原因?
(2)碳酸钠、碳酸氢钠热稳定性的实验探究
实验操作 | 实验现象 | 实验结论 |
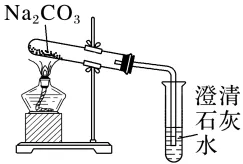
| 澄清石灰水__________ | __________ |
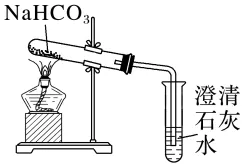
| 澄清石灰水__________ | __________;化学方程式:____________________ |
 思考3
思考3 用套管实验装置可以更好地比较Na2CO3和NaHCO3的热稳定性,其中小试管内有沾有无水硫酸铜粉末的棉花球,实验装置如图。
用套管实验装置可以更好地比较Na2CO3和NaHCO3的热稳定性,其中小试管内有沾有无水硫酸铜粉末的棉花球,实验装置如图。
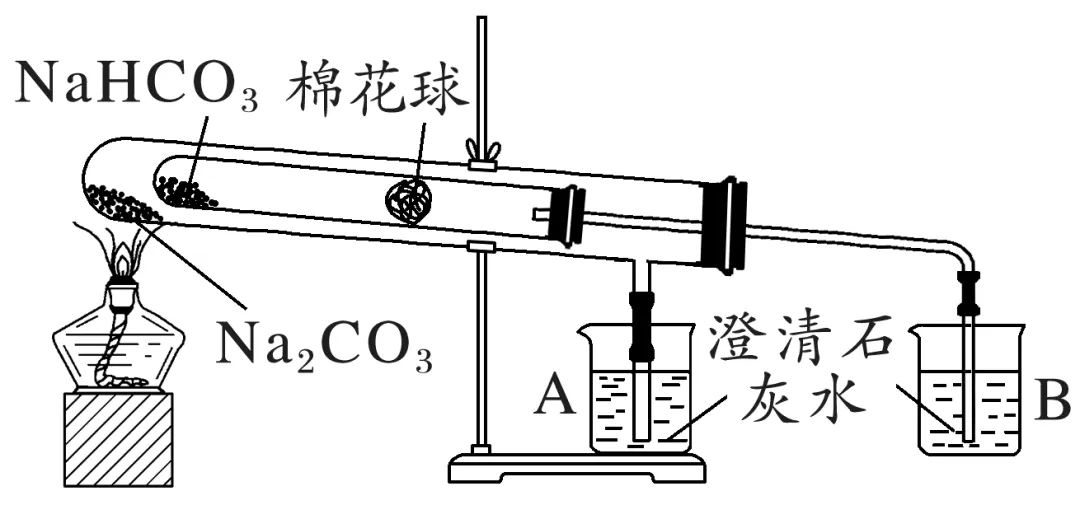
(1)实验时,小试管内棉花球上的无水硫酸铜由白色变为蓝色,说明NaHCO3受热分解生成了__________,烧杯B中澄清石灰水变浑浊,说明NaHCO3受热分解生成了__________。
(2)实验时,烧杯A中澄清石灰水不变浑浊,而烧杯B中澄清石灰水变浑浊,由此可得热稳定性:Na2CO3__________(填“>”或“<”)NaHCO3。
答案 (1)H2O CO2 (2)>
(3)探究Na2CO3和NaHCO3与稀盐酸的反应
实验步骤 | 在两支试管中分别加入3 mL同一稀盐酸,将两个分别装有0.3 g Na2CO3和0.3 g NaHCO3固体的小气球套在两支试管口,将气球内固体同时倒入试管中,观察现象 |
实验操作 | 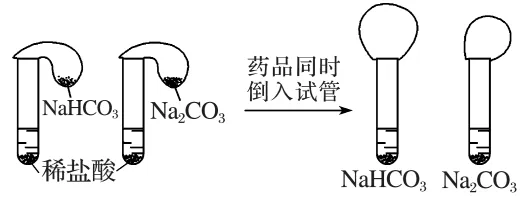
|
实验现象及结论 | 两支试管中都产生无色__________,气球__________,加入碳酸氢钠的试管中气泡产生得__________,气球膨胀得更大, 离子方程式分别为__________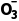 ____________________、__________ ____________________、__________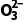 ____________________ ____________________ |
 思考4
思考4 某课外小组在实验中,将盐酸滴加到碳酸钠溶液中,开始无气泡产生,一段时间后产生气泡。试分析其原因?
某课外小组在实验中,将盐酸滴加到碳酸钠溶液中,开始无气泡产生,一段时间后产生气泡。试分析其原因?
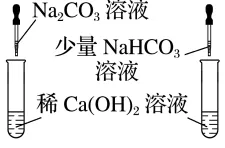
(4)探究Na2CO3、NaHCO3和盐(CaCl2)及碱[Ca(OH)2]的反应
| 盐(CaCl2) | 碱[Ca(OH)2] |
实验操作及步骤 | 
| 
|
现象及结论 | ①加入稀Na2CO3溶液,立即产生白色沉淀,离子方程式: ____________________; ②加入少量稀NaHCO3溶液,无明显现象,说明稀CaCl2溶液和少量稀NaHCO3溶液__________ | 两支试管中都产生__________。离子方程式分别为____________________、 ______________________________ |
 思考5
思考5 (1)试写出足量的NaHCO3溶液和少量Ca(OH)2反应的离子方程式。
(1)试写出足量的NaHCO3溶液和少量Ca(OH)2反应的离子方程式。

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享