《药品仓储与配送》-普通药品收货 学习笔记
- 2026-04-13 07:03:00
最近在学习王晓梅老师主编的《药品仓储与配送》一书,往期见:
《药品仓储与配送》-熟悉药品仓库2 仓库消防安全管理制度 学习笔记
普通药品收货是一套环环相扣的标准化流程,并非孤立的操作环节,GSP对其的要求贯穿全程,从前期准备到最终的收货记录,每一步都有明确的合规准则。
完整的收货流程可分为收货资料核查、运输工具与状况检查、实物与外包装核对、待验区放置与交接、收货记录录入五大步骤,各步骤层层递进,缺一不可。
一、收货资料核查
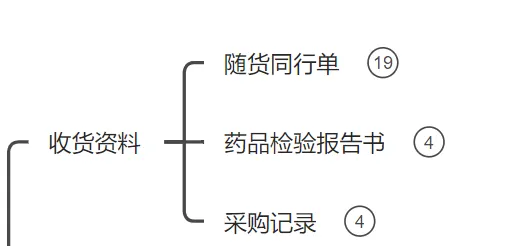
是GSP对药品流通溯源管理的硬性要求,核心是完成“三单核对”,即随货同行单(票)、药品检验报告书(单)、采购记录的一致性核验。
1、检查资料是否齐全,缺一不可;
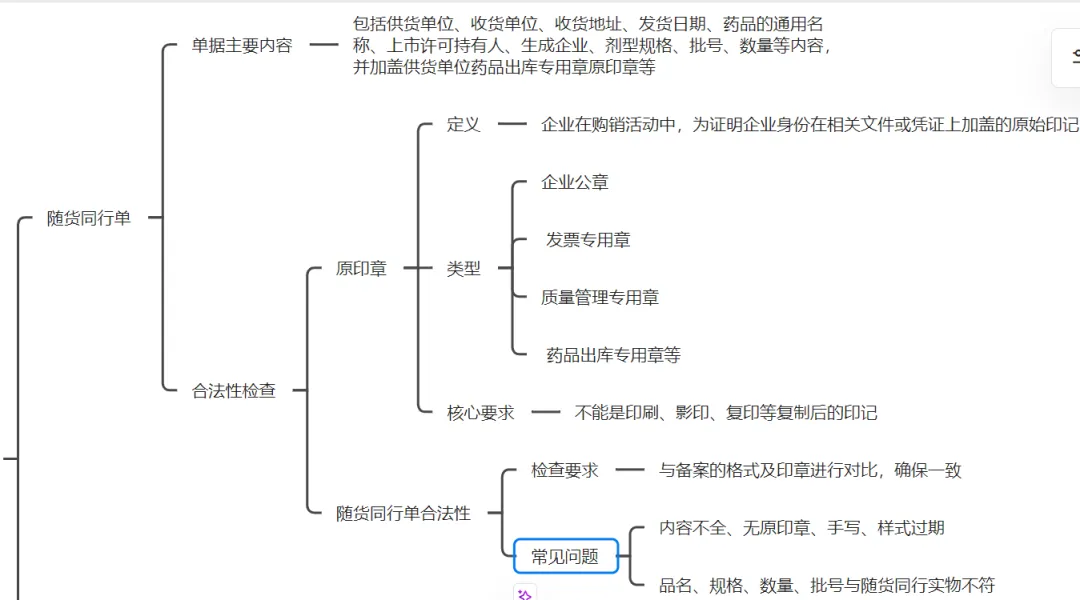
2、核查随货同行单(票)的合法性,需包含供货单位、收货单位、药品通用名称、上市许可持有人、生产企业、批号、数量等关键信息,且必须加盖供货单位药品出库专用章原印章。(现在也有企业采用电子随货同行单,问过药监领导,也是认可的,但是对于我们收货单位来说反而变得更加繁琐)。
3、逐字核对三份单据的核心信息,确保通用名称、规格、批号、数量、有效期至等内容完全一致,中药材、中药饮片还需核对产地信息,做到单单相符。

二、运输工具与运输状况检查
主要目的是保障药品在途质量未受影响,契合GSP对药品运输环节质量管控的要求。

1、药品卸车前,收货人员需现场检查运输车辆,首先确认运输工具为密闭式厢式货车;
2、其次检查车厢内部,不得有雨淋、腐蚀、污染、暴晒等可能影响药品质量的现象,车厢内整洁无杂物;
3、再核查运输单据载明的启运日期,确认是否符合与供货方协议约定的在途时限;
4、若为委托运输,需逐一核对实际承运方式、承运单位、车辆信息、启运时间与采购部门提前获取的资料是否一致,确保委托运输信息真实可查。
三、实物与外包装核对
这是严格遵循GSP“票货相符”的基本原则,操作上需做到“先拆防护、再查包装、最后核实物”。
1、首先拆除药品的运输防护包装,操作时轻拿轻放,避免药品落地或外包装破损;
2、随后对药品外包装进行全面查验,重点检查是否存在破损、渗漏、污染、封条损坏、标识模糊等问题,外包装上的药品信息需与单据一致;
3、最后逐批、逐箱核对实物,核心核对通用名称、剂型、规格、上市许可持有人、生产企业、批号、有效期至、数量等,做到票货一一对应。
四、待验区放置与签字交接
这是收货流程的衔接环节,需严格遵循GSP对药品待验管理的要求。
1、经以上步骤核查无误的药品,收货人员需用托盘将药品放置在指定的普通药品待验区,不得随意放置在其他区域;
2、随后收货人员在随货同行单(票)上清晰签署姓名与收货日期,完成与验收人员的现场交接,交接时需口头说明药品到货、核查的基本情况,验收人员确认后,收货人员方可完成该批次药品的现场收货操作。
五、收货记录录入
这是收货流程的收尾,也是GSP对药品经营“记录可溯”的核心要求,做到“没有记录,就没有发生”。收货人员需在完成现场交接后,及时录入收货记录。
六、异常情况处理
在标准化的收货流程中,异常情况的合规处置是检验实操能力与GSP落地效果的关键。以下是书中介绍的处理方法,实际操作中可能各个公司会根据实际情况采取不同的处理措施,公众号“GSP质管实务”中有好几篇文章详细写了具体操作,很实用,大家可以到其公众号中查看。
1、若出现无随货同行单(票)、无采购记录等资料缺失情况,书中是说直接拒收;
2、随货同行单内容不全、无出库专用章的,通知采购部门与供货方协调,补齐资料并核查无误后,方可继续收货;
3、印章与备案信息不一致的,立即上报质量管理部门处理,完成备案资料更换后再行操作。
4、若运输环节发现车厢污染、超时限运输、委托运输信息不符等问题,需暂停收货,第一时间通知采购部门并上报质量管理部门,由质量人员评估质量风险后制定处置方案。
5、若票货信息不符,除数量外的关键信息偏差,需由供货方确认并提供正确单据;
6、数量偏差需由采购部门调整采购数量。
7、若外包装出现破损、污染、标识不清等情况,直接拒收,从源头规避不合格药品进入仓储环节。
收货作为药品入库的第一道关口,将“资料必核、运输必查、实物必对、交接必签、记录必全”的要求内化为员工的操作习惯,才能真正筑牢质量防线,为后续的验收、储存、养护、配送环节打下坚实基础。
下期预告: 我们将学习《药品仓储与配送》模块二 ——冷藏、冷冻药品收货。
(本文基于王晓梅老师主编《药品仓储与配送》教材内容学习所著,结合个人对GSP规范的理解与行业实践进行的整合与阐述,旨在分享学习心得,非商业用途。)
