

第3课时 常见化学电源(二)——形形色色的燃料电池
[核心素养发展目标] 1.了解常见的氢氧燃料电池的种类,能正确书写电极反应式。2.了解气体燃料电池的工作原理。
一、常见氢氧燃料电池的种类及工作原理
1.燃料电池的概念
燃料电池是一种连续地将________和________的化学能直接转化为________的化学电源。
2.燃料电池的特点
(1)工作时,________和________连续地由外部供给并在电极上进行反应,生成物不断地被排出。
(2)能量转换率____(>80%),排放的废弃物______。
3.氢氧燃料电池
(1)基本构造
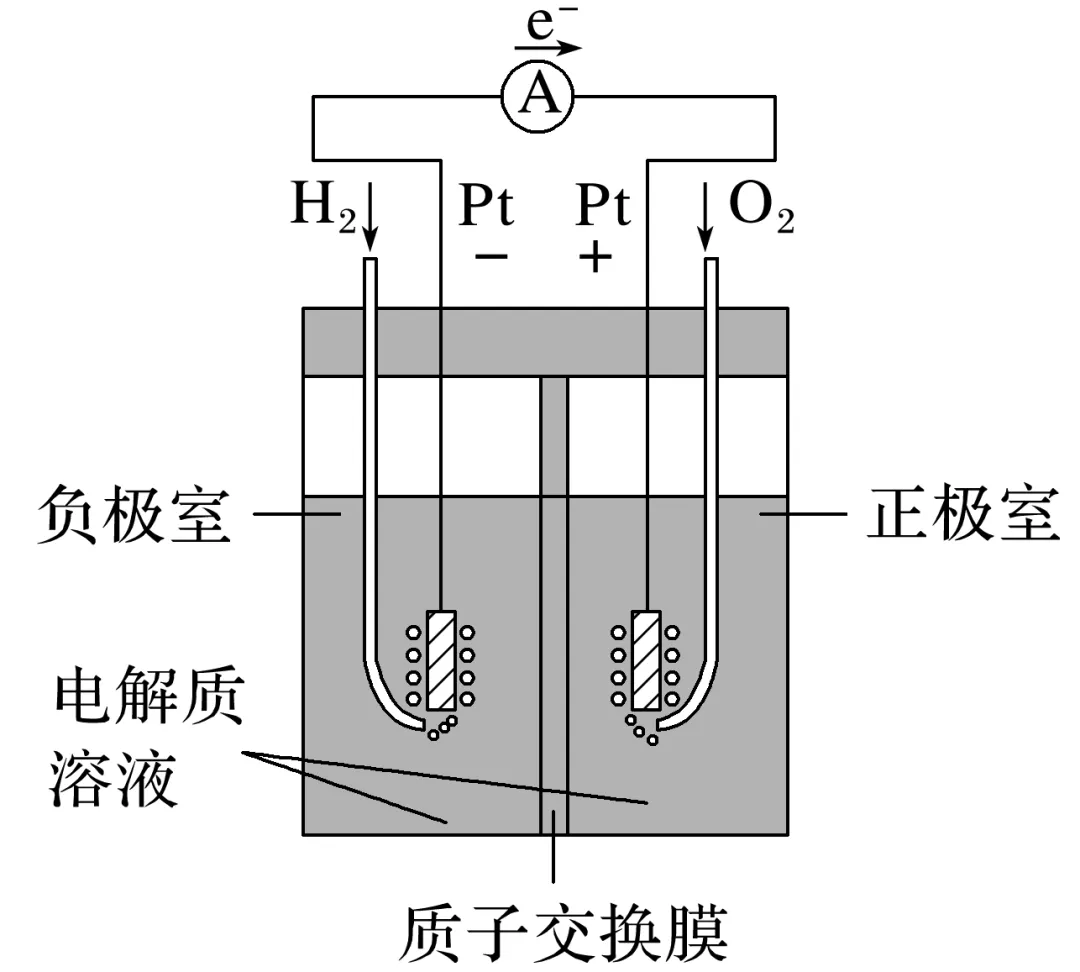
(2)工作原理
| 酸性电解质(H2SO4) | 碱性电解质(KOH) |
负极反应 | | |
正极反应 | | |
总反应 | |

1. 燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。
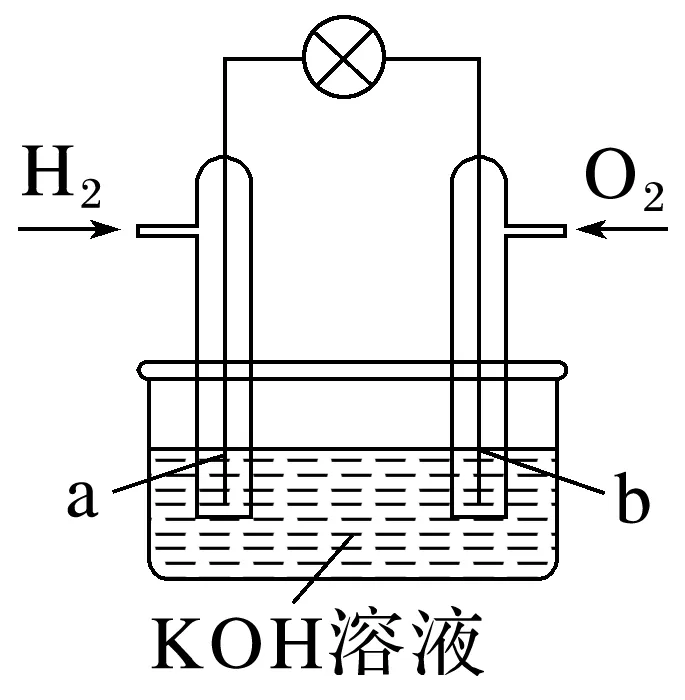
(1)负极是________(填“a”或“b”)。
(2)b极发生的电极反应式是________________________________________________
________________________________________________________________________。
(3)标准状况下,消耗11.2 L H2时,转移的电子数为________。
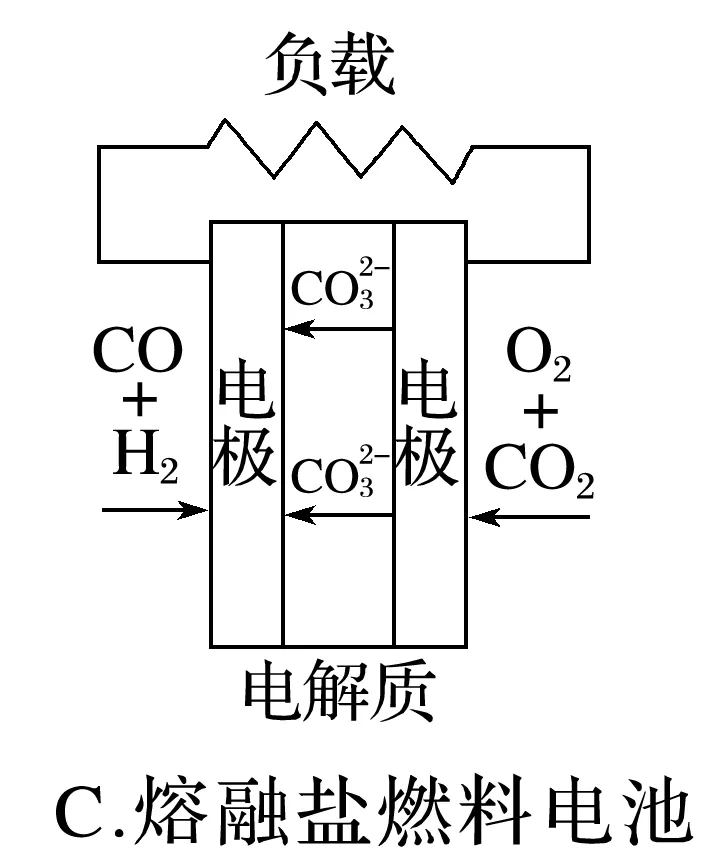
2.下面为3种燃料电池的工作原理示意图。
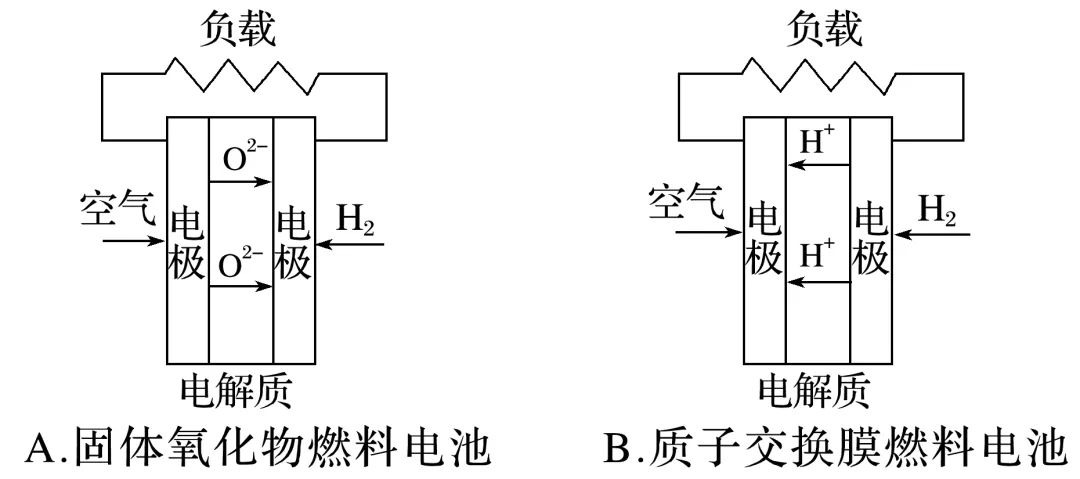
(1)A中,电池内部传导的离子是______,负极的电极反应式为_________________________。
(2)B中,电池内部传导的离子是______,正极的电极反应式为_________________________。
(3)C中,电池内部传导的离子是______,正极的电极反应式为_________________________。
二、其他新型燃料电池
1.甲烷燃料电池成本远低于以氢气为燃料的传统燃料电池。
(1)在酸性介质中
负极反应式:__________________________________________________________________;
正极反应式:__________________________________________________________________;
总反应式:____________________________________________________________________。
(2)在碱性(KOH溶液)介质中
负极反应式:__________________________________________________________________;
正极反应式:__________________________________________________________________;
总反应式:__________________________________________________________________。

在酸性介质和碱性介质中甲烷燃料电池的总反应不同,酸性条件下,+4价碳元素全部转化为CO2,碱性条件下,+4价碳元素全部转化为CO2-3。
2.一种固体电解质燃料电池的构造示意图如图所示。该电池以稀土金属材料作电极,两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。
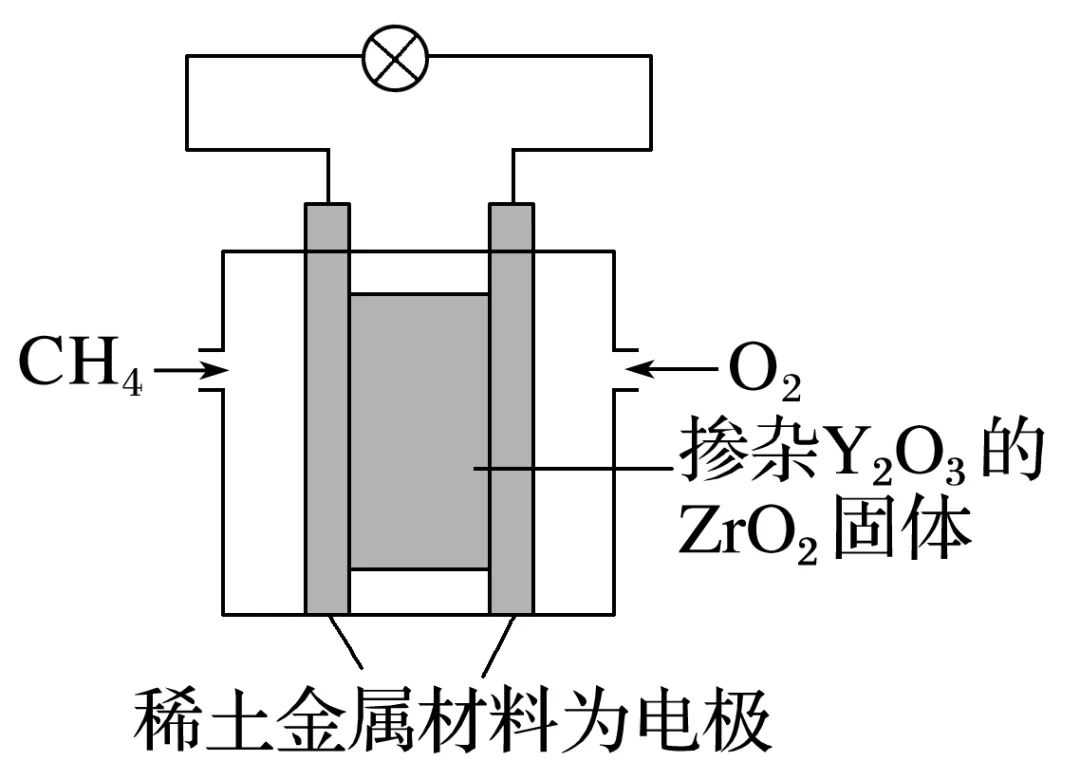
负极反应式:__________________________________________________________________;
正极反应式:__________________________________________________________________;
总反应式:____________________________________________________________________。
3.一种熔融碳酸盐燃料电池工作原理示意如图所示。
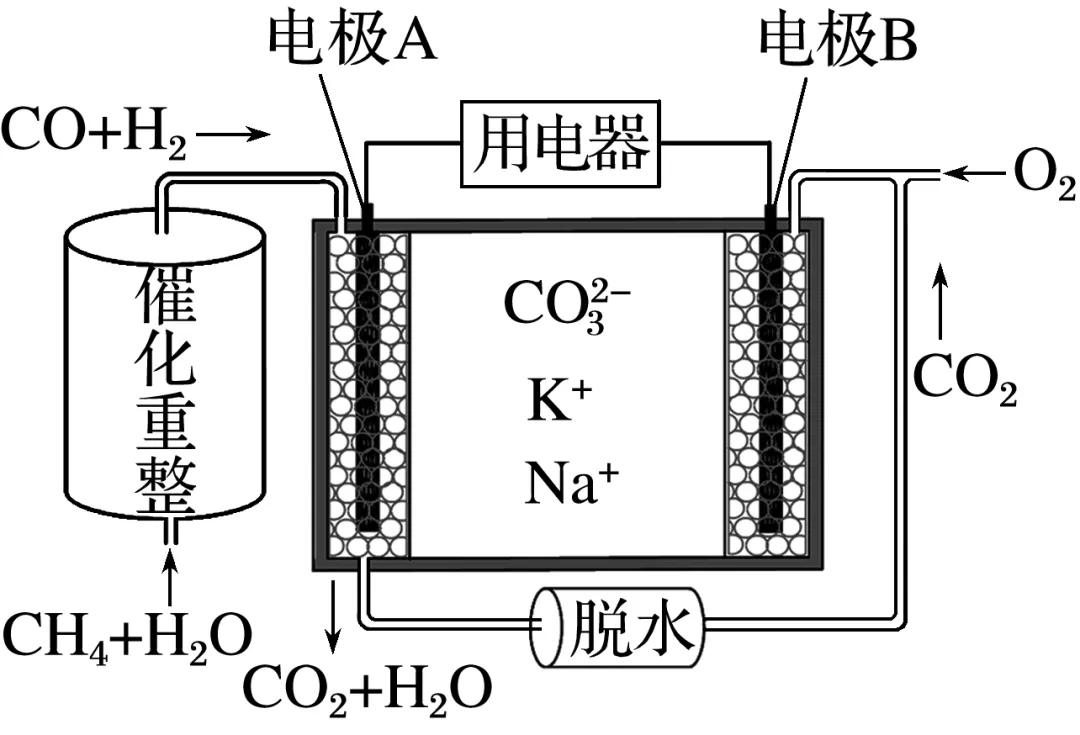
(1)电池工作时,外电路上电流的方向应从电极________(填“A”或“B”,下同)流向用电器。
(2)CO2-3向电极________移动。
(3)电极A上CO参与的电极反应为___________________________________________。

燃料电池电极反应式书写的方法
第一步:写出燃料电池反应的总反应式
燃料电池的总反应与燃料的燃烧反应一致,若产物能和电解质反应,则总反应为加和后的反应。
第二步:写出电池的正极反应式
正极一般为氧气得电子,介质不同时其电极反应式有所不同,如:
酸性电解质溶液:O2+4H++4e-===2H2O;
碱性电解质溶液:O2+2H2O+4e-===4OH-;
固体电解质(高温下能传导O2-):O2+4e-===2O2-;
熔融碳酸盐(如熔融K2CO3):O2+2CO2+4e-===2CO2-3。
第三步:根据电池总反应式和正极反应式,写出负极反应式。电池反应的总反应式-电池正极反应式=电池负极反应式。因为O2不是负极反应物,因此两个反应式相减时要彻底消除O2。

1.甲醇是重要的工业原料,利用甲醇设计的燃料电池具有启动快、效率高等优点,该电池的电解质为H2SO4溶液。下列说法正确的是( )
A.负极区溶液的pH减小
B.溶液中SO2-4向正极移动
C.正极反应式为2H++2e-===H2↑
D.该电池工作时,消耗1 mol CH3OH的同时生成11.2 L CO2(标准状况)
2.某学习小组以肼(N2H4)为原料设计了一种燃料电池,构造如图所示。其中两个电极均为铂电极,电池的总反应方程式为N2H4+O2===N2+2H2O。下列说法错误的是( )
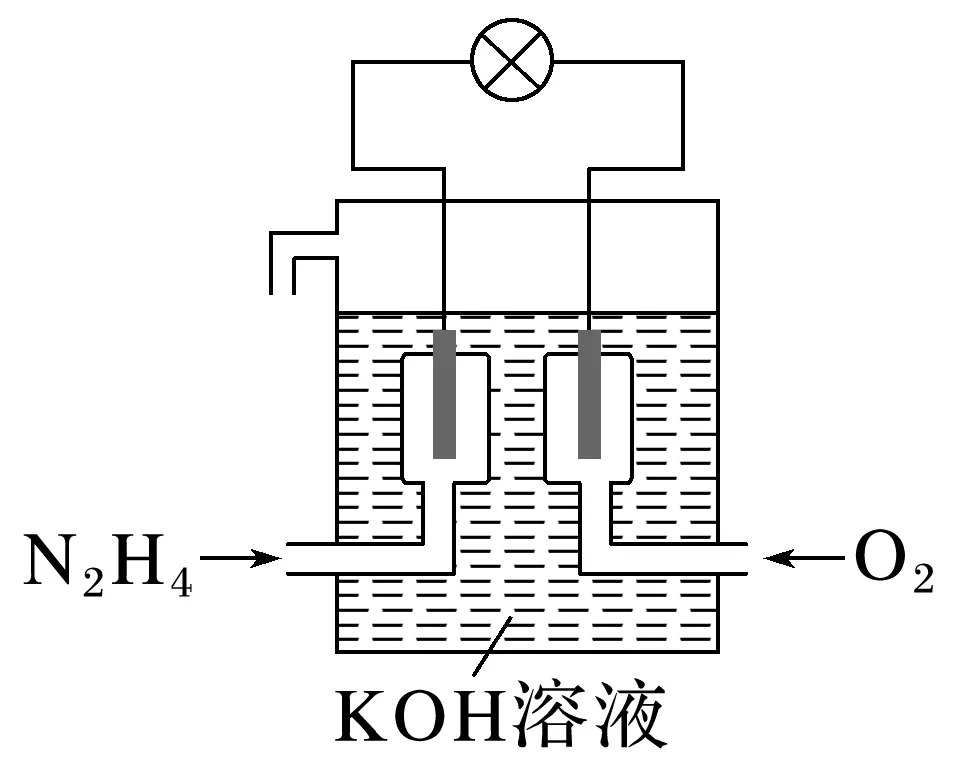
A.通入N2H4的一极是电池的负极
B.通入O2的电极反应式为O2+2H2O+4e-===4OH-
C.电池工作一段时间后电解质溶液的pH将变大
D.若消耗16 g N2H4,则理论上转移2 mol电子
3.热电厂尾气经处理得到较纯的SO2,可用于原电池法生产硫酸。下列说法不正确的是( )
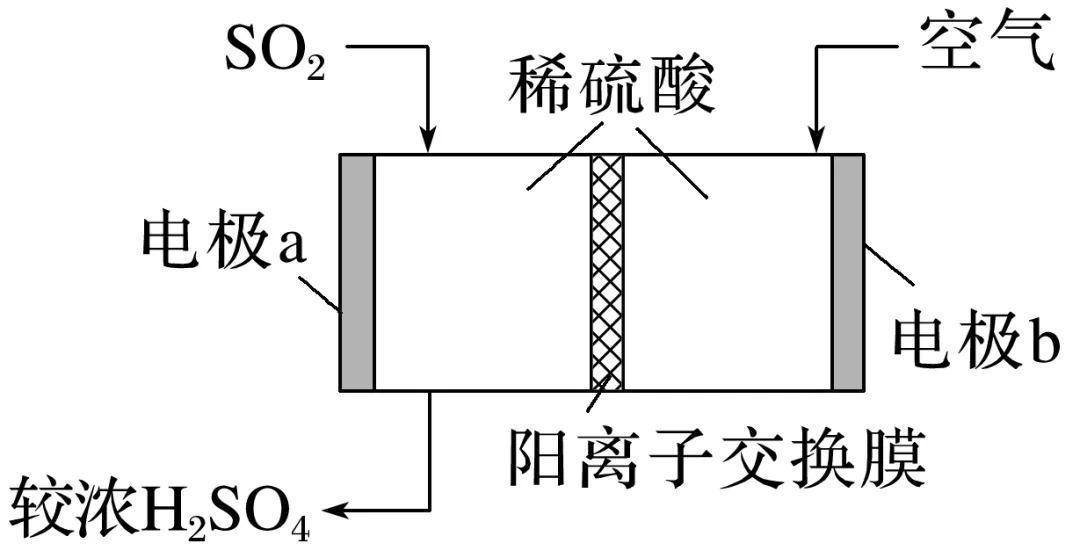
A.电极b周围溶液pH变大
B.溶液中H+由a极区向b极区迁移
C.电极a的电极反应式是SO2-2e-+2H2O===4H++SO2-4
D.一段时间后,a极消耗的SO2与b极消耗的O2物质的量相等

通过网盘分享的文件:同步PPT课件等3个文件
链接: https://pan.baidu.com/s/1WiBBQCVHpFgaci5JN4S3LA?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享