今天我们讨论的题目是PK/PD,即药代动力学和药效学指导的抗生素治疗。
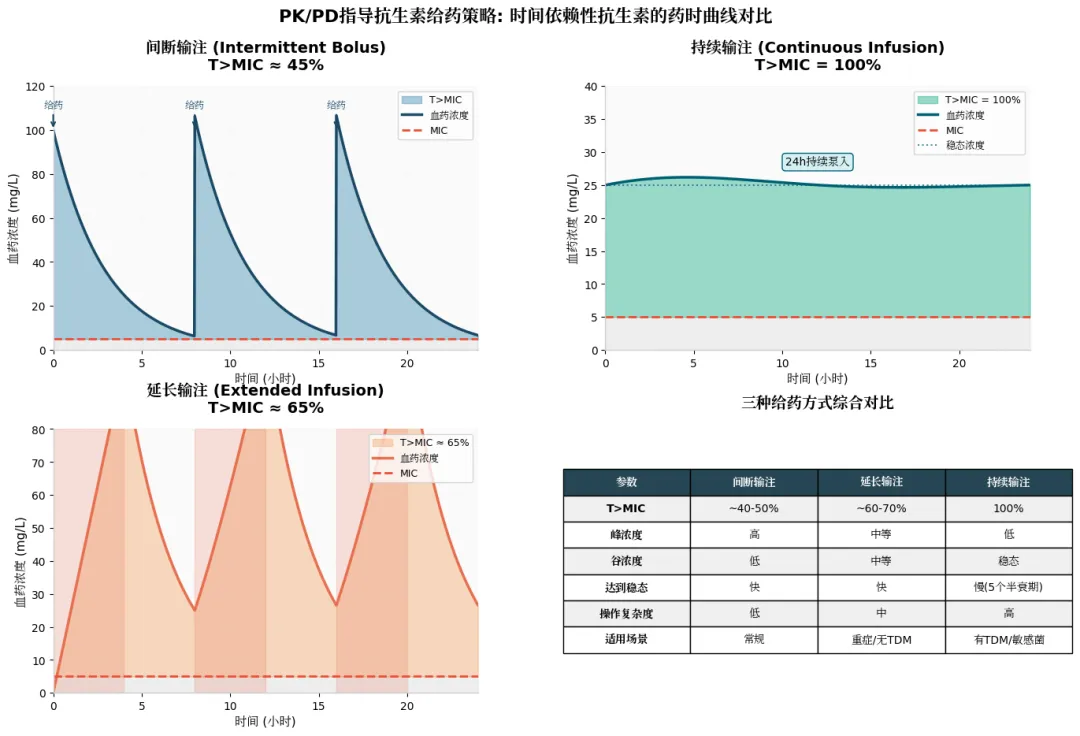
首先讨论支持抗生素持续输注的理论与证据。抗生素主要分为浓度依赖性和时间依赖性两大类。对于时间依赖性抗生素,其抗菌效果最大化需要尽可能延长血药浓度超过最低抑菌浓度的时间,即T>MIC。该时间越长,临床效果可能越好。
与间断输注相比,持续输注抗生素能使患者血药浓度在24小时内维持相对稳定,波动极小。其理论基础在于,若稳态血药浓度超过MIC,则能保证全天任何时间点的血药浓度均高于MIC,即T>MIC达到100%,从而更好地发挥疗效。
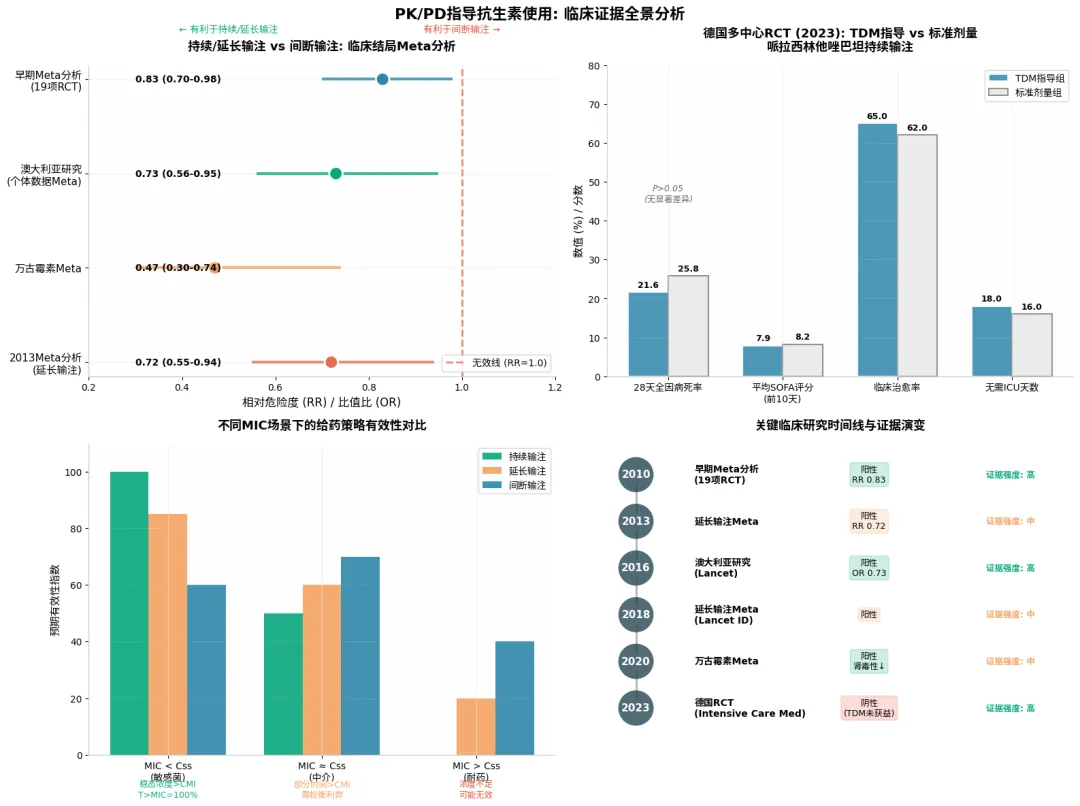
约10年前的Meta分析证实了这一点。一项对19项临床试验的荟萃分析显示,与间断输注相比,持续输注抗生素可使患者病死率的相对危险度降至0.83,临床治疗失败率的相对危险度降至0.6,均具有统计学显著性。换言之,持续输注可降低17%的病死率和近40%的临床治疗失败风险。进一步分析发现,阳性结果更多出现在持续输注哌拉西林他唑巴坦或美罗培南的研究中;而持续输注其他头孢菌素或万古霉素对预后的改善效果不明显。该研究提示,对于危重病人,持续输注特定抗生素能显著降低临床治疗失败率并改善病死率。
两年后发表在《柳叶刀》上的澳大利亚研究综合了三项随机对照试验,对总计超过630名患者进行个体数据Meta分析。结果显示,与间断输注相比,持续泵入β-内酰胺类抗生素可改善患者30天住院病死率,比值比为0.73。同时,28天内无需住ICU的时间及临床治愈率也有改善趋势。生存曲线显示,持续泵入组患者存活率显著改善。该研究表明,对于严重脓毒症患者,持续泵入β-内酰胺类药物可改善住院病死率。
后续的Meta分析也得到类似结果。对于脓毒症或死亡风险更高的患者,持续输注可能明显改善临床治愈率并降低病死率。2020年发表的Meta分析同样发现,持续输注组有更多机会达到PK目标。对万古霉素的研究表明,与间断输注相比,持续输注能显著降低急性肾损伤或肾毒性的发生风险,比值比仅为0.47。
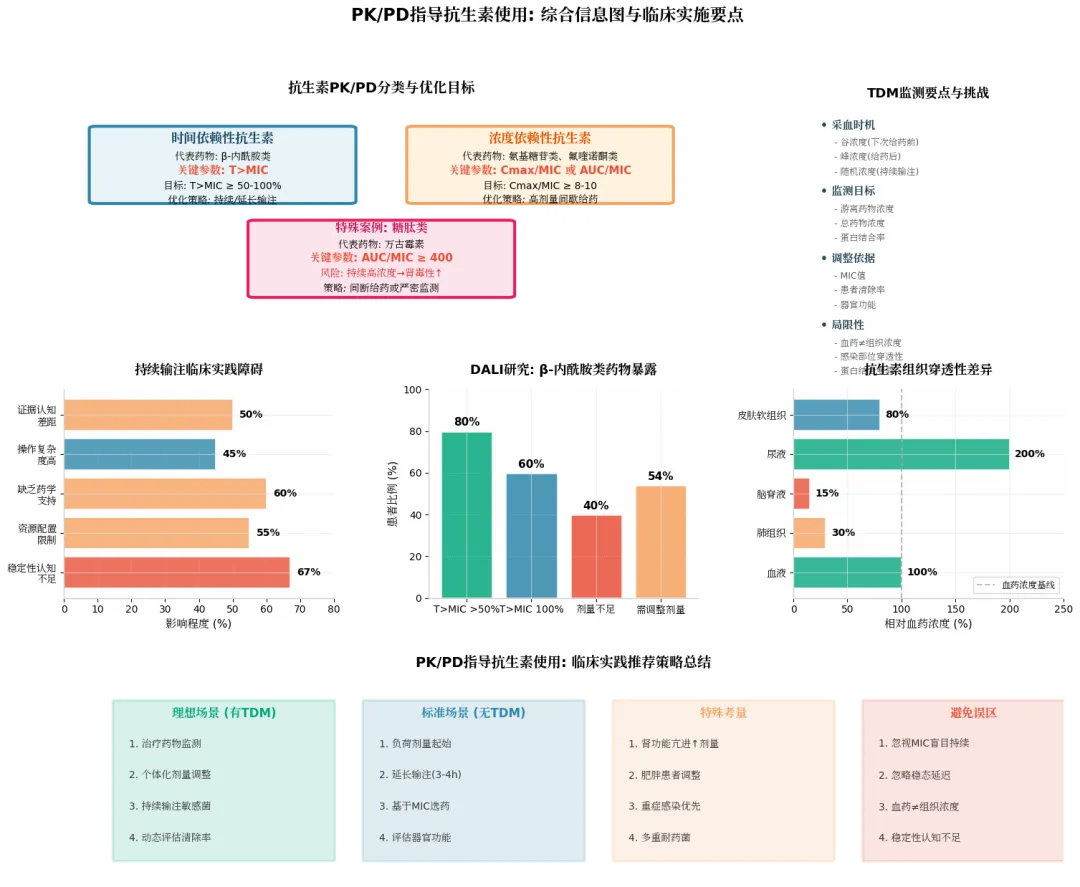
那么,临床实际应用情况如何?2014年发表的DALI研究是一项多国多中心研究,旨在通过血药浓度监测评估β-内酰胺类抗生素使用的合理性。研究监测了两个时间点的血药浓度:一是给药间隔中点,若该点浓度超过MIC,则T>MIC至少为50%;二是谷浓度,若超过MIC,则T>MIC为100%。结果显示,近80%的患者能达到T>MIC超过50%,且该指标与临床治愈率显著相关;60%以上的患者能达到T>MIC为100%,该指标也与临床治愈率密切相关。这表明,对于重症感染患者,抗生素剂量不足会导致临床结局不佳,因此需要个体化用药。
然而,关于抗生素持续输注的稳定性,问卷调查显示大多数临床医生了解不足。除万古霉素外,对其他抗生素稳定性回答正确的比例不超过三分之一。在临床实践中,除使用万古霉素治疗MRSA菌血症外,间断输注仍是主要给药方式。与ICU相比,感染科病房更倾向于不使用持续泵入抗生素,这可能与资源配置和缺乏合理用药团队有关。
接下来讨论持续输注抗生素的利弊。持续输注能使血药浓度在24-36小时内保持稳定,更容易达到T>MIC为100%的PK目标。体外研究表明,与间断输注相比,持续输注对MIC为1或4的敏感菌株杀菌效果更为显著,细菌负荷下降更明显。若仅考虑药物效应,持续输注具有一定优势。
但此方法也存在争议。以万古霉素为例,其PK/PD目标是AUC/MIC比值≥400。若通过持续输注达到此目标,需维持血药浓度在20 mg/L以上,而这可能显著增加肾毒性风险。此外,持续输注β-内酰胺类药物并非在所有情况下都更优。当治疗MIC较低的敏感菌感染时,持续输注可保证T>MIC为100%;而间断输注可能低于100%。然而,若治疗细菌的MIC高于稳态血药浓度,则持续输注期间血药浓度始终低于MIC,T>MIC为零;反而不如间断输注,因为后者产生的峰浓度可能在一段时间内超过MIC。因此,持续输注虽能维持血药浓度稳定,但对敏感菌感染能达到理想目标,对于剂量不足或MIC较高的情况则可能适得其反。
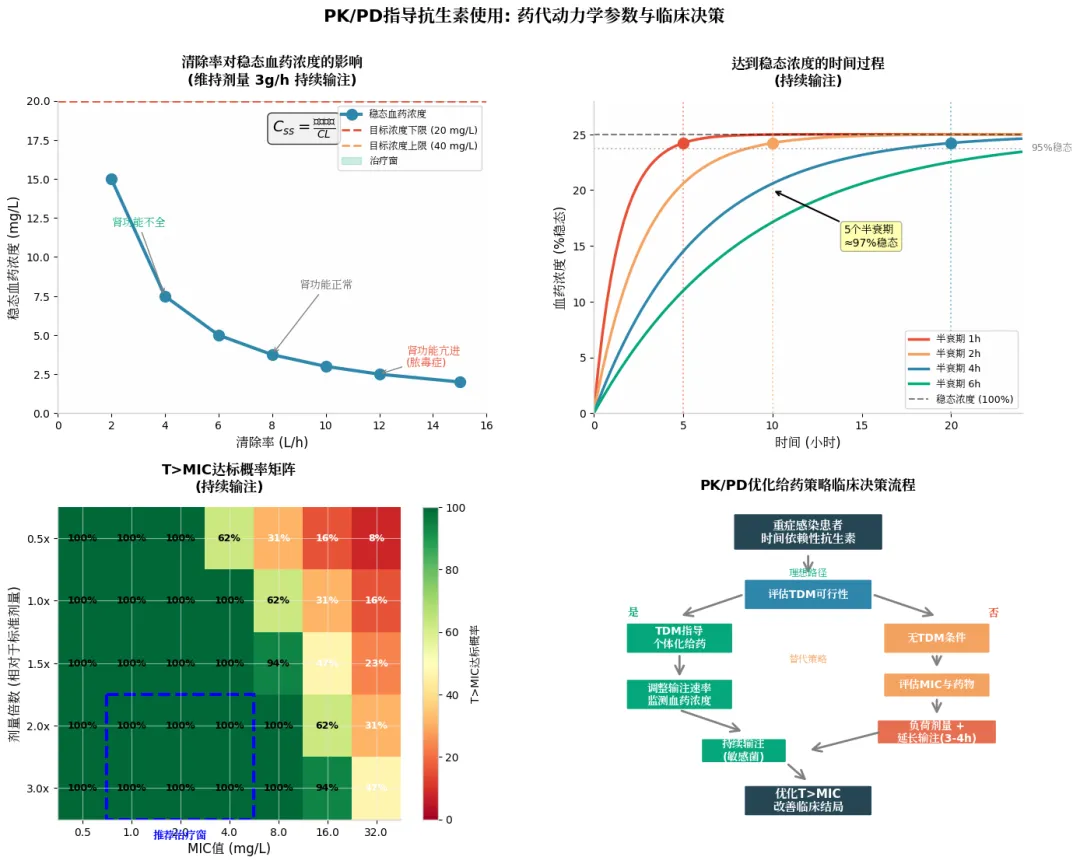
为避免血药浓度不足,一方面应选择敏感或MIC不高的菌株,另一方面需维持足够的稳态血药浓度。稳态血药浓度主要取决于维持剂量。示意图显示,随着维持剂量从0.35 g增至0.75 g,稳态血药浓度逐渐升高。从药代动力学角度,稳态血药浓度与目标稳态浓度、药物清除率及给药间隔相关。对于持续24小时静脉泵入,则与目标浓度和清除率相关。因此,为达到足够高的稳态血药浓度,需考虑清除率和维持剂量,而维持剂量与清除率密切相关。
示意图表明,在维持剂量不变时,清除率越低,血药浓度越高;清除率越高,血药浓度越低。类似地,在清除率不变时,增加维持剂量可提高血药浓度。因此,对于持续泵入,确定合理的维持剂量至关重要,而这显然与抗生素清除率紧密相关。
清除率并非一成不变。一项研究显示,在治疗过程中,β-内酰胺类抗生素的清除率增加了20%,而氨基糖苷类的清除率下降了6%,两者差异显著。这意味着初始确定的维持剂量可能随清除率变化而需要调整。事实上,危重病人β-内酰胺类抗生素的药代动力学个体间差异很大。因此,应通过治疗药物监测来指导个体化治疗。
那么,通过治疗药物监测指导抗生素治疗是否能达到理想效果?今年发表在《重症监护医学》上的一项德国多中心随机对照试验入选了249名感染性休克患者,均使用哌拉西林他唑巴坦抗感染。实验组每日监测血药浓度并调整剂量,以维持游离哌拉西林浓度≥4倍MIC;对照组采用固定剂量。主要结局是前10天平均SOFA评分。病原微生物主要为大肠杆菌、克雷伯菌属等,80%分离株MIC≤8,6%为8或16,14%≥16。两组每日药物用量无差异,但实验组有54%的住院日需要调整剂量,增减各占一半。血药浓度监测的确提高了目标范围内的比例,但临床结局方面:两组存活率无差异;主要结局平均SOFA评分(7.9分 vs 8.2分)无差异;28天全因病死率(21.6% vs 25.8%)无差异;SOFA评分变化、ICU/总住院日、临床/微生物学疗效、无需器官支持时间等均无差异。该研究为阴性结果,表明对于重症患者,基于血药浓度监测调整哌拉西林他唑巴坦持续泵入剂量,并未改善器官功能状态或其他临床结局。
作者探讨了可能原因:一是危重患者β-内酰胺类药物血药浓度个体差异大,超过半数患者需调整剂量;二是在监测下,仅约三分之一患者能达到PK/PD目标范围;三是80%分离株MIC≤8,较为敏感,可能掩盖了不同给药方式的差异。其他潜在原因包括:PK/PD模型是否正确;血药浓度是否能真实反映感染部位浓度。
首先,许多PK/PD模型基于既往药代动力学认识。例如万古霉素,即使在相同谷浓度下,达标概率差异也很大。因此,根据单一谷浓度推断达标概率可能不符合临床实际。正因如此,相关指南已修订,不再推荐仅凭谷浓度确定剂量,而是通过两个时间点的血药浓度建立模型来评估是否达标。这意味着既往对药代动力学的认识及所建模型可能不准确,据此推断的用药方式可能不合理。
其次,临床上易监测的是血药浓度,但更重要的是感染部位的药物浓度。有证据表明两者相关性可能很差。例如肺炎,许多抗生素肺部穿透性差,血药浓度与肺组织浓度相关性不佳。虽有研究测量上皮细胞衬液浓度,但尚无证据证实其PK特征与临床疗效相关,因为上皮细胞衬液浓度与肺组织浓度的相关性也不好。这意味着血药浓度未必能真实反映感染部位浓度。
若无血药浓度监测,持续输注是否有其他解决方案?可能的方法是延长输注时间而非24小时持续泵入。示意图显示,与间断输注相比,延长输注虽不如持续泵入稳定,但能比间断输注更好地延长T>MIC时间。
临床试验证据支持这一点。2018年《柳叶刀》子刊的Meta分析表明,与间断输注相比,延长输注时间能更好地改善患者结局,对不同抗生素几乎都有类似趋势。2013年的Meta分析也将用药方式分为持续泵入和延长输注,发现持续泵入两组临床疗效无显著差异,而延长输注可使病死率相对危险度降至0.72,即下降28%。
另一项10年前发表在《重症监护医学》上的研究,对比了治疗呼吸机相关性肺炎时,多利培南1g输注4小时、每8小时一次、疗程7天,与亚胺培南1g输注1小时、每8小时一次、疗程10天的方案。结果显示,两组临床治愈率、CPIS评分、生存率均无差异。考虑原因之一可能是延长输注时间(从1小时到4小时)有助于更好地达到PK/PD目标。示意图表明,与间断输注相比,持续输注虽能达更好稳态,但在治疗初期难以迅速达到足够高的治疗浓度;而延长输注作为一种折中方案,能比持续输注更早达到目标血药浓度。
总结而言,对于重症感染的抗生素治疗,PK/PD原则仍然非常重要。持续输注β-内酰胺类药物在理论上优于间断输注,但迄今缺乏强有力的临床证据支持。核心问题在于如何确定药物维持剂量、如何判定清除率,并据此设定合理剂量以达到PK/PD目标。相比之下,在无血药浓度监测的情况下,采用负荷剂量后延长输注时间,可能是一个可行的替代措施。
PK/PD指导抗生素使用
本课程核心主题为药代动力学/药效学(PK/PD)原则在指导重症感染患者抗生素治疗中的应用。课程系统阐述了时间依赖性抗生素(以β-内酰胺类为代表)持续输注与间断输注的理论基础、临床证据及实践争议。教学目标在于使学习者深入理解T>MIC等关键PK/PD靶标,辨析持续输注的潜在优势与局限性,并掌握在缺乏治疗药物监测条件下的优化给药策略。课程覆盖了从Meta分析证据解读、药代动力学模型构建,到临床随机试验结果批判性评估的全链条知识,对于指导危重患者个体化抗感染治疗、优化临床结局具有重要价值。
 详细章节摘要
详细章节摘要
章节1:持续输注的理论基础与早期证据
- 核心要点:本章阐述了时间依赖性抗生素的PK/PD核心参数T>MIC,并从理论推导和早期荟萃分析两个层面,论证持续输注相比间断输注在优化该参数上的潜在优势。
- 关键概念与定义
- T>MIC:指给药间隔内,血药浓度高于病原菌最低抑菌浓度(MIC)的时间。对于时间依赖性抗生素,延长T>MIC是优化疗效的关键。
- 持续输注:将24小时总剂量通过静脉泵持续、匀速地输入体内,以维持稳定的血药浓度。
- 间断输注:将每日总剂量分次(如每8小时一次)在较短时间内(如1小时)输注完毕。
- 内容详述首先明确了抗生素按PK/PD特性分为浓度依赖性和时间依赖性两类。对于后者,抗菌活性主要取决于血药浓度超过MIC的时间。通过药时曲线对比图直观展示:间断输注的血药浓度存在明显的峰谷波动,可能导致T>MIC不足;而持续输注能维持血药浓度在24小时内相对稳定。理论上,若稳态浓度高于MIC,则可实现T>MIC=100%,最大化抗菌效果。随后,引用了约10年前的一项Meta分析作为早期证据。该分析汇总了19项临床试验,结果显示,与间断输注相比,持续输注能显著降低危重患者的病死率(RR=0.83)和临床治疗失败率(RR=0.60)。亚组分析提示,这种获益在哌拉西林他唑巴坦和美罗培南中更为明显,而在其他头孢菌素或万古霉素中效果不彰。这初步支持了持续输注在特定人群和药物中的价值。
章节2:后续临床研究与现实实践差距
- 核心要点:本章介绍了更大规模的个体数据Meta分析提供的阳性证据,同时通过调查数据揭示了持续输注在临床实践中的采纳率低与认知不足的现实困境。
- 关键概念与定义
- 个体数据Meta分析:一种将多项研究的原始个体患者数据合并后进行再分析的统计方法,比传统基于汇总数据的Meta分析更为精确。
- DALI研究:一项旨在描述危重患者β-内酰胺类药物暴露情况与临床结局关联的多中心观察性研究。
- 内容详述讲师首先介绍了发表在《柳叶刀》上的澳大利亚研究,该研究将三项RCT的个体数据合并分析(n>630)。结果显示,持续泵入β-内酰胺类可显著降低30天住院病死率(OR=0.73),并显示出改善临床治愈率和缩短ICU住院时间的趋势。生存曲线直观展示了持续泵入组的生存优势。然而,理论优势并未完全转化为临床实践。讲师引用了DALI研究的数据,该研究通过监测血药浓度发现,达到理想的PK目标(如T>MIC>50%或100%)与更好的临床治愈率相关,这反证了剂量不足的普遍性及个体化给药的必需性。但随后的问卷调查显示,临床医生对各类抗生素在溶液中的稳定性认知严重不足(除万古霉素外,正确率<33%)。在实际应用中,除万古霉素治疗MRSA菌血症外,间断输注仍是绝对主流。这种理论与实践的巨大差距,可能与医疗资源配置、药学支持团队缺失等因素有关。
章节3:持续输注的深度辨析与药代动力学挑战
- 核心要点:本章辩证分析了持续输注的利弊,深入探讨了其核心药代动力学挑战——如何确定并维持有效的稳态血药浓度,并指出治疗药物监测是实现个体化给药的理想手段。
- 关键概念与定义
- 稳态血药浓度:在固定方案重复给药或持续输注后,药物在体内的吸收与消除达到平衡时的血药浓度。
- 清除率:单位时间内机体清除药物的血浆体积,是决定维持剂量的关键参数。
- 治疗药物监测:通过测定患者体液中的药物浓度,以调整给药方案,实现个体化治疗。
- 内容详述首先重申了持续输注在维持稳定血药浓度、确保T>MIC方面的理论优势,并引用体外实验数据证明其对敏感菌的杀菌效果优于间断输注。然而,讲师重点剖析了其局限性与风险。第一,并非万能:当病原菌MIC高于所能维持的稳态血药浓度时,持续输注的T>MIC可能为零,反而不如间断输注可能产生的短暂峰浓度有效。第二,毒性风险:以万古霉素为例,为达到AUC/MIC≥400的目标而持续维持高血药浓度(如>20 mg/L),会显著增加肾毒性风险。随后,课程进入核心难点:如何确定合适的维持剂量以达成有效且安全的稳态浓度?讲师通过公式和示意图阐明,稳态浓度取决于维持剂量和药物清除率。而危重患者的清除率个体差异极大,且可能在治疗过程中动态变化(如β-内酰胺类清除率可增加20%)。因此,初始的标准剂量对许多患者并不适用。逻辑结论是,必须依靠TDM来实时指导剂量调整,实现真正的个体化给药。
章节4:TDM指导治疗的临床证据与根本性质疑
- 核心要点:本章通过一项最新的阴性RCT,揭示了即使采用TDM指导剂量调整,也未能改善临床结局,进而深入反思了当前PK/PD模型和血药浓度监测本身的局限性。
- 关键概念与定义
- 阴性结果:在临床试验中,实验组与对照组在主要结局指标上未显示出统计学显著差异的结果。
- PK/PD模型:用于描述和预测药物在体内的浓度变化(PK)与其效应(PD)之间定量关系的数学模型。
- 内容详述详细解读了2023年发表在《重症监护医学》上的一项德国多中心RCT。该研究在感染性休克患者中比较了TDM指导下的个体化哌拉西林他唑巴坦持续输注与固定剂量方案。尽管TDM组有超过一半的时间需要调整剂量,并显著提高了血药浓度在目标范围内的比例,但两组在主要终点(平均SOFA评分)、28天病死率、临床治愈率等所有次要终点上均无差异。分析了可能原因:1)患者群体中敏感菌(MIC≤8)占主导(80%),可能削弱了精细化剂量调整的收益;2)即便有TDM,仅约1/3时间能精确达标。进而,提出了更根本的质疑:第一,模型是否准确? 例如万古霉素,基于传统单点谷浓度推算AUC/MIC的模型已被证明不可靠,新版指南已推荐基于两点的模型估算。第二,监测位点是否相关? 血药浓度能否代表感染部位(如肺组织)的药物浓度?现有证据表明,对于肺部感染,血药浓度与肺组织浓度相关性差,甚至上皮细胞衬液浓度也不能很好代表组织浓度。这动摇了以血药浓度为唯一调控靶标的基础。
章节5:替代策略:延长输注与课程总结
- 核心要点:本章在反思持续输注与TDM挑战的基础上,提出了“延长输注”这一折中且更具实操性的优化策略,并总结了课程核心观点。
- 关键概念与定义
- 延长输注:将每次给药的输注时间显著延长(如从1小时延长至3-4小时),但并非24小时持续输注。通常需先给予一个负荷剂量。
- 内容详述面对TDM的局限性和实施的复杂性,提出了一个务实的替代方案:延长输注时间。药时曲线示意图显示,延长输注(如4小时)是介于间断输注(1小时)和持续输注(24小时)之间的策略。它既能比间断输注更有效地延长T>MIC,又能比持续输注更快地达到治疗浓度(因后者需等待5个半衰期才能达稳态)。多项临床证据支持该策略。2018年《柳叶刀》子刊的Meta分析表明延长输注能改善患者结局。2013年的Meta分析更发现,在改善病死率方面,延长输注显示效益,而持续泵入则未显示优势。另一项针对呼吸机相关性肺炎的RCT也证实,7天延长输注多利培南与10天标准输注亚胺培南疗效相当。最后总结:PK/PD原则对重症感染治疗至关重要。持续输注β-内酰胺类药物虽有理论优势,但面临确定个体化维持剂量的巨大挑战,且当前高级别临床证据不足。在缺乏TDM的条件下,采用负荷剂量后延长输注时间,是一个被证据支持、易于实施的优化选择。
关键数据与参数汇总
表1: 持续输注 vs. 间断输注的关键临床研究数据汇总
表2: 药代动力学关键参数与概念
| | |
|---|
| | 抑制病原菌可见生长的最低药物浓度,是PK/PD靶标计算的基石。 |
| | 时间依赖性抗生素的关键PK/PD指标,与疗效正相关。目标通常为100%给药间隔。 |
| | 浓度依赖性抗生素(如万古霉素、氨基糖苷类)的关键PK/PD指标。万古霉素目标通常≥400。 |
| | 决定药物从体内清除速率的参数,个体差异大,直接影响维持剂量的设定。 |
| | 持续输注或多次给药达平衡后的稳定血药浓度。Css = 输注速率 / CL。 |
核心流程与概念图解
图1: 重症感染患者时间依赖性抗生素给药策略决策流程
本图概括了课程中关于如何为重症感染患者选择优化给药策略的核心决策逻辑。它从PK/PD目标(T>MIC)出发,对比了持续输注、延长输注和间断输注的适用场景与前提条件,并纳入了治疗药物监测(TDM)的考量,最终导向临床决策。