抗体偶联药物(ADC)学习笔记(上):基础概念与五大核心决定因素
- 2026-06-02 16:35:35

小
寒
学习笔记

本文为个人学习记录,不保证信息准确完整,不构成任何投资建议或行动指南。据此操作,盈亏自负,本人不承担任何责任。
之前在《从亏损到盈利:荣昌生物2025年商业化与全球化双突破》就发现荣昌生物好多ADC在财报中消失,查了下资料再学习一下ADC,希望对ADC技术原理有更多了解。
一、ADC基础概念与平台技术演进
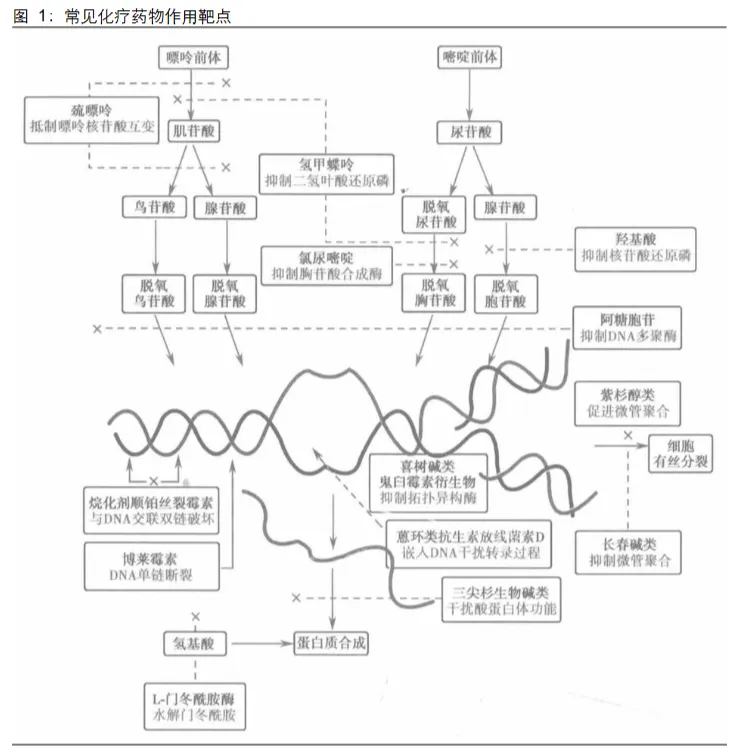
肿瘤治疗史上,化疗作为系统性治疗手段,常用的化疗药物有几十种,根据抗肿瘤作用的生化机制不同,这些常用的化疗药物分别属于影响核酸生物合成的药物、影响DNA结构与功能的药物、干扰转录过程和阻止RNA合成的药物,以及抑制蛋白质合成与功能的药物。但化疗最明显缺点就是即不仅作用于肿瘤细胞,也会作用于正常细胞,导致的毒副作用,所以ADC药物应运而生。就像精确制导出世,既能提高效率也减少不必要伤亡。
想象一下有一种“生物导弹”,它拥有导航系统(抗体)来识别并锁定目标(肿瘤细胞),一个可靠的连接体(连接子)来确保“弹头”在运输途中安全,以及一枚威力强大的弹头(细胞毒素)在抵达目标后实施致命打击。这,就是抗体偶联药物(Antibody-Drug Conjugate,简称ADC) 的核心理念,旨在实现“增效减毒”。其实吧,ADC称为生物导弹还不是很恰当,在目前技术条件下,ADC给药后仅有约0.1%-1%的总给药剂量最终递送至实体瘤组织,绝大多数药物被正常组织清除代谢,因此“生物导弹”的精准递送效率仍有极大提升空间
(一)ADC是什么?
ADC本质上是一种新型生物药或靶向疗法。其定义就是通过一个名为“连接子(Linker)”的化学桥梁,将具有高度靶向性的单克隆抗体(Antibody) 与高效杀伤肿瘤细胞的小分子细胞毒性药物(Payload,也称为毒素) 连接在一起。ADC 抗体部分识别并结合抗原后,ADC 就会被细胞内吞/内化形成早期的内体,随后成熟为晚期内体,最终与溶酶体融合,细胞毒性有效载荷通过酶体介导的化学或酶促释放,最终达成细胞凋亡或死亡。
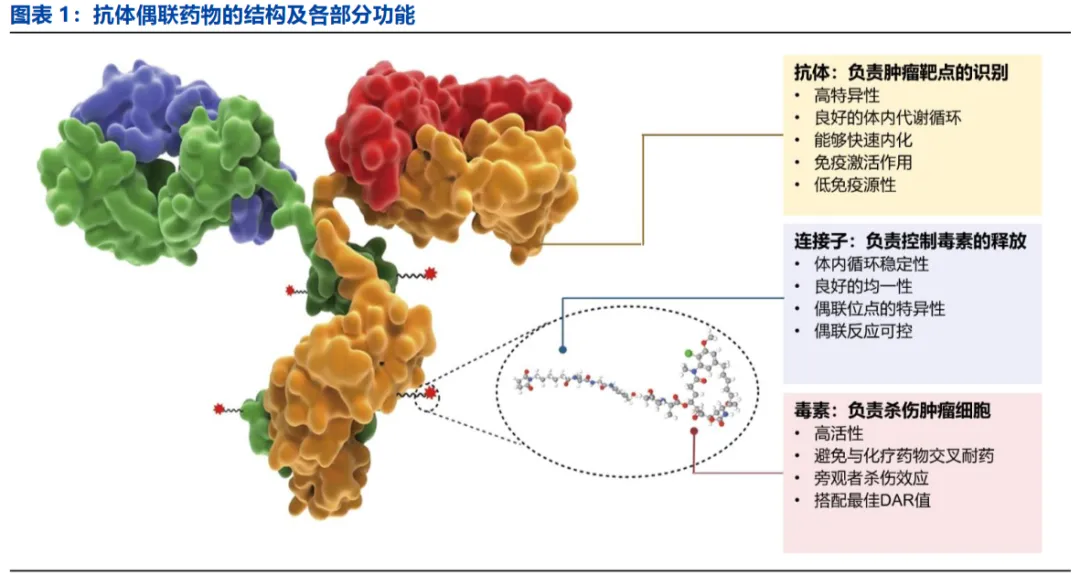
这三个核心部件共同决定了ADC的成败:
①抗体:制导系统。通常采用人源化或全人源的IgG1单克隆抗体。它的核心任务是高特异性地识别并结合肿瘤细胞表面过度表达的靶点抗原(如HER2、CD30等),并将整个ADC分子引导至肿瘤细胞。一个优秀的抗体还需具备强效的内化能力,能促使药物-抗原复合物被肿瘤细胞“吞”进去,以及低免疫原性,避免被人体自身免疫系统攻击。
②连接子:安全开关。这是控制毒素释放的关键。它必须在血液循环中保持绝对稳定,防止毒素“提前爆炸”伤及无辜(即脱靶毒性)。同时,它又要在进入肿瘤细胞后,能在特定环境(如酸性、特定酶、高浓度还原物质)下被精准切割,及时释放出毒素。目前主流的可裂解连接子(如酶裂解的“缬氨酸-瓜氨酸”二肽或GGFG四肽)因其能实现肿瘤内特异性释放并可能产生“旁杀效应”(杀伤邻近不表达靶抗原的肿瘤细胞)而备受青睐。
③细胞毒性药物:高效弹药。这是ADC最终杀伤肿瘤的效应分子。与传统化疗药不同,ADC所用毒素的效力通常要强数百至上千倍(IC₅₀在10⁻¹⁰至10⁻¹² M级别),属于“剧毒”物质,因此必须依赖抗体的精准导航才能安全使用。主流毒素分为两大类:一是破坏细胞有丝分裂的微管蛋白抑制剂(如MMAE、DM1);二是造成DNA不可逆损伤的DNA损伤剂,其中又分为DNA双链断裂剂(如卡奇霉素)、DNA烷基化剂(如PBDs)、拓扑异构酶I抑制剂(如DXd、SN-38)等子类。
(二)什么是ADC平台?
一个完整的ADC技术平台,就像一家高度自动化的“生物导弹”设计制造工厂,它整合了从设计、生产到测试的全链条能力:
① 核心元件库:拥有丰富的“零件”储备,包括针对不同靶点的抗体库、各种类型的连接子库(可裂解/不可裂解),以及作用机制各异的毒素库(微管抑制剂、DNA损伤剂、拓扑异构酶抑制剂等)。
②核心偶联工艺:掌握将“弹药”安装到“导弹”上的关键技术。从早期的随机偶联(如在抗体表面随机连接,导致产物不均一),到更先进的定点偶联技术(如工程化半胱氨酸、酶促偶联),能够精确控制每个抗体上连接的毒素数量(即药物抗体比,DAR),从而生产出均一、稳定、药效可预测的ADC药物。
③筛选与优化体系:具备高效的“试射场”,能够快速测试不同“抗体-连接子-毒素”组合的活性、稳定性和安全性,从而智能地挑选出最优方案。
④可扩展性:先进的平台其“载体-连接子-载荷”范式可进一步拓展,将载体从抗体延伸到多肽、小分子,或将载荷从毒素扩展到 PROTAC、免疫调节剂等,从而衍生出更广阔的偶联药物(XDC) 领域,应用于肿瘤以外的疾病。
(三)ADC技术的“模块化”演进
如同战机会更新换代,ADC技术也在迭代升级。每一代的进步,都围绕着抗体、连接子、毒素和偶联方式这些核心模块进行优化。
第一代ADC:概念验证,但问题重重
①技术特征:采用鼠源或嵌合抗体(免疫原性强);连接子稳定性差(如酸裂解的腙键),易在血液中提前释放毒素;采用高毒性但适配性差的毒素(如卡奇霉素);采用随机偶联,导致产物是DAR值(0-8)不均一的混合物。
②代表药物:Mylotarg(吉妥珠单抗奥唑米星,靶向CD33)。它于2000年率先获批,证明了ADC概念的可行性,但因严重的肝毒性等问题曾撤市,后经优化方案才重返市场。其历程集中暴露了第一代ADC在疗效、毒性和药代动力学方面的短板。
第二代ADC:临床成功,确立范式
① 技术特征:抗体升级为人源化/优化的嵌合抗体,显著降低免疫原性;连接子稳定性提高;引入活性极高的微管蛋白抑制剂作为毒素(如MMAE、DM1),杀伤力大幅增强;偶联方式主要为半胱氨酸随机偶联,均一性有所改善,但DAR分布仍较宽(通常在4-8)。
②代表药物:Adcetris(维布妥昔单抗,靶向CD30)和 Kadcyla(T-DM1,靶向HER2)。Kadcyla(2013年获批)是首个在实体瘤(乳腺癌)取得巨大成功的ADC,其商业成功让整个行业重拾信心。第二代ADC证明了该疗法的巨大潜力,但产品均一性不足和脱靶毒性(如周围神经病变、眼毒性)等问题,提示治疗窗口仍有优化空间。
第三代ADC:精准升级,突破瓶颈
①技术特征:抗体迈向全人源化;连接子普遍采用高稳定性、可在肿瘤细胞内特异性酶切的可裂解连接子(如Val-Cit二肽、GGFG四肽);毒素库极大丰富,拓扑异构酶I抑制剂(如DXd) 成为新主流,它毒性相对温和,允许更高的DAR值,并能产生强大的“旁杀效应”;定点偶联技术开始应用,实现DAR值的均一可控。由此形成了两种优化策略:“低DAR高毒”(高活性微管抑制剂类毒素,DAR~4)和“高DAR可控毒”(活性强、全身毒性更可控的拓扑异构酶I抑制剂如DXd,DAR~8)。
②代表药物:Enhertu(德曲妥珠单抗,T-DXd,靶向HER2)。它采用人源化曲妥珠单抗、可裂解GGFG连接子、DXd毒素,DAR值精确为8。Enhertu不仅在HER2高表达乳腺癌中表现卓越,更凭借其旁观者效应,成功将适应症拓展至HER2低表达人群,改写了治疗格局,是第三代ADC技术集大成的典范。
从第一代到第三代,ADC技术的演进是一部围绕“导弹”各系统不断精密化的历史。抗体更“人源”、连接子更“智能”、毒素更“强悍”、偶联更“精准”,每一次模块的升级,都旨在扩大治疗窗口,让这把“生物导弹”打得更准、炸得更有效,同时最大程度减少附带损伤。
二、决定ADC有效性与安全性的五大关键因素
ADC研发的核心目标在于扩大“治疗窗口”——即在对肿瘤细胞实现最大杀伤的同时,将对正常组织的损伤降至最低。这一目标的实现,高度依赖于对构成ADC的五个核心模块的理性设计与精妙平衡:靶点、抗体、连接子、毒素与偶联方式。这五大因素相互关联,共同决定了ADC最终能否安全、有效地完成其精准递送“弹头”的使命。
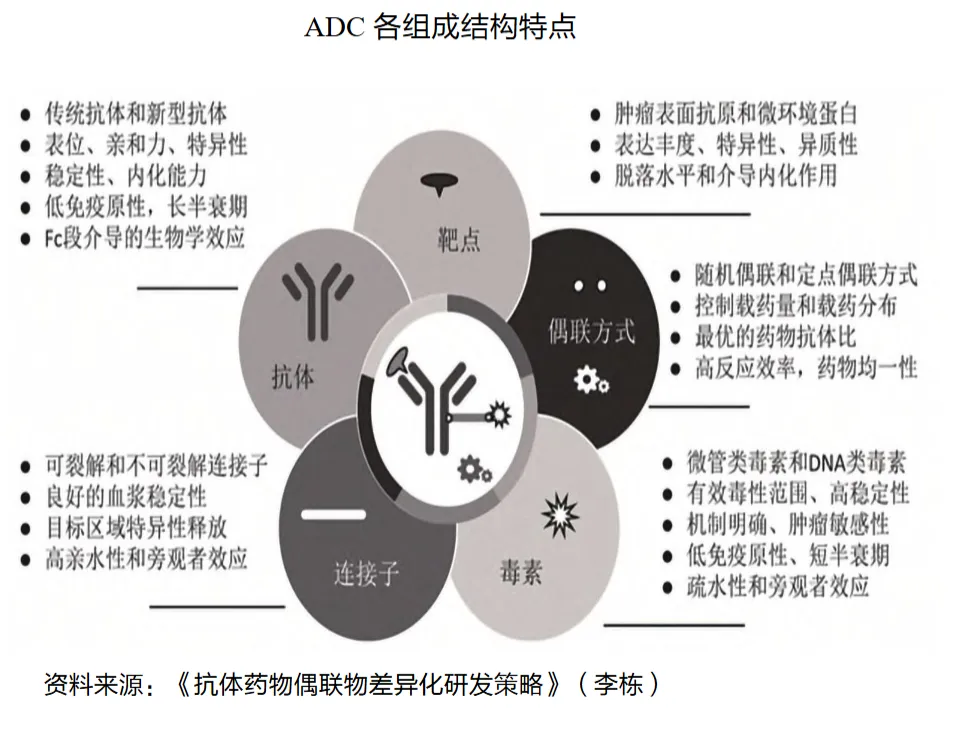
(一)靶点
靶点抗原是ADC识别肿瘤细胞的“导航地址”,其选择是ADC实现肿瘤特异性的根本。
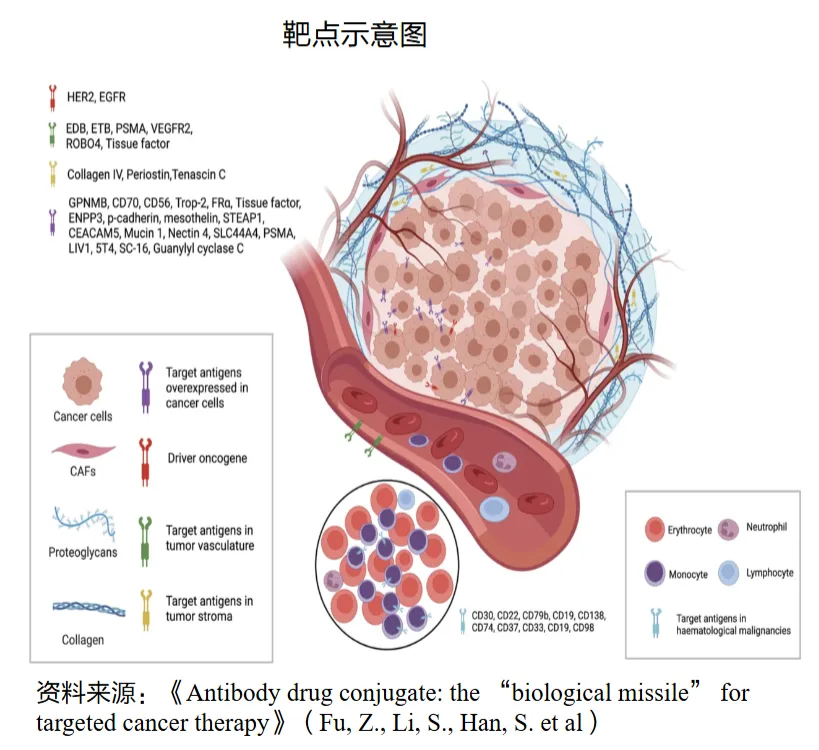
VEGFR2、EDB、ETB、ROBO4 | |||||
①高特异性与差异化表达:理想的靶抗原应在肿瘤细胞表面过表达,而在健康组织中表达极低或不表达。②靶点蛋白像一根“天线”一样,有一段特定的结构伸出在肿瘤细胞的细胞膜外面。③抗原应避免大量分泌至血液循环,以免在抵达肿瘤前就被耗竭。④高效的内化与溶酶体导向:抗体与靶抗原结合后,必须能有效介导“受体介导的内吞作用”,将整个ADC复合物“拉”进细胞内部。内化后,复合物还需被有效分选并转运至溶酶体进行降解,这是释放毒素的关键步骤。内化效率低或复合物被回收至细胞表面是导致耐药的重要原因。
知识拓展:现代ADC的靶点已不限于肿瘤细胞本身,正扩展到肿瘤微环境,如肿瘤新生血管、基质或浸润免疫细胞上的抗原,其基因组更稳定,可能降低耐药风险。
(二)抗体
抗体作为“导航系统”,负责靶点识别,同时也作为毒素的载体 ,其设计直接影响到靶向效率、体内行为和安全性。理想抗体需具备高特异性、高亲和力、高效内吞、低免疫原性、长半衰期,以减少脱靶损伤与提前消耗。
①高亲和力与高特异性:抗体需与靶抗原强效、专一地结合,这是导航精准度的热力学基础。
②低免疫原性:通过采用人源化或全人源抗体(目前主流),显著降低免疫原性,减少因人体产生抗药抗体而导致的疗效下降或过敏反应。
③较长的体内半衰期:绝大多数在研ADC均采用IgG骨架,因其循环半衰期长。IgG1和IgG3对比IgG2和IgG4具有更强的ADCC和CDC效应,可以增强ADC对肿瘤细胞的杀伤作用。而IgG3分子在循环中的半衰期较短,难以满足临床使用中对于给药周期的要求,所以IgG1是目前最常用的亚型。
IgG四种亚型特征对比
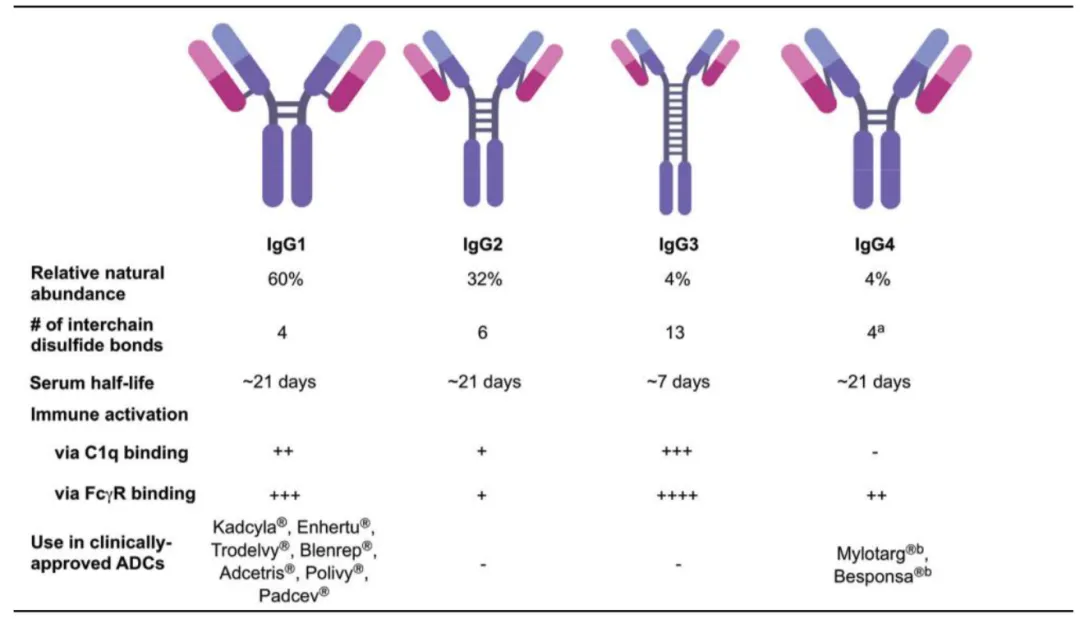
④Fc效应的理性调控:根据设计需要,可对Fc段进行工程化改造。既可增强ADCC/CDC效应以提升疗效,也可进行“沉默”突变以降低免疫效应相关毒性或优化药代动力学。
知识补充:抗体是一种 Y 形免疫蛋白,Fab手臂部分负责抓靶点,Fc尾巴部分负责激活免疫。按 “人源程度” 分四代,决定免疫原性:①鼠源抗体,全是老鼠的,排斥强,现在基本淘汰。②嵌合抗体,鼠源 Fab + 人源 Fc,代表:Adcetris(本妥昔单抗)。③人源化抗体,90%+ 人源,只保留鼠源识别区,代表:RC48、Kadcyla。④全人源抗体,100% 人源,免疫原性最低,代表:Padcev、Enhertu、大部分第三代 ADC。
(三)连接子
连接子是连接抗体与毒素的“安全锁”,其设计需要在全身循环的稳定性与肿瘤内的特异性释放之间取得精妙平衡。
核心矛盾:循环稳定 vs. 肿瘤内释放:理想连接子必须在血液循环中绝对稳定,防止毒素“早释”造成全身毒性;但进入肿瘤细胞后,又能被特定条件触发,高效释放活性毒素。
Linker可分为可裂解和不可裂解两大类型。具体对比如下表,总体看来,与不可裂解连接子相比,可裂解连接子的循环稳定性稍逊,但具有更好的肿瘤特异性,可与不同类型的有效载荷协同使用,是目前研发的主流方向。
对比维度 | 可裂解Linker(连接子) | 不可裂解Linker(连接子) |
|---|---|---|
核心定义 | 可在体内(主要是肿瘤细胞内)被特异性物质切断,释放载荷(毒素) | 全程不被切断,需等待抗体被细胞完全降解后,才释放载荷(毒素) |
血液循环稳定性 | 高稳定,避免提前释放毒素,降低脱靶毒性 | 极高稳定,几乎不会提前释放毒素,脱靶毒性更低 |
毒素释放机制 | 进入肿瘤细胞后,被特定物质裂解(如蛋白酶、酸性环境、谷胱甘肽) | 抗体被肿瘤细胞内吞后,经溶酶体降解,Linker随抗体降解释放毒素 |
旁观者效应 | 有,释放的毒素可穿透细胞膜,杀伤周边未被ADC结合的癌细胞 | 几乎无,毒素仅在ADC结合的癌细胞内释放,杀伤范围窄 |
常见类型/代表 | 蛋白酶可裂解(vc-PAB,最常用)、酸敏裂解、谷胱甘肽敏感;代表:Padcev、RC48、Enhertu | 硫醚类等;代表:Kadcyla(T-DM1) |
适用场景 | 新一代ADC主流选择,适合肿瘤异质性强、需扩大杀伤范围的场景 | 老一代ADC常用,适合对脱靶毒性要求极高、肿瘤边界清晰的场景 |
核心优势 | 杀伤范围广、抗肿瘤活性强,适配强效毒素 | 稳定性极强、脱靶毒性低,安全性更有保障 |
潜在不足 | 若裂解过度,可能增加全身毒性 | 无旁观者效应,对异质性肿瘤杀伤效果有限 |
根据触发释放机制的不同,可裂解连接子可以分为酶裂解型、酸裂解型和还原裂解型连接子等。
| 酶裂解型连接子 | 酸裂解型连接子 | 还原裂解型连接子 | |
|---|---|---|---|
| vc-PAB(缬氨酸 - 瓜氨酸) | |||
| 最高,血液中几乎不裂解 | |||
| 最强,仅肿瘤内高效切割 | |||
| 现代 / 第三代 ADC 主流 |
β-葡萄糖醛酸酶、硫酸酯酶、磷酸酶和天冬酰胺内切酶作为裂解酶的连接子还处于研究阶段。
(四)有效载荷(毒素)
小分子毒素是直接杀伤肿瘤的“弹药”,其选择决定了 ADC 的效力和安全性特征。
理想的 ADC 小分子毒素应具备①极高细胞毒性,其 IC₅₀需达到纳摩尔甚至皮摩尔水平,以适配肿瘤细胞表面有限的抗原数量及 ADC 分子有限的载药量;②明确且适配胞内起效的抗肿瘤机制,主要通过干扰细胞微管合成或 DNA/RNA 复制发挥作用;③旁观者效应,以提升对异质性肿瘤的杀伤效果;④毒素需在血液循环中稳定、不易提前释放,且游离后可被机体快速清除、免疫原性低,避免蓄积引发全身毒性与不良反应。已上市的ADC药物的载荷毒素主要有两大类型,微管蛋白抑制剂及DNA损伤剂。
微管蛋白抑制剂,通过抑制细胞微管组装,阻断有丝分裂,使癌细胞凋亡,包括长春碱、单甲基Auristatin E(MMAE)和单甲基Auristatin F(MMAF)、Maytansinoids美登素类化合物如DM1、DM3、DM4等。微管蛋白抑制剂对于活跃分裂的肿瘤细胞非常有效,但对于静息状态的肿瘤细胞效果并不理想。
DNA损伤剂可以通过双链断裂、烷基化、嵌合、交联等方式破坏DNA结构,干扰肿瘤细胞DNA合成,从而杀伤肿瘤细胞。根据不同作用机制分为DNA双链断裂:卡奇霉素。DNA烷基化:Duocarmycin倍癌霉素。DNA嵌入:喜树碱类似物/拓扑异构酶Ⅰ抑制剂ExatecanMesylate(DX-8951f)。DNA交联:吡咯并苯二氮䓬类化合物Pyrrolobenzodiazepines,即PBD。
目前已有部分采用 RNA合成抑制剂、免疫抑制剂等新载荷的 ADC 管线进入临床开发阶段。
ADC有效载荷的作用机制和相关毒性
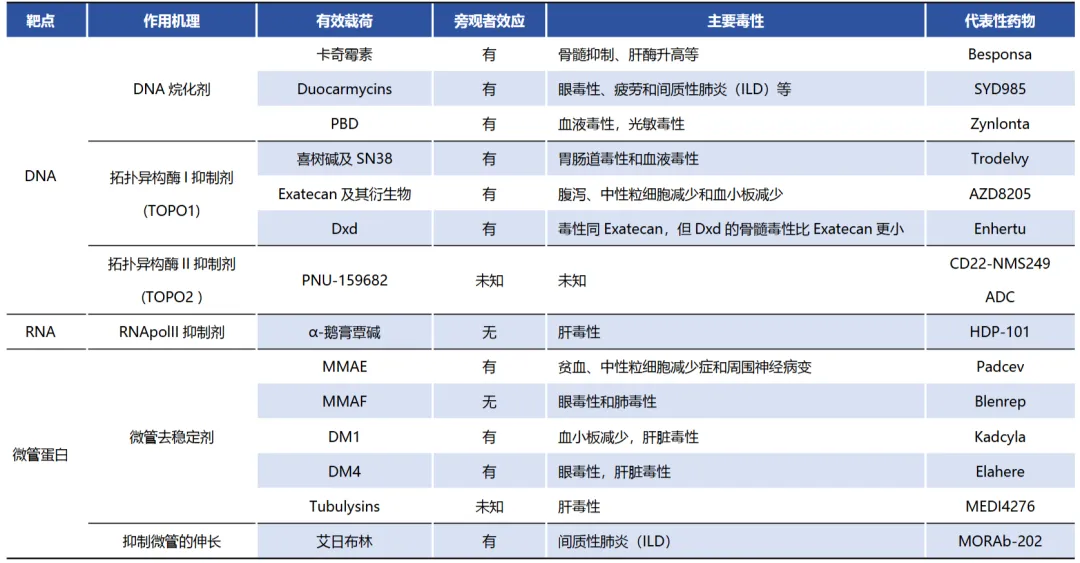
(五)偶联方式
如何将毒素稳定地连接到抗体上,决定了最终产物的均一性、稳定性和药代动力学行为。ADC药物的偶联方式包括氨基酸位点的选择、药物抗体比率(DAR)控制以及使用的化学反应。偶联方式主要有两种:
一是随机偶联:早期主要方式,产物异质性强,影响治疗效果窗口。
①赖氨酸偶联:利用抗体上大量赖氨酸的氨基反应。简单快速,但DAR分布极宽(0-8),均一性差,可能影响抗体亲和力。代表:早期ADC如Mylotarg。
②半胱氨酸偶联:通过还原抗体链间二硫键,在形成的游离巯基上偶联。目前最常用,均一性有所提升,可主要获得DAR为2、4、8的产物。但仍是混合物,且使用的马来酰亚胺连接可能发生逆反应,导致毒素提前释放。
二是定点偶联:新一代ADC的技术趋势,旨在实现定点、定量、均一的连接,大幅提升产品质量和疗效可预测性。
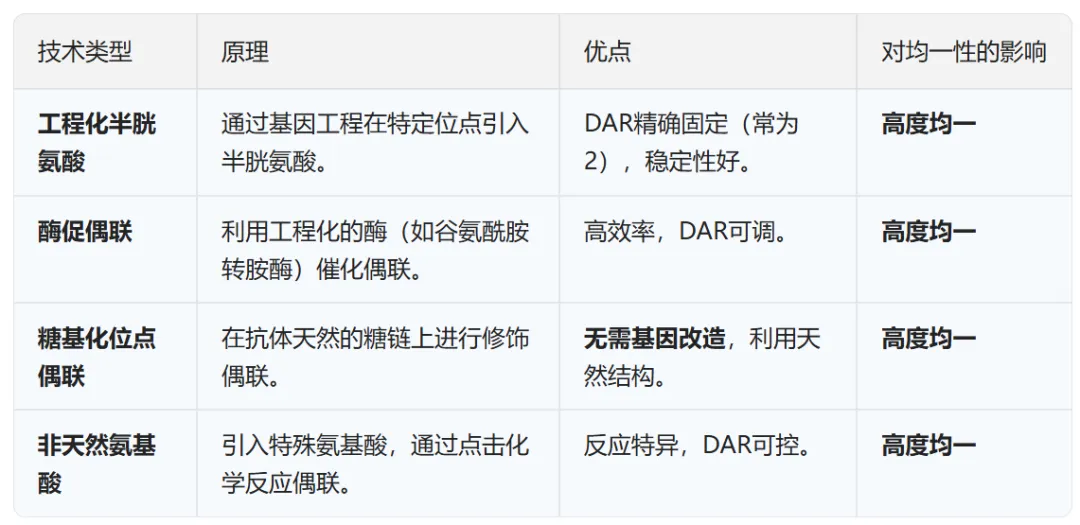
总之,一个成功的ADC,其靶点决定了打击目标是否精准;抗体优化了导航系统的性能与续航;连接子确保了弹头在途中安全锁闭、在目标处准时引爆;毒素则提供了足以摧毁目标的强大火力;而偶联方式保证了整个武器系统被稳定、均一地装配起来。对这五大因素的深刻理解与持续创新,是推动ADC药物不断突破疗效与安全性瓶颈、扩大治疗窗口的根本动力。
1
END
1
日拱一卒不期而至
公众号|小寒书巢
