学习笔记(19):多组学揭示乳腺癌淋巴结转移的关键蛋白与磷酸化机制
- 2026-05-29 21:12:07

乳腺癌是全球女性中发病率最高的恶性肿瘤之一,具有高度异质性、易复发及转移等特点,其中淋巴结转移是乳腺癌进展为远处转移的重要早期事件,也是影响患者预后的关键因素。尽管近年来在基因组和转录组层面对乳腺癌转移机制的研究不断深入,但越来越多证据表明,单纯依赖转录层面的信息难以全面反映肿瘤的功能状态,尤其是与蛋白表达、翻译后修饰及信号通路激活相关的关键变化。
在此背景下,蛋白质组学与磷酸化蛋白质组学等多组学技术逐渐成为解析肿瘤生物学行为的重要手段。但针对乳腺癌原发肿瘤与其配对转移性淋巴结的系统性多组学研究仍然相对有限,淋巴结转移过程中蛋白层面的动态重塑及其潜在调控机制尚未得到充分阐明。2026年1月发表于 Protein& Cell1的研究Multi‑omics Analysis Reveals Comprehensive Aberrant Protein and Phosphorylation Characteristics in Breast Cancer and Paired Metastatic Lymph Nodes2 通过多组学整合分析阐述乳腺癌早期转移分子基础,并为未来生物标志物发现及靶向治疗策略提供理论依据。


研究方法学
该研究基于严格配对的人体临床样本,纳入 65 例乳腺癌患者,每例均采集原发肿瘤、配对转移性淋巴结及癌旁组织,所有样本经病理学确认并满足肿瘤细胞比例要求。研究整合全外显子组测序(WES) 和 RNA‑seq 数据,系统分析体细胞突变、拷贝数变异、基因表达及可变剪接特征;以及基于等标记串联质量标签(TMT) 的整体蛋白质组和磷酸化蛋白质组分析。同时,通过多组学整合、生物信息学分析及功能实验(细胞侵袭、Western blot、CD8⁺ T 细胞共培养杀伤实验),从分子机制层面系统解析乳腺癌淋巴结转移的关键驱动过程。
整体实验设计流程示意图见 图 1A
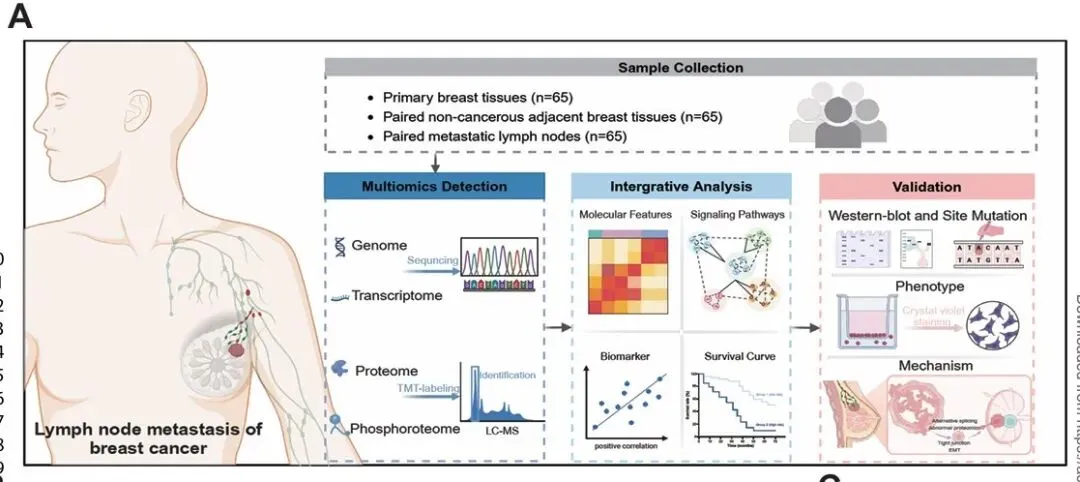
本研究在不同组学层面共纳入 54/58 例原发肿瘤/转移性淋巴结进行 WES,51/55/58 例 NAT/原发肿瘤/转移性淋巴结进行 RNA‑seq,65 对原发肿瘤‑转移性淋巴结完成蛋白质组分析,以及 65/55 例原发肿瘤/转移性淋巴结完成磷酸化蛋白质组分析。
乳腺癌早期转移的整合多组学分析
本研究基于严格配对的多组学数据,系统刻画了乳腺癌早期淋巴结转移的分子特征。基因组层面(图1B)共鉴定出 7,280 个非同义体细胞突变 和 25,988 个体细胞拷贝数变异(SCNV),且原发肿瘤与转移性淋巴结在突变谱上差异较小,提示转移前后新增基因突变有限。
转录组(图1C)分析共定量 16,892 个FPKM>0 的基因;蛋白质组和磷酸化蛋白质组(图1D)分别鉴定 8,588 种蛋白 及 24,178 个高置信度磷酸化位点(来自 5,182 种蛋白),数据质量高、重复性好且无明显批次效应,构建了高质量、多维度的多组学资源。
基因组层面(图1B)/蛋白质组分析图(1C)/磷酸化蛋白质组分析(图1D)
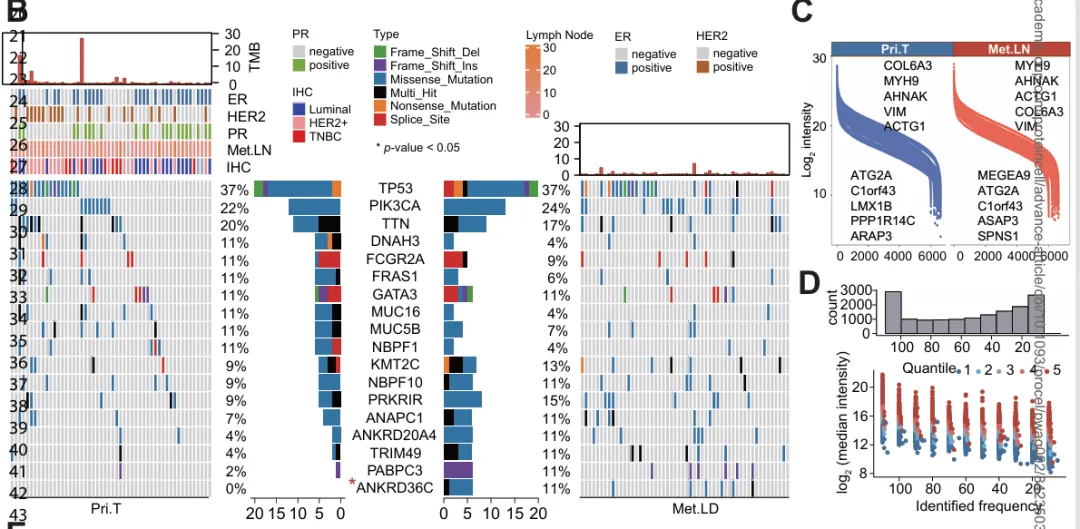
综合多组学分析显示,由于原发肿瘤与转移性淋巴结来源于同一患者,转移前后新增的基因突变数量相对有限;尽管 mRNA 与蛋白整体表达在原发灶与转移灶中呈中度相关(Spearman ρ ≈ 0.4),但并非完全一致,提示转移过程中存在超越转录调控层面的功能重塑。在多条与乳腺癌转移密切相关的通路(如 EMT、Wnt/β‑catenin、HER2 和 Notch)中,基因突变发生频率整体较低,差异主要集中于 CNV 和转录水平,而蛋白质组及磷酸化蛋白质组层面的改变最为显著,表明乳腺癌淋巴结转移更多体现为蛋白功能和信号通路层面的重编程。
淋巴结转移中的蛋白质组改变及潜在生物标志物
多组学分析显示,乳腺癌淋巴结转移过程中基因组层面的改变整体较为有限。在 FUSCC 队列中,仅筛选出18 个高频突变基因,其中 TP53、PIK3CA 和 TTN 为突变频率最高的基因(图 S1E),且其在原发肿瘤与转移性淋巴结中的突变率高度相似(如 TP53:37% vs 37%,PIK3CA:22% vs 24%,TTN:20% vs 17%)。
与 TCGA 数据对比验证表明,本研究中各基因突变频率具有良好的外部一致性(图 S1E)
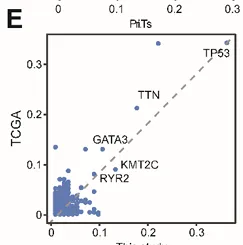
除上述经典突变基因外,多数其他高频突变基因在两者间亦未表现出显著差异,仅 ANKRD36C 在转移性淋巴结中出现特异性突变(11% vs 0%),基因包括:
1)编码染色质修饰酶的基因(KMT2C、ANAPC1);
2)微管相关马达蛋白编码基因(DNAH3、FRAS1);
3)转录调控因子(GATA3、NBPF1、NBPF10);
4) ANKRD 家族成员(ANKRD20A、ANKRD36C)
结合 TCGA 数据验证结果,原发灶与转移灶的突变谱整体高度一致,提示乳腺癌淋巴结转移并非主要由新增体细胞突变驱动。
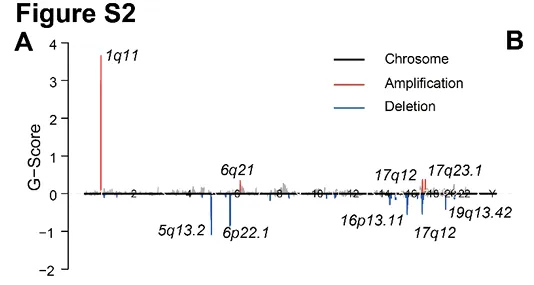
进一步结合拷贝数变异(CNV)分析发现,乳腺癌淋巴结转移过程中存在广泛的基因扩增与缺失事件(图S2A),包括 17q12 和 1q11 染色体区域的显著扩增 以及 6p22.1 和 5q13.2 区域的缺失,其中 17q12 区域检测到与乳腺癌密切相关的 ERBB2 扩增。
然而,多组学整合分析显示,CNV 对下游功能层面的影响呈现出明显的逐级衰减效应:尽管共识别出 138 个扩增基因和 3,367 个缺失基因,但其向转录和蛋白层面的传递受到显著限制,在转移性淋巴结中仅有极少数蛋白表现出显著丰度变化。顺式(cis)效应分析进一步证实这一趋势,即 CNV‑mRNA 层面的相关性最为显著,而在蛋白及磷酸化蛋白层面显著减弱,支持基因结构性改变在乳腺癌早期转移中的功能影响有限。
体细胞拷贝数变异(SCNV)进行了系统分析(图S2A)
相比之下,原发肿瘤与转移性淋巴结在蛋白质组及磷酸化蛋白质组重塑最为显著且具有明确的功能指向性。研究共鉴定 695 个差异蛋白(其中 193 个在转移性淋巴结中上调,502 个下调),主要富集于细胞黏附、ECM‑受体相互作用、细胞骨架调控及多条免疫相关通路。值得注意的是,蛋白层面还观察到 可变剪接通路显著上调,以及 色氨酸代谢和补体‑凝血级联反应通路下调,呈现出区别于转录组的特异性调控特征。
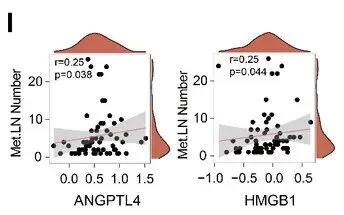
在潜在临床转化层面,研究进一步筛选出ANGPTL4和HMGB1等关键蛋白,其蛋白水平而非转录水平在转移性淋巴结中显著升高(图 S2I),并与淋巴结转移程度密切相关;独立队列血清学验证及 TCGA 生存分析进一步证实,ANGPTL4和HMGB1高表达与不良预后显著相关。总体而言,这些结果表明乳腺癌早期淋巴结转移更多体现为蛋白功能与信号通路层面的重编程,而非基因突变或拷贝数改变的简单累积,并揭示了具有潜在临床应用价值的生物标志物和治疗靶点。
ANGPTL4 和 HMGB1 蛋白表达水平与淋巴结转移数显著相关(图 S2I)
乳腺癌早期转移的磷酸化蛋白质组学洞见
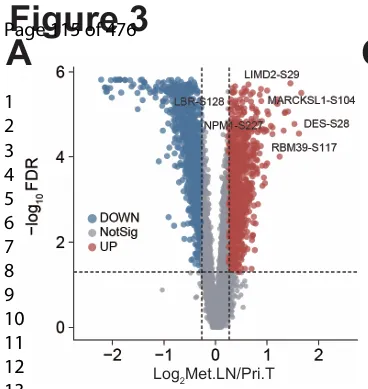
磷酸化蛋白质组分析显示,乳腺癌早期淋巴结转移伴随显著的信号通路重塑。与原发肿瘤相比,转移性淋巴结中共鉴定出 1,170 个上调和 991 个下调的磷酸化位点(图3A),且 PCA 分析显示两者在整体磷酸化谱上明显分离。通路分析提示上皮–间质转化(EMT)和Myc靶基因通路上调,而糖代谢和黏附斑通路下调。
Pri.Ts 与 Met.LNs 之间的磷酸化位点和磷酸化蛋白系统性的差异分析(图3A)
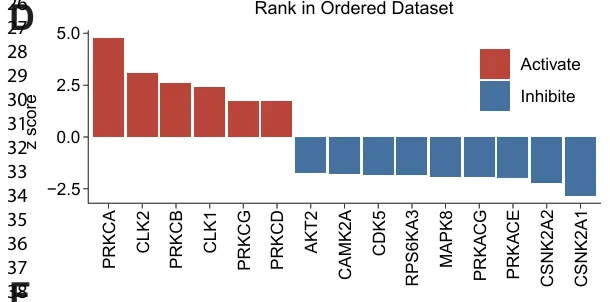
激酶活性推断进一步识别出15 种激酶活性增强(图 3D),其中 PKC 家族成员(PRKCA/B/C/D/G)和 CLK1/2 变化最为显著。
15 种在 Met.LNs 中活性升高的激酶(图 3D)
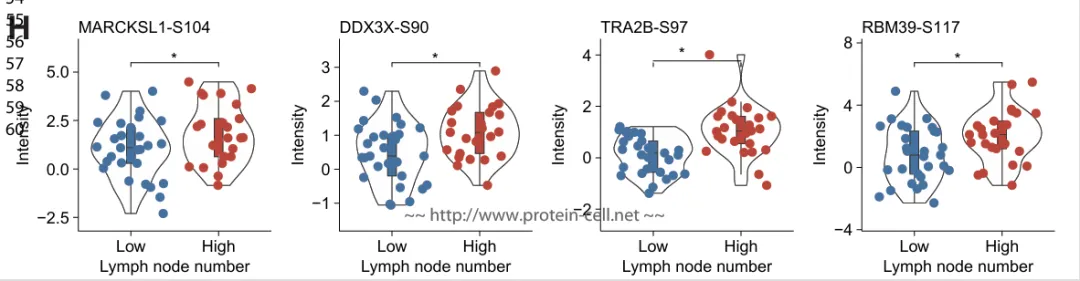
在生物标志物筛选方面,研究通过严格频率和表达标准,从 190 个候选位点中最终确定 62 个在转移性淋巴结中稳定上调的磷酸化位点,其中 9 个关键位点(如 MARCKSL1‑S104、RBM39‑S117、DDX3X‑S90 和 TRA2B‑S97) 具有较高的功能预测评分,并与淋巴结转移负荷显著相关(图3H)。这些位点主要参与 可变剪接与 RNA 调控过程,其上游调控以 PKC 激酶家族为主。总体而言,结果表明乳腺癌早期转移更加体现为磷酸化介导的信号调控与可变剪接重编程,为发现新的功能性标志物和潜在治疗靶点提供了重要依据。
9 个功能评分 >0.5 的显著上调磷酸化位点(图 3G)
异常可变剪接调控乳腺癌早期转移
可变剪接分析显示,乳腺癌早期淋巴结转移伴随着广泛而特异的剪接重塑。RNA‑seq 共鉴定742,279个可变剪接(AS 事件),其中258个AS事件在原发肿瘤与癌旁组织之间存在显著差异,且AS事件与淋巴结转移程度显著相关;
互斥外显子(MXE)是最主要的AS类型。多组学整合分析进一步表明,AS 事件在蛋白及磷酸化层面的影响尤为突出,主要涉及核糖体组装、蛋白翻译及肌动蛋白相关过程。
在调控层面,多种剪接因子和RNA结合蛋白(如 ALYREF、HNRNPK、HNRNPC、HNRNPU) 在转移性淋巴结中仅在蛋白层面上调,而转录层面无明显变化,且其蛋白丰度与淋巴结转移数量呈正相关(图 4F)。
蛋白层面和转录层面的变化(图 4F)
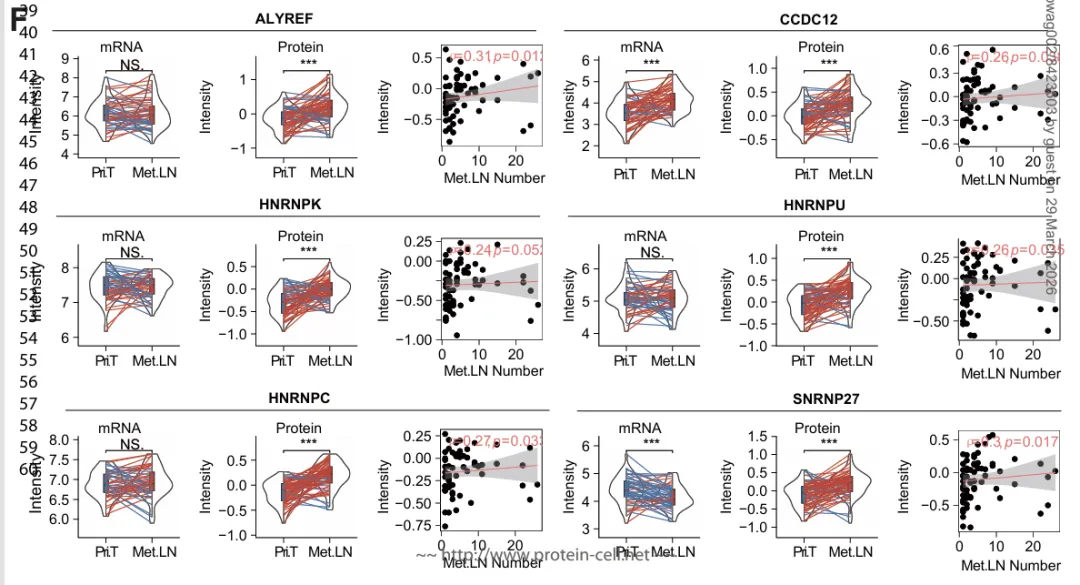
结合 TPM1、MFF、METTL26 和 PRKCB 等高频 AS 靶基因的差异特征,结果表明乳腺癌早期转移更多体现为 AS‑介导的转录后调控和蛋白表达重编程,进一步支持可变剪接及其调控因子作为潜在治疗靶点的生物学意义。
特异性磷酸化位点的鉴定与预后生物标志物验证
基于磷酸化蛋白质组学分析,鉴定出MARCKSL1‑S104和FKBP15‑S320作为与乳腺癌淋巴结转移密切相关的关键磷酸化位点,其磷酸化水平在转移性淋巴结中显著升高,而总蛋白表达无明显变化(图 5A);
原发肿瘤(Pri.Ts)转移性淋巴结(Met.LNs)蛋白变化(图 5A)
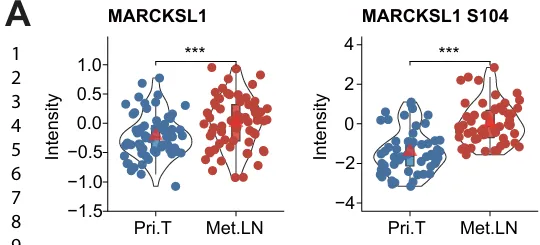
并行反应监测(PRM) 定量进一步证实,MARCKSL1‑S104 在 57%、FKBP15‑S320 在 67% 的转移淋巴结样本中显著上调。MARCKSL1‑S104 与 FKBP15‑S320 的磷酸化在乳腺癌向淋巴结转移中具有重要功能意义。功能实验表明,这两个位点的磷酸化显著增强乳腺癌细胞迁移能力,并通过调控紧密连接、黏附斑和细胞迁移相关通路发挥作用。
机制分析显示,PRKCB 是上述磷酸化事件的关键上游激酶,且其活性受剪接因子(HNRNPU)调控;敲低 HNRNPU 或抑制 PRKCB 均可显著降低 MARCKSL1‑S104/FKBP15‑S320 的磷酸化水平并抑制肿瘤细胞迁移。
总体而言,本研究揭示了 “HNRNPU–PRKCB–磷酸化轴” 在乳腺癌早期淋巴结转移中的关键作用,并确立了具有潜在临床应用价值的预后生物标志物和干预靶点。
原发肿瘤与配对转移性淋巴结的免疫特征
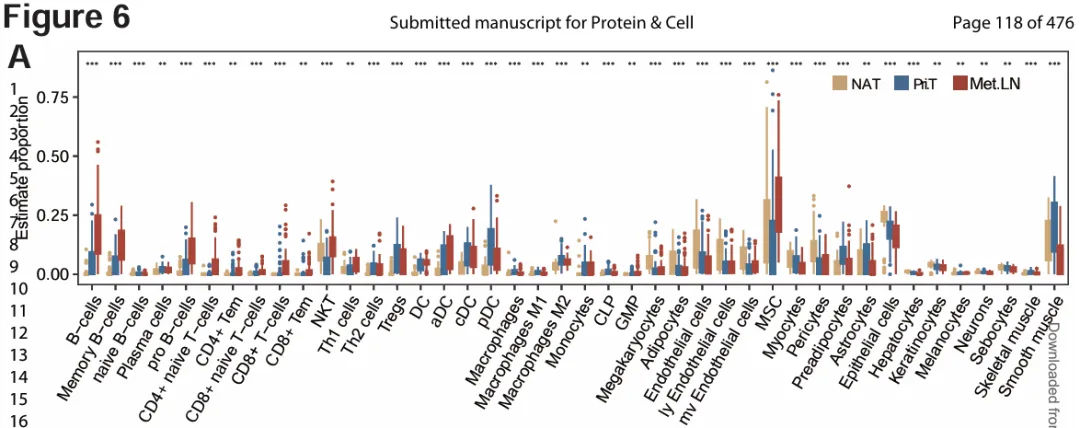
免疫微环境分析显示,乳腺癌淋巴结转移伴随显著的免疫重塑。xCell 分析表明,与原发肿瘤相比,转移性淋巴结中CD8⁺T细胞、B细胞、NK细胞、活化树突状细胞(aDCs)和Th1细胞,同时免疫抑制性细胞(如调节性 T 细胞和 M2 型巨噬细胞)的特征也明显增强(图 6A),同时调节性 T 细胞和 M2 巨噬细胞等免疫抑制细胞亦明显增加。免疫相关通路(如 JAK‑STAT、B 细胞受体和 NK 细胞介导的细胞毒作用)在转移性淋巴结中显著上调,该特征主要集中于 Luminal 和 HER2 阳性亚型。在TNBC中,转移淋巴结与原发灶之间并未检测到显著的免疫细胞浸润差异。
xCell 方法评估免疫细胞浸润水平(图 6A)
进一步机制分析发现,PRKCB‑介导的MARCKSL1‑S104和FKBP15‑S320 磷酸化与PD‑L1、PD‑1和CTLA4 等免疫检查点分子的表达呈正相关;在细胞实验中,模拟磷酸化状态可显著上调 PD‑L1 表达并抑制 CD8⁺ T 细胞介导的肿瘤细胞凋亡。
总体而言,结果表明 “PRKCB‑磷酸化‑免疫检查点”轴 在乳腺癌淋巴结转移中的免疫逃逸中发挥关键作用,并提示 Luminal 型患者可能更适合免疫治疗干预策略。

讨论与总结
本研究通过整合原发肿瘤与配对转移性淋巴结的多组学数据,系统揭示了乳腺癌淋巴结转移的分子机制。结果表明,基因突变和转录改变对转移的驱动作用有限,而蛋白质组及磷酸化蛋白质组的重塑最为显著。
研究鉴定出 62 个与转移相关的关键磷酸化位点,其中 MARCKSL1‑S104 和 FKBP15‑S320 在转移灶中显著升高,并由 PRKCB 等 PKC 家族激酶调控;功能实验进一步证实抑制 PRKCB 可有效抑制肿瘤细胞的增殖与迁移。
免疫层面分析显示,转移性淋巴结中免疫信号增强的同时伴随免疫检查点分子上调,提示存在免疫逃逸机制。总体而言,本研究强调乳腺癌早期淋巴结转移主要体现为蛋白功能和信号通路层面的重编程,并为精准诊断和干预策略提供了重要理论依据。

参考资料

