第1课时 醇
[核心素养发展目标]1.通过认识羟基的结构,了解醇类的结构特点,进而从化学键、官能团的角度理解醇类消去反应、催化氧化反应的特征和规律。2.通过对乙醇性质的学习,能利用反应类型的规律判断、说明和预测醇类物质的性质。
一、醇的概述
羟基与碳原子相连的化合物称为醇。
1.醇的分类
(1)根据醇分子中所含羟基的数目,可以分为
一元醇:如甲醇(CH3OH)
二元醇:如乙二醇()
多元醇:如丙三醇(又叫甘油)()
(2)根据烃基种类,可以分为
脂肪醇:如乙醇(CH3CH2OH)
芳香醇:如苯甲醇(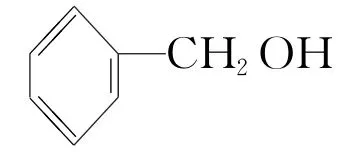 )
)
其中由链状烷烃衍生出来的一元醇,叫做饱和一元醇,通式:,可简写为R—OH。
2.醇的物理性质
(1)三种重要的醇
名称 | 状态 | 溶解性 | 用途 |
甲醇 | 无色、具有的液体 | 溶于水 | 化工原料,车用燃料 |
乙二醇 | 无色、黏稠的液体 | 溶于水和乙醇 | 化工原料,汽车防冻液 |
丙三醇 | 化工原料,配制化妆品 |
特别提醒甲醇有毒,误服会损伤视神经,甚至致人死亡。
(2)物理性质
①在水中的溶解度
a.饱和一元醇在水中的溶解度随分子中碳原子数的增加而;
b.羟基个数越多,溶解度。
②沸点
a.相对分子质量相近的醇和烷烃相比,醇的沸点远远烷烃;
b.饱和一元醇随分子中碳原子数的增加,沸点逐渐;
c.碳原子数目相同,羟基的个数越多沸点越。
醇的命名
注意当醇分子中含有多个羟基时,应选择含羟基最多的最长碳链为主链,羟基的个数用“二”“三”等表示。如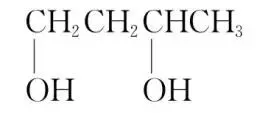 的名称为1,3⁃丁二醇。
的名称为1,3⁃丁二醇。
(1)乙醇与甲醚(CH3—O—CH3)互为碳架异构()
(2)分子中含有—OH的有机物是醇()
(3)质量分数为95%的乙醇溶液常作消毒剂()
(4)向工业酒精中加入生石灰,然后加热蒸馏,可制得无水乙醇()
(5)沸点由高到低的顺序为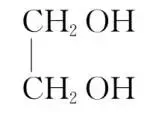 3CH2OH>CH3CH2CH3()
3CH2OH>CH3CH2CH3()
(6)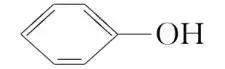 与
与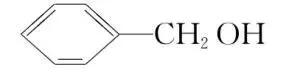 互为同系物()
互为同系物()
1.甲醇、乙醇、丙醇可与水以任意比例互溶的原因为。
2.醇比同碳原子烃的沸点高的原因为。
1.结合下表数据分析,下列关于乙醇、乙二醇的说法不合理的是( )
物质 | 分子式 | 沸点/℃ | 溶解性 |
乙醇 | C2H6O | 78 | 与水以任意比例混溶 |
乙二醇 | C2H6O2 | 197.3 | 与水和乙醇以任意比例混溶 |
A.二者的溶解性与其在水中能够形成氢键有关
B.可以采用蒸馏的方法将二者进行分离
C.丙三醇的沸点应该高于乙二醇的沸点
D.二者组成和结构相似,互为同系物
2.请写出分子式为C3H8O的有机化合物的同分异构体的结构简式。
(1)醇因分子中烃基碳架结构不同和官能团羟基位置不同产生同分异构体。
(2)脂肪醇和等碳原子数的醚互为官能团异构。
二、醇的化学性质——以乙醇为例
1.取代反应
(1)醇与氢卤酸的取代反应
乙醇与浓氢溴酸发生取代反应:
。
(2)醇分子间脱水成醚的取代反应

通过网盘分享的文件:【学生用书Word版文档】全书等5个文件
链接: https://pan.baidu.com/s/1sFAOgLwdgopx5f4PfrFk6A?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享