
【实验目的】
1.加深对同周期、同主族元素性质递变规律的认识。
2.体会元素周期表和元素周期律在学习元素化合物知识中的重要作用。
【实验仪器】
试管、试管夹、试管架、量筒、胶头滴管、酒精灯、白色点滴板、镊子、砂纸、火柴。
【实验药品】
镁条、新制的氯水、溴水、NaBr溶液、NaI溶液、MgCl2溶液、AlCl3溶液、氨水、2 mol·L-1 NaOH溶液、2 mol·L-1 盐酸、酚酞溶液、蒸馏水。
【实验步骤】
1.同主族元素性质的递变
(1)在点滴板的3个孔穴中分别滴入3滴NaBr溶液、NaI溶液和新制的氯水,然后向NaBr溶液和NaI溶液中各滴入3滴新制的氯水,观察到的现象是滴入浅黄绿色的氯水后,NaBr溶液________,NaI溶液__________。化学方程式:____________________,____________________。
(2)在点滴板的两个孔穴中分别滴入3滴NaI溶液和溴水,然后向NaI溶液中滴入3滴溴水,观察到的现象是NaI溶液__________。化学方程式:____________________。
结论:卤素单质的氧化性:__________。卤族元素的非金属性:__________。
2.同周期元素性质的递变
(1)钠、镁与水的反应
①向盛有冷水的烧杯中加入一块绿豆粒大小的钠块,向盛有冷水的试管中加入一小块已用砂纸打磨好的镁条,并分别向烧杯和试管中滴入3滴酚酞溶液,观察到烧杯中钠______________,___________, __________,__________,溶液变__________,试管内镁条表面产生__________,镁条周围溶液变为__________。
化学方程式:______________________________。
②向一支试管中加入少量冷水,并加入一小块已用砂纸打磨好的镁条,用酒精灯加热至沸腾,滴入3滴酚酞溶液,观察到的现象是__________,溶液变为__________。
结论:与水反应的剧烈程度:__________,金属性:__________。镁与热水反应比与冷水反应快。
(2)镁和铝的金属性、非金属性
①向一支试管中加入MgCl2溶液,然后滴加氨水,直到不再产生白色沉淀为止。将Mg(OH)2沉淀分装在两支试管中,向一支试管中滴加2 mol·L-1 盐酸,向另一支试管中滴加2 mol·L-1 NaOH溶液,边滴加边振荡,观察到的现象是_____________________________。反应的化学方程式:___________________________。
②向另一支试管中加入AlCl3溶液,然后滴加氨水,直到不再产生白色沉淀为止。将Al(OH)3沉淀分装在两支试管中,向一支试管中滴加2 mol·L-1 盐酸,向另一支试管中滴加2 mol·L-1 NaOH溶液,边滴加边振荡,观察到的现象是______________________。反应的化学方程式:_____________________,____________。
结论:Mg(OH)2是中强碱;Al(OH)3是两性氢氧化物。这说明铝虽是金属,但已表现出一定的非金属性。金属性:____________。
综合以上实验可得出:同一主族元素,从上到下,随着原子序数的增加,非金属性__________,金属性__________。 同一周期元素,从左至右,随着原子序数的增加,金属性________________,非金属性__________。
【问题和讨论】
1.实验中所用氯水为什么要用新制的?
2.通过本实验活动,你对原子结构与元素性质的关系及元素周期律(表)有什么新的认识?
3.为了比较氯元素与碳元素的非金属性强弱,可否用盐酸与碳酸钠反应生成二氧化碳,得出非金属性氯大于碳?原因是什么?
4.把一小块钠投入到氯化镁溶液中,钠并不能置换出镁,能否说明钠元素的金属性不如镁?

1.(2024·河南周口高一段考)在点滴板①②③三个孔穴中分别滴入3滴新制的氯水,再向②③中分别滴入3滴NaBr溶液、NaI溶液;向④⑤两个孔穴中分别滴入3滴溴水,向⑤中滴入3滴NaI溶液。下列关于该实验的说法正确的是( )
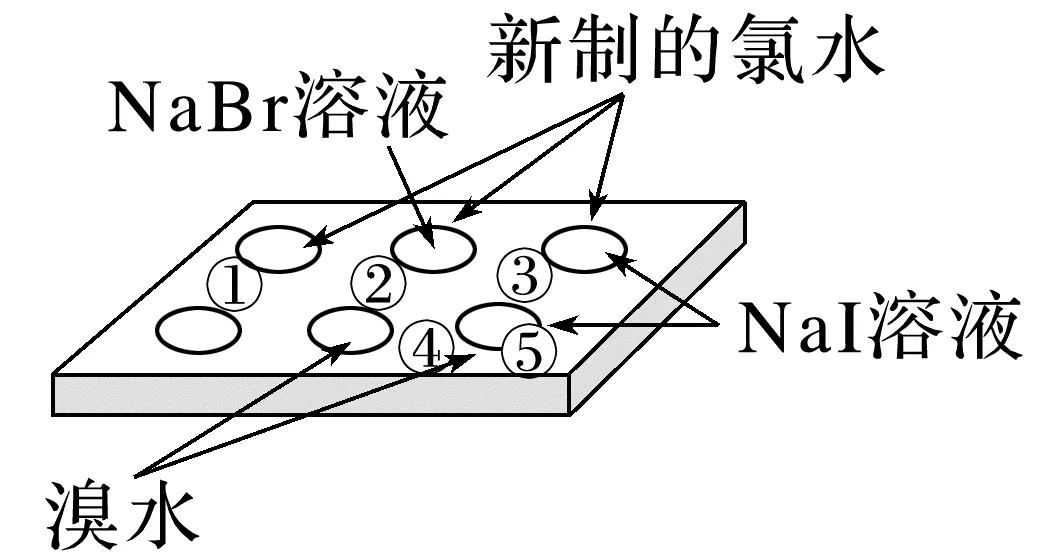
A.上述实验中可以探究同主族元素性质的递变规律
B.①②③可得出氧化性:Cl2>Br2>I2
C.若用久置的氯水进行上述实验,实验现象与原实验现象完全相同
D.新制氯水中存在大量的次氯酸分子
2.将甲、乙两种金属的性质相比较,已知:①甲与H2O反应比乙与H2O反应剧烈;②单质甲能从乙的盐溶液中置换出单质乙;③甲的最高价氧化物对应的水化物碱性比乙的最高价氧化物对应的水化物碱性强;④与某非金属反应时甲原子失电子数目比乙原子失电子数目多;⑤甲单质的熔、沸点比乙的低;⑥高价阳离子氧化性甲比乙弱。能说明甲的金属性比乙强的是( )
A.①④B.①②③⑥
C.③⑤D.①②③④⑤
3.中学化学中很多“规律”都可以类推,下列根据有关“规律”推出的结论正确的是( )
A.Na在空气中燃烧会生成Na2O2,故Li在空气中燃烧也会生成Li2O2
B.浓硫酸可以干燥HCl气体,故也可用浓硫酸干燥HI气体
C.硅是半导体材料,故同族的锗也是半导体材料
D.卤素单质随核电荷数的增加熔点升高,故碱金属单质的熔点也随核电荷数的增加而升高
4.某化学课外活动小组为了验证元素化学性质的递变规律,进行如下实验探究。
Ⅰ.探究1:验证同周期X、Y、Z三种元素金属性递变规律
实验内容 | 实验现象 |
各取1.0 g金属X和金属Z,分别加入到5 mL水中 | 金属X与水反应比金属Z剧烈 |
各取1.0 g的金属Z和金属Y(形状相同),分别加入到5 mL 1.0 mol·L-1盐酸中 | 金属Z与盐酸反应比金属Y剧烈 |
通过实验验证三种元素金属性由强到弱的顺序是,则下列判断正确的是(填字母)。
A.原子序数:Y>Z>X
B.原子的最外层电子数:X>Y>Z
C.原子半径:Y>Z>X
D.Y的最高价氧化物对应水化物的碱性最强
Ⅱ.探究2:验证氯元素的非金属性比硫元素的非金属性强,设计如下实验:
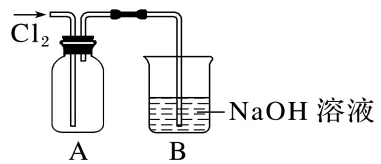
(1)装置A中盛放的试剂是(填字母),反应的化学方程式是。
A.Na2SO3溶液
B.Na2S溶液
通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享