
【研究目的】
铁是人体必需的微量元素。食用富含铁元素的食品,可以补充人体所需的铁元素。通过化学实验的方法检验食品中的铁元素,体验实验研究的一般过程和化学知识在实际中的应用。
【阅读材料】
一、铁元素在人体中的作用
成年人体内含有4~5克铁,根据在体内的功能状态可分成功能性铁和储存铁两部分。功能性铁存在于血红蛋白、肌红蛋白和一些酶中,约占体内总铁量的70%。其余30%为储存铁,主要储存在肝、脾和骨髓中。
铁是合成血红蛋白的主要原料之一。血红蛋白的主要功能是把新鲜氧气运送到各组织。铁缺乏时不能合成足够的血红蛋白,造成缺铁性贫血。铁还是体内参与氧化还原反应的一些酶和电子传递体的组成部分,如过氧化氢酶和细胞色素都含有铁。
二、人体铁元素的来源
动物内脏(特别是肝脏)、血液、鱼、肉类都是富含血红素铁的食品。深绿叶蔬菜所含铁虽不是血红素铁,但摄入量多,所以仍是我国人民膳食铁的重要来源。
三、常用的二、三价铁离子的检验方法
1.苯酚检验法
铁离子与苯酚反应,可生成显紫色的络离子(络合物)。
2.硫氰化物鉴别法
取溶液各少量,滴入可溶性硫氰化物(如KSCN、NaSCN等)溶液,变红色的是含铁离子的溶液,因为生成了显红色的络合物。
3.碱鉴别法
加入氢氧化钠、氨水或氢氧化钾等碱性溶液后,有红褐色沉淀生成,并检测开始沉淀和沉淀完全时的pH,发现从开始沉淀到沉淀完全时溶液的pH(常温下)为2.3~3.2的是铁离子。
4.铁氰化钾溶液法(赤血盐溶液)
亚铁离子在酸性溶液中与铁氰化钾溶液生成蓝色沉淀,称为滕氏蓝。
【实验仪器】
研钵、烧杯、剪刀、漏斗、玻璃棒、试管、滴管、滤纸。
【实验药品】
菠菜、蒸馏水、稀硝酸、KSCN溶液。
【实验步骤】
1.取新鲜的菠菜10 g,将菠菜剪碎后放在研钵中研磨,然后倒入烧杯中,加入30 mL蒸馏水,搅拌。将上述浊液过滤,得到的滤液作为试验样品。
2.取少许试验样品加入试管中,然后加入少量稀硝酸(稀硝酸具有氧化性),再滴加几滴KSCN溶液,振荡,观察到溶液___________。
结论:菠菜中___________铁元素。

1.在实验中由于菠菜汁有颜色,所以对于实验现象的观察有一定的影响,想一想可以怎么改进这个实验。
2.实验中加入稀硝酸的目的是什么?

1.(2024·安徽宣城高一期末)“检验菠菜中的铁元素”要经历下列步骤,有关实验装置或实验原理中,不合理的是( )
2.(2024·湖北荆州中学高一期末)某兴趣小组同学为探究黑木耳中含铁量,进行如下实验。
已知:ⅰ.黑木耳富含蛋白质、糖类、卵磷脂、铁及一些还原性物质(如维生素C)等。每100 g黑木耳含铁量高达185 mg。
ⅱ.紫红色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。
ⅲ.K3[Fe(CN)6]与亚铁离子反应生成特征蓝色沉淀。
Ⅰ.为确定黑木耳中含有铁元素,甲同学设计实验方案如下。
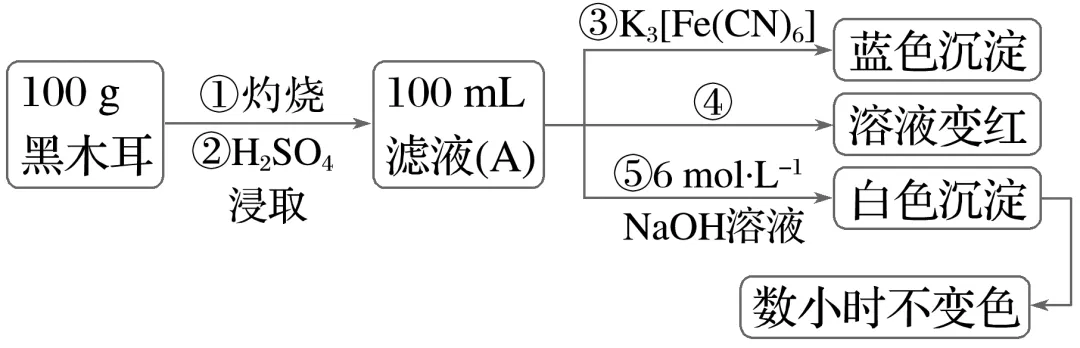
(1)步骤②得到滤液A的操作是。
(2)步骤④检验Fe3+所用试剂是溶液。
(3)下列有关上述实验得出的结论是(填字母,下同)。
a.黑木耳中一定含Fe2+和Fe3+
b.滤液A中一定含Fe2+和Fe3+
c.白色沉淀中一定含Fe(OH)2
Ⅱ.为测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
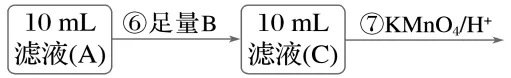
(4)可选做试剂B的物质是。
a.Na b.Zn c.Fe d.Cu
(5)步骤⑦中观察到的实验现象是,
反应的离子方程式是。
(6)若乙同学实验操作规范,但测得含铁量远大于实际的含量,其可能的原因是。
3.铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
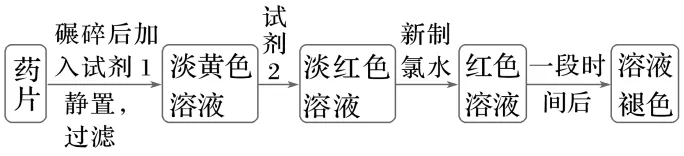
试回答下列问题:
(1)试剂1是,试剂2是,加入新制氯水后溶液中发生反应的离子方程式是、 。
(2)加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为,写出+2价Fe在空气中转化为+3价Fe的化学方程式:。
(3)该同学猜想红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗?。若你认为合理,请说明理由(若你认为不合理,该空不作答);若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不作答)。

通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享