 2课时 有机化合物中的共价键、同分异构现象及表示方法
2课时 有机化合物中的共价键、同分异构现象及表示方法
[核心素养发展目标]1.了解有机化合物中共价键的类型,理解键的极性与有机反应的关系。2.理解有机化合物的同分异构现象,能判断有机化合物的同分异构体。
一、有机化合物中的共价键
在有机化合物的分子中,碳原子通过与其他原子形成不同类型的共价键,共价键的_________和对有机化合物的性质有很大的影响。
1.有机化合物中共价键的类型
(1)根据原子轨道的重叠方式可分为σ键和π键。
| σ键 | π键 |
原子轨道重叠方式 | 沿键轴方向以“”的形式相互重叠 | 以“”的形式从侧面重叠 |
原子轨道重叠程度 | 大 | 小 |
键的强度 | 较大 | 较小 |
能否绕键轴旋转 | 能,化学键断裂 | |
(2)根据成键原子形成共用电子对的数目可分为单键、、,它们与σ键和π键的关系:
有机化合物
的共价键
(3)共价键的类型与有机反应类型的关系
σ键断裂,能发生反应,如CH4等;π键比较断裂,π键更活泼,能发生反应,如CH2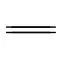 CH2、CH≡CH等。
CH2、CH≡CH等。
2.共价键的极性与有机反应
不同成键原子间的差异,会使共用电子对发生偏移,使共价键产生极性,在一定条件下发生断裂。有机化合物的及其往往是发生化学反应的活性部位。
实例分析(教材实验1⁃1)
(1)水、无水乙醇分别与钠反应的比较
实验操作 |
|
|
实验现象 | 金属钠,反应 | 金属钠,反应平稳 |
化学方程式 | |
|
实验结论 | CH3CH2—OH分子中氢氧键的极性比H—OH分子中氢氧键的极性 , 之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质 |
(2)乙醇与氢溴酸的反应
由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,也可断裂,如乙醇与氢溴酸的反应:。
3.有机反应的特点
共价键的断裂需要吸收能量,而且有机化合物分子中共价键断裂的位置存在多种可能。相对无机反应,有机反应一般反应速率,副反应,产物比较。
(1)σ键比π键牢固,所以不会断裂()
(2)乙烯分子中含有π键,所以化学性质比甲烷活泼()
(3)乙酸与钠反应比水与钠反应更剧烈,是因为乙酸分子中氢氧键的极性更强()
(4)共价键的极性强弱不仅取决于成键原子双方电负性差值的大小,还取决于共价键所处的环境()
(5)CH3COOH有酸性,而C2H5OH没有,体现了基团之间的相互影响()
1.请从化学键和官能团的角度分析下列反应中有机化合物的变化。
①CH4+Cl2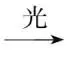 CH3Cl+HCl
CH3Cl+HCl
②CH2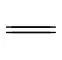 CH2+Br2
CH2+Br2 CH2Br—CH2Br
CH2Br—CH2Br
2.某有机物分子的结构简式为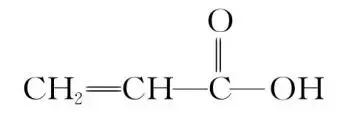 ,该分子中有个σ键,个π键,(填“有”或“没有”)非极性键。根据共价键的类型和极性可推测该物质可发生反应和反应,与钠反应的剧烈程度比水与钠反应的剧烈程度。原因是。
,该分子中有个σ键,个π键,(填“有”或“没有”)非极性键。根据共价键的类型和极性可推测该物质可发生反应和反应,与钠反应的剧烈程度比水与钠反应的剧烈程度。原因是。
利用碳原子成键方式的有关知识,分析和预测有机分子在反应中可能的断键部位。可以从两个角度进行分析:一是判断分子中是否有双键、三键等不饱和键。若分子中有不饱和键,在加成反应中反应活性就会较强;二是寻找分子中有极性的化学键,通常,不同元素的两个原子成键时所形成的共价键是极性键,极性键反应活性较强,在反应中是可能的断键部位。
1.乙酸、水和乙醇的分子结构如表所示,三者结构中的相同点是都含有氢氧键,下列说法错误的是()
物质 | 结构 |
乙酸 | 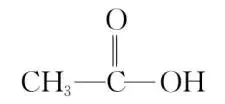
|
水 | H—OH |
乙醇 | CH3—CH2—OH |
A.氢氧键的极性:乙酸>水>乙醇

通过网盘分享的文件:【学生用书Word版文档】全书等5个文件
链接: https://pan.baidu.com/s/1sFAOgLwdgopx5f4PfrFk6A?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享