

第四节 沉淀溶解平衡
第1课时 难溶电解质的沉淀溶解平衡
[核心素养发展目标] 1.掌握难溶电解质存在沉淀溶解平衡及影响因素。2.掌握溶度积常数的概念并能进行简单计算、判断反应进行的方向。
一、沉淀溶解平衡及影响因素
1.25 ℃时,溶解性与溶解度的关系
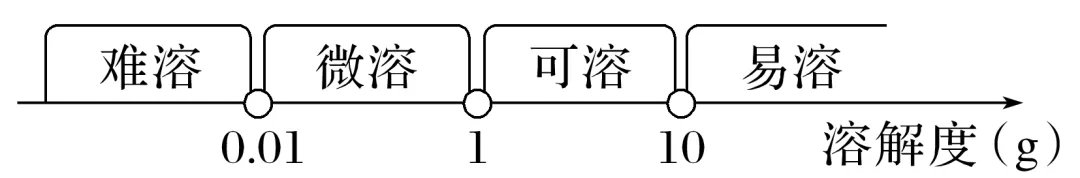
特别提醒 大多数电解质的溶解度随温度升高而增大,但也有例外,如Ca(OH)2,温度越高,溶解度越小。
2.沉淀溶解平衡(以AgCl为例分析)
(1)沉淀溶解平衡建立
AgCl在溶液中存在下述两个过程:一方面,在水分子作用下,少量Ag+和Cl-脱离AgCl的表面进入水中,即________过程;另一方面,溶液中的Ag+和Cl-受AgCl表面阴、阳离子的吸引,回到AgCl的表面析出,即________过程。在一定温度下,当沉淀和溶解的速率相等时,达到平衡状态,得到AgCl的________。
(2)沉淀溶解平衡的概念
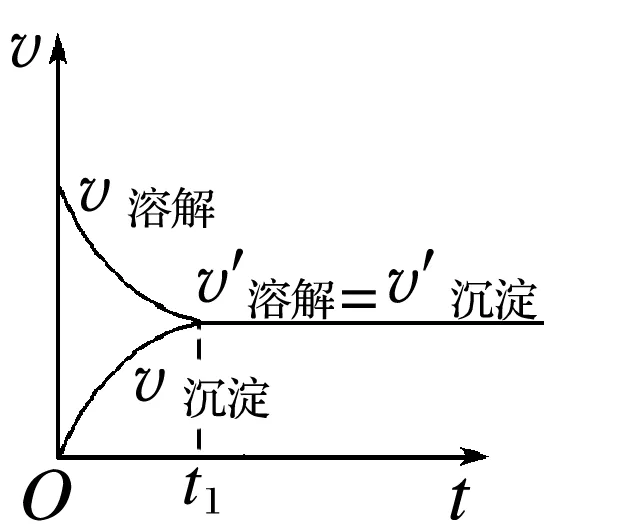
一定温度下,当沉淀和溶解的速率________时,即建立了动态平衡,叫做沉淀溶解平衡。
(3)沉淀溶解平衡方程式
以AgCl沉淀溶解平衡为例:AgCl(s)溶解沉淀Ag+(aq)+Cl-(aq)。
特别提醒 ①要标明各微粒的状态;②要与AgCl电离方程式区分开,强电解质完全电离:AgCl===Ag++Cl-。
(4)沉淀完全的判断
化学上通常认为,当溶液中剩余离子的浓度小于________________时,已沉淀完全。
3.难溶电解质沉淀溶解平衡的影响因素
(1)内因(决定因素):难溶电解质本身的性质。
(2)外因:温度、浓度等条件的影响符合勒夏特列原理。
(3)实例分析
已知沉淀溶解平衡:Mg(OH)2(s)Mg2+(aq)+2OH-(aq),请分析当改变下列条件时,对该沉淀溶解平衡的影响,填写下表(浓度变化均指平衡后和原平衡比较):
条件改变 | 移动方向 | c(Mg2+) | c(OH-) |
加少量水 | | | |
升温 | | | |
加MgCl2(s) | | | |
加盐酸 | | | |
加NaOH(s) | | | |

(1)BaSO4在相同物质的量浓度的硫酸钠和硫酸铝溶液中的溶解度相同( )
(2)升高温度,沉淀溶解平衡一定正向移动( )
(3)向一定量的饱和NaOH溶液中加入少量Na2O固体,恢复到原来温度时,溶液中的Na+总数不变( )
(4)难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动( )

1.常温下,把足量熟石灰放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s)Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的叙述错误的有__________________(填序号)。
(1)升高温度,平衡逆向移动
(2)恒温下,向溶液中加入CaO,溶液的pH升高
(3)给溶液加热,溶液的pH升高
(4)向溶液中加入少量NaOH固体,Ca(OH)2固体增多
(5)向溶液中加入Na2CO3溶液,Ca(OH)2固体增多
2.将AgCl分别放入①5 mL H2O、②10 mL 0.2 mol·L-1 MgCl2溶液、③20 mL 0.5 mol·L-1 AgNO3溶液、④40 mL 0.1 mol·L-1 HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是________(填序号)。
3.牙齿表面有一层硬的成分为Ca5(PO4)3OH的物质保护,它在唾液中存在下列平衡:Ca5(PO4)3OH(s)5Ca2+(aq)+3PO3-4(aq)+OH-(aq)。
(1)在牙膏中添加适量的Ca2+或PO3-4,能否保护牙齿?为什么?
______________________________________________________________________________
______________________________________________________________________________
(2)多吃酸性食物或食用食醋对保护牙齿有利吗?为什么?
______________________________________________________________________________
______________________________________________________________________________
二、溶度积常数
1.概念
难溶电解质的沉淀溶解平衡也存在________,称为________,简称溶度积,符号为________。
2.表达式
AmBn(s)mAn+(aq)+nBm-(aq)
Ksp=________________________________________________________________________。
如:Fe(OH)3(s)Fe3+(aq)+3OH-(aq)
Ksp=c(Fe3+)·c3(OH-)。
3.影响因素
溶度积Ksp只与__________________________________________________________的性质和
________有关。
4.Ksp的意义
反映了难溶电解质在水中的溶解能力。
5.应用
定量判断给定条件下有无沉淀生成。
离子积(Q):对于AmBn(s)mAn+(aq)+nBm-(aq),任意时刻Q=cm(An+)·cn(Bm-)。
(1)Q>Ksp,溶液过饱和,有________析出,直至溶液________,达到新的平衡。
(2)Q=Ksp,溶液饱和,沉淀与溶解处于________________。
(3)Q<Ksp,溶液未饱和,无________析出,若加入过量难溶电解质,难溶电解质______直至溶液________。

(1)溶度积是沉淀溶解平衡时难溶电解质在溶液中的各离子浓度的乘积( )
(2)溶度积常数Ksp只受温度影响,温度升高,Ksp一定增大( )
(3)Ksp越小,难溶电解质在水中的溶解能力一定越弱( )
(4)改变外界条件使沉淀溶解平衡正向移动,Ksp一定增大( )
(5)可利用溶液混合后的Q与Ksp的相对大小来判断溶液混合后是否有沉淀生成( )

1.常温下,Ksp(PbI2)=8.5×10-9。取适量黄色PbI2粉末溶于水,充分搅拌后得到浊液,过滤。在滤液中加入少量KI后测得c(I-)=1.0×10-2 mol·L-1。下列说法正确的是( )
A.Ksp(PbI2)减小
B.溶液中c(I-)减小
C.产生黄色沉淀
D.溶液中c(Pb2+)=8.5×10-7 mol·L-1
2.已知几种难溶电解质在25 ℃时的溶度积。
化学式 | AgCl | AgBr | AgI | Mg(OH)2 | Ag2CrO4 |
Ksp | 1.8×10-10 | 5.4×10-13 | 8.5×10-17 | 5.6×10-12 | 2.0×10-12 |
(1)25 ℃时AgCl(s)、AgBr(s)、AgI(s)溶于水形成的饱和溶液中,c(Ag+)大小关系能否直接判断?三种物质的溶解能力由大到小如何排序?
______________________________________________________________________________
______________________________________________________________________________
(2)能否利用上表数据直接比较AgCl、Mg(OH)2的溶解能力?计算分析二者溶解能力的大小?
______________________________________________________________________________
______________________________________________________________________________
(3)25 ℃时,氯化银的饱和溶液和铬酸银的饱和溶液中,Ag+浓度大小顺序为__________________,由此可得出________更难溶。
(4)将等体积的4×10-3 mol·L-1的AgNO3溶液和4×10-3 mol·L-1的K2CrO4溶液混合,请通过计算说明是否有Ag2CrO4沉淀产生。
______________________________________________________________________________
______________________________________________________________________________
(5)25 ℃时,取一定量含有I-、Cl-的溶液,向其中滴加AgNO3溶液,当AgCl和AgI同时沉淀时,计算溶液中cI-cCl-=___________________________________________________。

(1)Ksp只与难溶电解质的性质和温度有关,而与沉淀的量和溶液中的离子浓度无关。
(2)对于同类型物质(如AgCl、AgBr、AgI等),可直接用溶度积比较难溶电解质的溶解能力,Ksp越大,难溶电解质在水中的溶解能力越强。
(3)对于不同类型的物质,Ksp不能直接作为比较依据,而应通过计算将Ksp转化为饱和溶液中溶质的物质的量浓度来确定溶解能力的强弱。
3.利用上题溶度积数据,分析25 ℃时,在Cl-、Br-和CrO2-4的浓度均为0.010 mol·L-1的混合溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为______________________。

通过网盘分享的文件:同步PPT课件等3个文件
链接: https://pan.baidu.com/s/1WiBBQCVHpFgaci5JN4S3LA?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享