n
第2课时 杂化轨道理论
[核心素养发展目标]1.通过对杂化轨道理论的学习,能从微观角度理解中心原子的杂化轨道类型对分子空间结构的影响。2.掌握中心原子杂化轨道类型判断的方法,建立分子空间结构分析的思维模型。
一、杂化轨道及其类型
1.用杂化轨道理论解释甲烷分子的形成
当碳原子与4个氢原子形成甲烷分子时,碳原子的轨道和3个轨道发生混杂,混杂时保持轨道总数不变,却得到4个新的能量相同、方向不同的轨道,各指向正面体的4个顶角,夹角为109°28',称为sp3杂化轨道。当碳原子跟4个氢原子结合时,碳原子以4个杂化轨道分别与4个H原子的1s轨道重叠,形成4个C—H σ键,因此呈现形的空间结构。
2.杂化轨道的形成及特点
3.杂化轨道的类型
(1)sp3杂化轨道
sp3杂化轨道是由个s轨道和个p轨道杂化而成的,sp3杂化轨道间的夹角为,空间结构为(如图所示)。
(2)sp2杂化轨道
sp2杂化轨道是由个s轨道和个p轨道杂化而成的。sp2杂化轨道间的夹角都是,呈(如图所示)。
(3)sp杂化轨道
sp杂化轨道是由个s轨道和个p轨道杂化而成的。sp杂化轨道间的夹角为,呈(如图所示)。
1.正误判断
(1)发生轨道杂化的原子一定是中心原子( )
(2)原子轨道的杂化只有在形成分子的过程中才会发生,孤立的原子是不可能发生杂化的( )
(3)只有能量相近的轨道才能杂化( )
(4)杂化轨道能量更集中,有利于牢固成键( )
(5)杂化轨道只用于形成σ键或用来容纳未参与成键的孤电子对,未参与杂化的p轨道可用于形成π键( )
(6)2s轨道和3p轨道能形成sp2杂化轨道( )
2.下列分子的中心原子杂化轨道类型相同的是( )
A.CO2与SO2B.CH4与NH3
C.BeCl2与BF3D.C2H2与C2H4
3.下列分子或离子的中心原子为sp3杂化,且杂化轨道容纳了1个孤电子对的是( )
A.CH4、NH3B.BBr3、S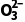
C.SO2、BeCl2D.PCl3、H3O+
4.下列分子中的中心原子的杂化方式为sp杂化,分子的空间结构为直线形且分子中没有形成π键的是( )
A.CH≡CHB.CO2
C.BeCl2D.BF3
以碳原子为中心原子的分子中碳原子的杂化轨道类型
(1)没有形成π键,采取sp3杂化,如CH4、CCl4等。
(2)形成一个π键,采取sp2杂化,如CH2 2等。
2等。
(3)形成两个π键,采取sp杂化,如CH≡CH、CO2等。
二、杂化轨道类型与分子空间结构的关系
1.杂化轨道用于形成σ键或用来容纳未参与成键的孤电子对。
(1)没有孤电子对:能量相同的杂化轨道彼此远离→形成的分子为对称结构。
(2)有孤电子对:孤电子对占据一定空间且对成键电子对产生排斥→形成的分子的空间结构发生变化。
2.杂化轨道与分子的空间结构的关系
(1)杂化轨道全部用于形成σ键
杂化类型 | sp | sp2 | sp3 |
轨道组成 | 一个ns和一个np | 一个ns和两个np | 一个ns和三个np |
轨道夹角 | 180° | 120° | 109°28' |
杂化轨道示意图 |
|
|
|
实例 | BeCl2 | BF3 | CH4 |
分子的空间结构 | | | |
(2)杂化轨道中有未参与成键的孤电子对
杂化类型 | sp2 | sp3 |
中心原子所在族 | 第ⅥA族 | 第ⅤA族 | 第ⅥA族 |
中心原子的孤电子对数 | 1 | 1 | 2 |
分子空间结构 | V形 | 三角锥形 | V形 |
实例 | SO2 | NH3、PCl3、PH3 | H2O、H2S |
CH4、NH3、H2O中心原子的杂化轨道类型都是sp3,键角为什么依次减小?从杂化轨道理论的角度比较键角大小。
1.正误判断
(1)杂化轨道的空间结构与分子的空间结构不一定一致( )
(2)杂化轨道间的夹角与分子内的键角一定相同( )
(3)凡AB3型共价化合物,其中心原子A均采用sp3杂化轨道成键( )
(4)NH3分子的空间结构为三角锥形,则氮原子的杂化方式为sp3( )
(5)C2H4分子中的键角都约是120°,则碳原子的杂化方式是sp2( )
2.下列分子的空间结构可用sp2杂化轨道来解释的是( )
①BF3②CH2 CH2③
CH2③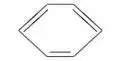 ④CH≡CH ⑤NH3⑥CH4
④CH≡CH ⑤NH3⑥CH4
A.①②③B.①⑤⑥C.②③④D.③⑤⑥
3.下列中心原子的杂化轨道类型和分子空间结构不正确的是( )
A.PCl3中P原子为sp3杂化,三角锥形
B.N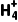 中N原子为sp3杂化,正四面体形
中N原子为sp3杂化,正四面体形
C.H2S中S原子为sp杂化,直线形
D.SO2中S原子为sp2杂化,V形
4.(2024·苏州高二检测)已知某XY2分子属于V形分子,下列说法正确的是( )
A.X原子一定是sp2杂化
B.X原子一定为sp3杂化
C.X原子上一定存在孤电子对
D.VSEPR模型一定是平面三角形
5.按要求回答下列问题:
(1)CH3COOH中C原子的杂化轨道类型是。
(2)醛基中碳原子的杂化轨道类型是_____________________________。
(3)化合物[H3O]+[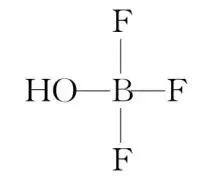 ]-中阳离子的空间结构为,阴离子的中心原子采取杂化。
]-中阳离子的空间结构为,阴离子的中心原子采取杂化。
(4)X的单质与氢气可化合生成气体G,G的水溶液的pH>7。G分子中X原子的杂化轨道类型是。
常见物质中心原子的杂化方式
(1)采取sp3杂化:有机物中饱和碳原子、NH3、H2O、金刚石中的碳原子、晶体硅中的硅原子、SiO2、N 等。
等。
(2)采取sp2杂化:有机物中的双键碳原子、BF3、石墨中的碳原子、苯环中的碳原子等。
(3)采取sp杂化:有机物中的三键碳原子、CO2、BeCl2等。
说明注意结构相似的物质,如CO2与CS2、BF3

通过网盘分享的文件:同步PPT课件等3个文件
链接: https://pan.baidu.com/s/1aX91ROOZJC0j7zSsZs4sQQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享