学习笔记(23):KEYNOTE‑B96研究开启铂耐药复发卵巢癌免疫治疗新篇章
- 2026-04-22 10:37:56

长期以来,卵巢癌被认为是典型的“免疫冷肿瘤”——肿瘤免疫原性低、免疫微环境抑制性强,免疫检查点抑制剂单药治疗疗效有限。在铂耐药复发卵巢癌这一预后极差的人群中,免疫治疗更是屡屡受挫,始终未能在III期随机研究中取得明确的生存获益。ENGOT-ov65/KEYNOTE-B961研究的发表,正在改变这一格局。这项全球多中心、随机、双盲III期研究首次证实,在每周紫杉醇(±贝伐珠单抗)的基础上联合PD-1抑制剂帕博利珠单抗,能够显著改善铂耐药复发卵巢癌患者的临床结局,标志着免疫治疗在这一“冷肿瘤”中的重要突破。该研究不仅为“免疫治疗 + 化疗 + 抗血管生成治疗”的协同机制提供了高质量循证医学证据,也为长期缺乏有效治疗选择的铂耐药复发卵巢癌人群,带来了具有临床实践意义的全新治疗策略。

研究设计
1.研究类型
全球多中心、随机、双盲、安慰剂对照 III 期研究
覆盖 25 个国家、187 家妇科肿瘤中心
注册并已完成的关键注册研究
2. 研究人群
铂耐药复发上皮性卵巢癌(含输卵管癌、原发腹膜癌)
既往 1–2 线系统治疗
ECOG 0–1
强调真实世界代表性与严格排除原发性铂难治人群
3.分组与分层
帕博利珠单抗+每周紫杉醇±贝伐珠单抗 vs 安慰剂+每周紫杉醇±贝伐珠单抗
按贝伐珠单抗使用、地区、PD-L1 CPS 分层
4. 治疗策略亮点
低剂量、每周紫杉醇作为免疫协同化疗骨架
允许联合抗血管生成治疗
免疫治疗支持延长用药与进展后继续治疗设计
5. 主要与关键次要终点
主要终点:无进展生存期
关键次要终点:总生存期,同时评估生活质量和患者报告结局
6.统计学设计
采用分层递进假设检验策略,并通过Mauer–Bretz图形法严格控制整体单侧 α=0.025。α 值预分配如下:
1)PD-L1 CPS ≥1 人群的无进展生存期(PFS):α=0.020
2)整体人群的无进展生存期(PFS):α=0.005
若PFS达到统计学显著性,α值顺延用于总生存期(OS),并按相同顺序先在 PD-L1 CPS ≥1 人群、再在整体人群中进行检验;
正式的 PFS 假设检验仅在第一次和第二次中期分析中进行;一旦在中期分析中跨越预设疗效界值,即视为主要终点达成,不再进行后续 α 控制下的 PFS 检验;
充分的事件数与中期分析设计,保证结论稳健性。

研究结果
1.研究人群与随访
共 643 例铂耐药复发卵巢癌患者随机入组 1)帕博利珠单抗 + 紫杉醇组:322 例 2) 安慰剂 + 紫杉醇组:321 例
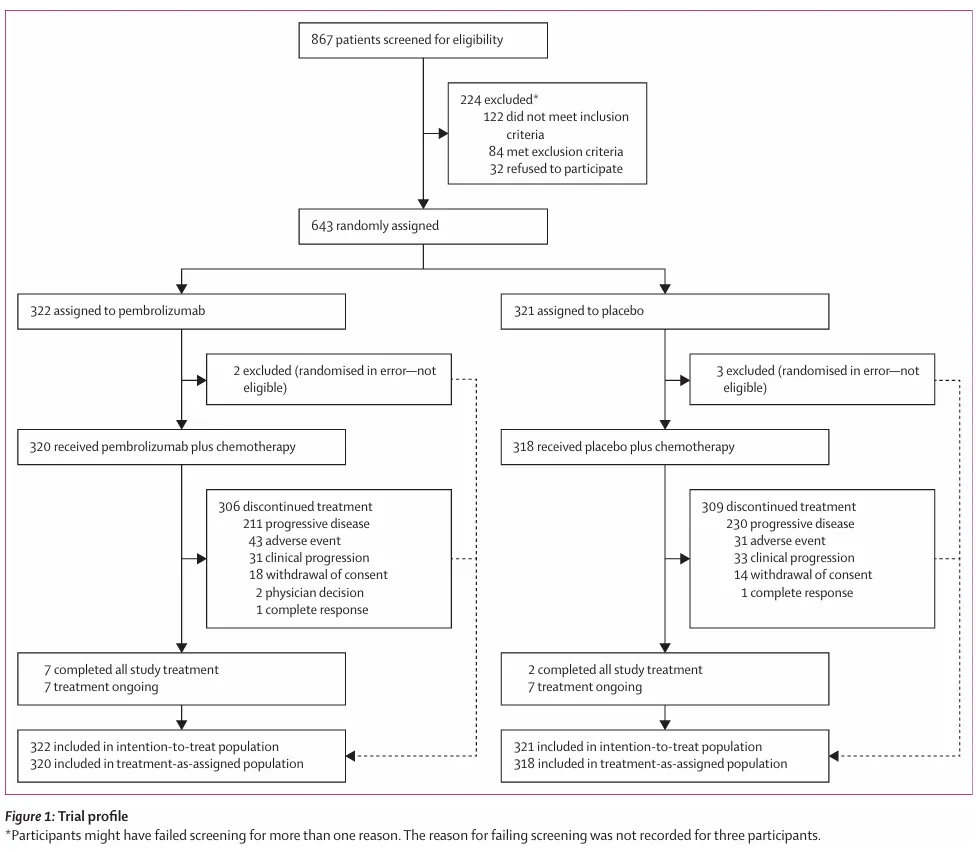
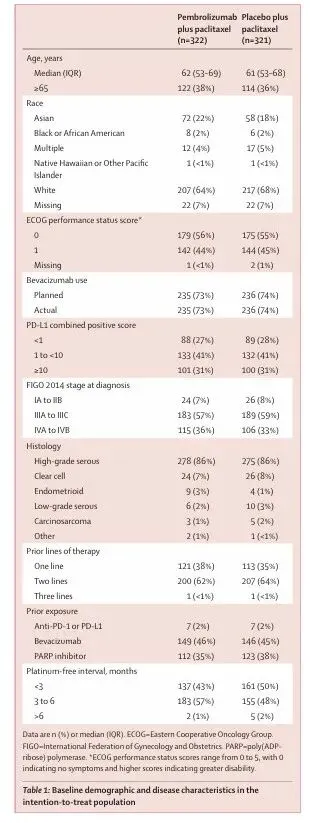
- 72%(466/643) 为 PD-L1 CPS ≥1
- 86%(553/643) 为高级别浆液性癌
- 73%(471/643) 预先计划联合贝伐珠单抗
既往治疗史与疾病侵袭性特征
1)63%(407/643) 既往已接受 2 线系统治疗
2)46%(295/643) 既往使用过 贝伐珠单抗
3)37%(235/643) 既往接受过 PARP 抑制剂治疗
4)2%(14/643) 既往接受过 PD-1/PD-L1 抑制剂
高度侵袭性的铂耐药特征
1)46%(298/643) 在最近一次含铂治疗后 <3 个月即出现疾病进展
2)53%(338/643) 在最近一次含铂治疗后 3–6 个月出现疾病进展
中位随访时间: 1)第一次中期分析:15.6 个月 2)第二次中期分析:26.6 个月 3)最终分析:32.7 个月
2. 主要终点:无进展生存期(PFS)——一次中期分析即成功
PD-L1 CPS ≥1人群:中位PFS=8.3 vs 7.2个月,HR=0.72(95%CI 0.58–0.89),P=0.0014
整体人群:中位PFS=8.3 vs 6.4个月,HR=0.70(95% CI 0.58–0.84),P <0.0001
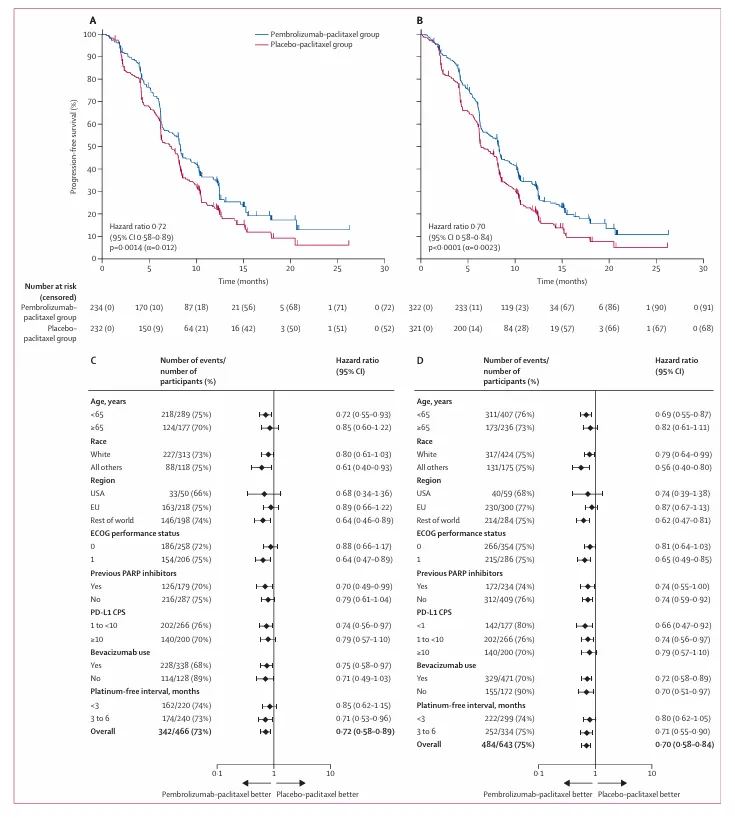
图 2:无进展生存期
(A) 在首次期中分析时,PD‑L1 CPS ≥1 人群的无进展生存期 Kaplan–Meier 估计。
(B) 在首次期中分析时,总体人群的无进展生存期 Kaplan–Meier 估计。
(C) PD‑L1 CPS ≥1 人群中,按照方案预先指定亚组的无进展生存期分析。
(D) 总体人群中,按照方案预先指定亚组的无进展生存期分析。
3. 关键次要终点:总生存期(OS)——冷肿瘤中的罕见突破
在第一次中期分析时,PD-L1 CPS≥1人群的总生存期尚未达到统计学显著改善(风险比 0.72,95% CI 0.55–0.94,P=0.0084,未达到预设 α 值),因此研究继续进入第二次中期分析。
PD-L1 CPS ≥1 人群(第二次中期分析):中位 OS=18.2 vs 14.0个月,HR 0.76(95% CI 0.61–0.94),P=0.0053(达到 α 控制标准)
整体人群(最终分析):中位 OS=17.7 vs 14.0 个月,HR=0.82(95% CI 0.69–0.97),P=0.011
属于少数在铂耐药卵巢癌 III 期研究中证实 OS 获益的免疫治疗方案
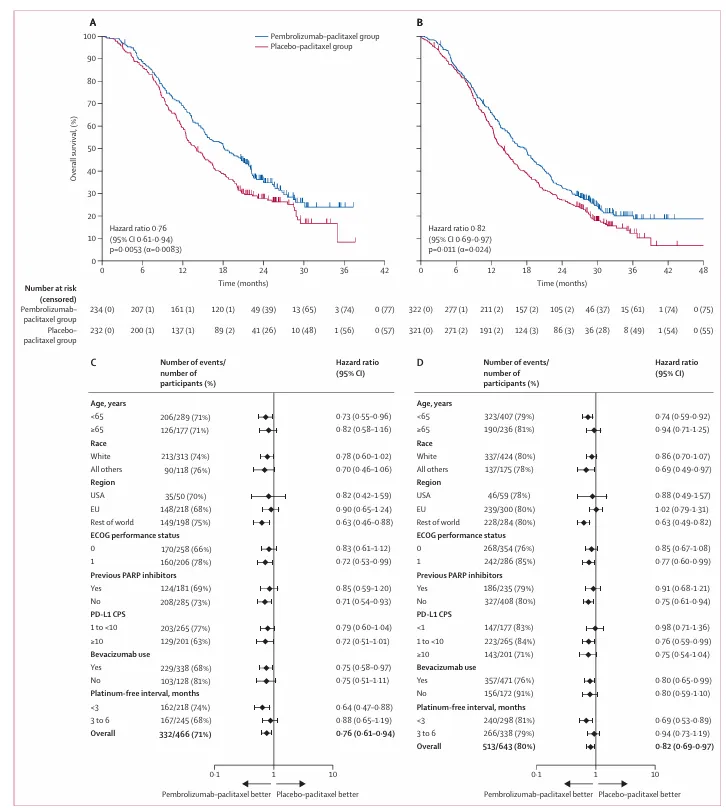
图 3:总生存期
(A) 在第二次期中分析时,PD‑L1 CPS ≥1 人群的总生存期 Kaplan–Meier 估计。
(B) 在最终分析时,总体人群的总生存期 Kaplan–Meier 估计。
(C) PD‑L1 CPS ≥1 人群中,按照方案预先指定亚组的总生存期分析。
(D) 总体人群中,按照方案预先指定亚组的总生存期分析。
4. 客观缓解率(ORR)与缓解深度
- ORR1)PD-L1 CPS ≥1 人群:ORR=53% vs 47%2)整体人群:ORR=50% vs 41%
- 中位缓解持续时间:1)PD-L1 CPS ≥1 人群:10.4 vs 8.1 个月 2)整体人群:10.4 vs 7.9 个月
缓解 ≥12 个月的比例: 1)PD-L1 CPS ≥1 人群:47% vs 30% 2)整体人群:47% vs 28%
5.治疗暴露与耐受性
中位治疗持续时间:32.5 周 vs 27.6 周 中位治疗周期数:6 个周期 vs 5 个周期
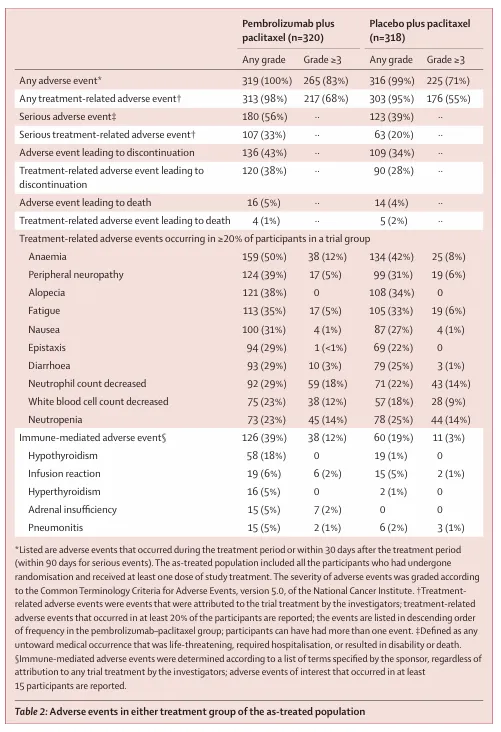
6. 安全性结果
≥3 级不良事件:83% vs 71% ≥3 级治疗相关不良事件:68% vs 55% 严重治疗相关不良事件:33% vs 20% 治疗相关死亡:1% vs 2% 免疫相关不良事件: 1)任意级别:39% vs 19% 2)3 级:12% vs 3% 3)免疫相关死亡:1%(仅见于联合组)
7.生活质量(PRO)
第 24 周 QLQ-C30 完成率:69% vs 58% 生活质量改善或稳定(≥10 分变化):59% vs 61% 腹部/胃肠道症状改善或稳定:74% vs 68% 疗效获益未以明显生活质量下降为代价

1.核心结论:冷肿瘤中免疫治疗的关键突破
ENGOT-ov65/KEYNOTE-B96 是首个 III 期随机研究,在铂耐药复发卵巢癌中证实免疫检查点抑制剂为基础的方案可显著改善总生存期 帕博利珠单抗联合每周紫杉醇(±贝伐珠单抗)显著改善 PFS 和 OS,获益具有明确的临床意义 疗效在PD-L1 CPS≥1和整体人群中均可观察到
2. PD-L1 的价值与局限:既是富集标志物,也并非唯一决定因素
- PD-L1 CPS≥1人群的OS获益幅度更大,支持其作为患者富集策略,但在整体人群中,不同 CPS 分层的HR 均一致倾向于帕博利珠单抗,说明:
1) PD-L1 作为卵巢癌预测性生物标志物的复杂性 2)免疫疗效还受到肿瘤生物学特征和宿主免疫状态等多重因素影响 强调未来需要更精细的免疫预测标志物
与既往失败的 III 期研究不同:本研究采用每周(节律性)紫杉醇 每周紫杉醇具有免疫调节作用: 1)增强抗原呈递 2)调控抗原呈递过程以及免疫抑制性细胞群,从而增强抗肿瘤免疫反应 既往探索性分析亦提示:免疫治疗+每周紫杉醇 > + 脂质体多柔比星 不同研究间差异还可能:试验设计、入组人群、PD-1vsPD-L1通路抑制差异
优势:
1)对照方案采用当前最活跃的标准治疗(每周紫杉醇 ± 贝伐珠单抗)
2) 提供高度临床相关的比较基础
局限
1)贝伐珠单抗由研究者选择,可能受患者或疾病特征的影响导致偏倚;
2)研究并非为评估贝伐珠单抗独立贡献而设计,无法仅基于本研究数据明确界定贝伐珠单抗在该联合方案中的具体作用;
3)仅纳入≤2 线治疗患者,对更重度治疗人群外推有限;
4)既往 PARP 使用率受全球实践差异影响;

1.Pembrolizumab plus weekly paclitaxel in platinum-resistant recurrent ovarian cancer (ENGOT-ov65/KEYNOTE-B96): a multicentre, randomised, double-blind, phase 3 study;Lancet 2026; 407: 1525–1537

