重症脑出血的临床管理学习笔记:从急会诊到共享决策的深度整合
- 2026-04-17 19:08:45
这份笔记将从急会诊到日常管理的全链条,进行系统性的梳理、整合与深化。
仅为个人学习梳理,不构成医疗或指导建议。
一、急会诊处理:黄金时间的“作战地图”
急会诊的核心是快速稳定、精准评估、明确去向。流程应高度结构化,避免遗漏。
1.初级评估(ABCDE,<1分钟):
–A(气道):立即评估气道通畅性。昏迷(GCS≤8)、呕吐、咽喉反射消失者,立即准备气管插管。强调“任何原因造成的中枢神经系统抑制,足以影响气道及保护性反射”是ICU收治的明确指征。
–B(呼吸):观察呼吸频率、节律、氧饱和度。出现陈-施呼吸[注解见文末]、中枢性过度通气或呼吸衰竭,预示脑干受压,需紧急处理并准备呼吸支持。
–C(循环):快速测量血压、心率。高血压是脑出血的因果双刃剑,需立即控制,但避免骤降。目标通常为收缩压140-160 mmHg。出现休克征象,需排查合并损伤或严重并发症。
–D(神经功能快速评估):
•GCS评分:≤8分为重症明确标志。
•瞳孔:不等大、对光反射消失提示脑疝。
•脑干体征:检查眼动、角膜反射、肢体对疼痛的反应(去脑/去皮质强直)。
–E(暴露与查体):快速查体寻找外伤迹象、脑膜刺激征等。
2.次级评估与紧急干预(5-10分钟):
–建立监测与通路:心电监护、末梢氧饱和度,建立两条静脉通路(避免在瘫痪侧 当然深静脉得用双腔)。
–紧急降颅压:对于有脑疝征象者,立即给予20%甘露醇(0.5-1.0 g/kg)或高渗盐水快速静滴。同时抬高床头30°。
–控制血压:使用可滴定、短效的静脉降压药(如乌拉地尔、尼卡地平)。
–完善关键检查:急查头颅CT(明确出血量、部位、破入脑室情况、中线移位)、血常规、凝血功能、电解质、血糖、动脉血气等。
3.会诊决策输出(明确三件事):
–诊断与严重性:明确“重症脑出血”及可能病因(高血压性?血管畸形?)。
–紧急处理是否完成:气道、颅压、血压是否初步稳定。
–去向建议:必须明确是否收入ICU。依据下述收治指征,结合医院流程,向家属和病房清晰传达。
二、ICU收治指征:基于“优先度模型”的决策
ICU收治不仅看单一指标,更基于 “患者是否能从ICU的严密监测和器官支持中明确获益”的核心原则。可应用美国危重病医学学会的优先度模型进行决策:
•优先度1(最应收入):病情不稳定,需要ICU特有且无法在普通病房进行的加强治疗与监测。
–对应重症脑出血的明确指征:
1.高级呼吸支持:需要机械通气(如GCS≤8,气道保护能力丧失);或呼吸功能迅速恶化需立即插管。
2.循环支持:需要血管活性药物维持血压(如合并神经源性休克或严重感染)。
3.神经系统监测与支持:任何原因导致的意识障碍(GCS评分显著下降)影响气道;或需要进行有创颅内压监测。
4.多器官支持:≥2个器官系统需要上述支持。
•优先度2(通常收入):需要密切监测且可能需要立即干预。
–对应指征:出血量大(幕上≥30ml,幕下≥10ml)或位于关键部位(脑干、丘脑),虽目前生命体征尚平稳,但病情进展风险极高,需在ICU进行连续神经功能评估和随时干预。
•不适宜收治(优先度4):慢性消耗性疾病终末状态、不可逆的严重颅脑损伤(如大量脑出血伴脑疝时间过长已致脑死亡)、患者/家属明确拒绝积极治疗等。此决策需谨慎,并应由ICU主任参与。
实操锚点:对于脑出血,只要符合以下一条,应强烈建议收治ICU:
1.GCS评分≤12分或进行性下降。
2.出现脑干受压或脑疝的临床表现(瞳孔不等大、呼吸节律异常、去脑强直)。
3.出血破入脑室系统,引起急性梗阻性脑积水。
4.需要紧急手术干预(血肿清除、去骨瓣减压、脑室引流)。
5.合并严重的内科并发症(如神经源性肺水肿、严重电解质紊乱)。
三、日常查房与临床实操:结构化与个体化的融合
ICU查房必须高效、全面、以患者为中心。可整合 “五环节架构”和“核查清单”思维。
1.查房前准备(信息结构化采集):
–一线医生:完成“一页式摘要”,梳理时间线:何时发病→如何加重→已做干预→当前问题。
–多学科信息:护士(生命体征趋势、出入量、护理问题)、药师(用药合理性、不良反应)、康复师(肢体功能、吞咽评估)、营养师(营养状态与方案)。
2.床旁查房与评估(遵循固定范式):
–汇报与补充:管床医生简洁汇报,主治医生补充关键点。
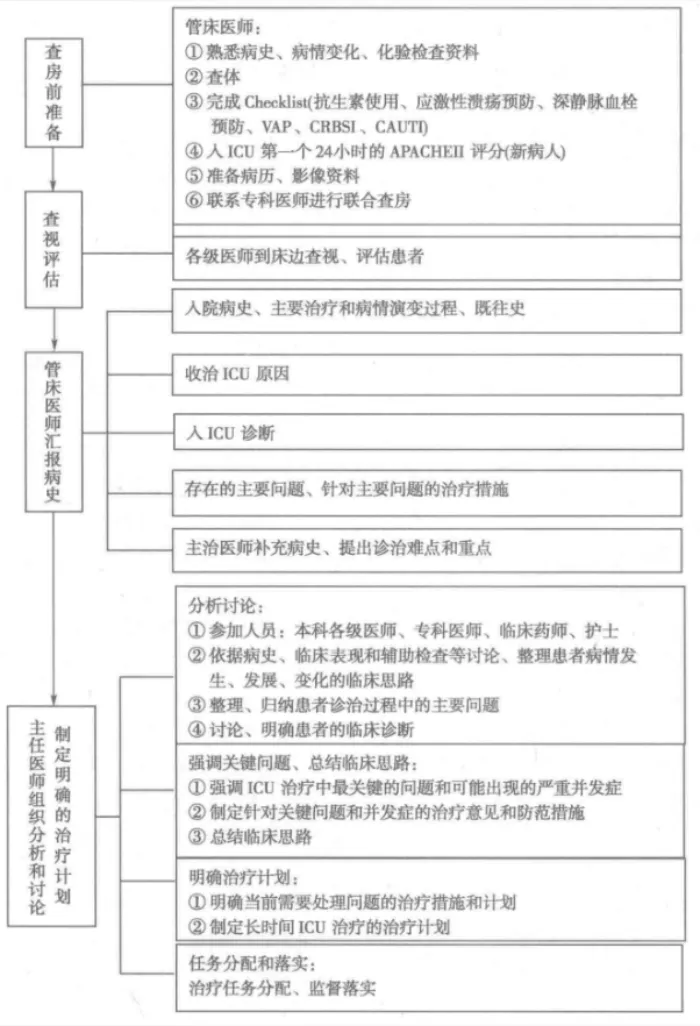
–重点体格检查:
•神经系统:GCS评分、瞳孔、脑干反射、肢体肌力与张力、病理征。这是脑出血患者查房的核心。
•全身评估:心肺听诊(排查肺炎、肺水肿)、腹部(肠鸣音、应激性溃疡迹象)、皮肤(压疮、水肿)、所有导管部位。
•设备与数据:核对呼吸机参数(若使用)、输液泵药物、监护仪趋势(血压、心率、氧合)。
–数据审查:当日血气分析、电解质、血常规、影像学(必要时床旁超声评估视神经鞘直径以无创评估颅压)。
3.临床实操关键细节:
–血压管理:是每日查房必议事项。依据指南设定个体化目标(如收缩压130-140 mmHg),并评估其与脑灌注、肾功能平衡。
–颅内压管理:不仅是脱水剂使用。需综合评估:床头角度、镇静深度、疼痛控制、体温、二氧化碳分压(PaCO₂)、电解质平衡。避免过度脱水导致肾前性损伤。
–气道与呼吸:每日评估自主呼吸试验(SBT)条件,尽早脱机。加强气道湿化与口腔护理,预防VAP。
–并发症预防集束化治疗:
•深静脉血栓预防:在出血稳定后(通常24-48小时),如无禁忌,应启动药物预防(低分子肝素)联合机械预防。
•应激性溃疡预防:使用质子泵抑制剂或H2受体阻滞剂。
•早期康复:一旦生命体征平稳,即开始被动活动、体位管理,预防挛缩和ICU获得性衰弱。
四、鉴别诊断与临床决策锚点
1.超越“高血压性脑出血”的鉴别诊断(避免锚定效应):
–血管结构性:动静脉畸形、动脉瘤、海绵状血管瘤、烟雾病。线索:年轻患者、无高血压史、脑叶出血、CT上异常血管影或钙化、SAH混合成分。
–肿瘤性:原发或转移性肿瘤卒中。线索:出血灶周围异常水肿、多发病灶、非急性期影像可见强化结节。
–凝血障碍性:抗凝/抗血小板药物过量、血友病、DIC。线索:用药史、全身出血倾向、凝血功能严重异常。
–其他:脑血管炎、静脉窦血栓、可逆性脑血管收缩综合征。
2.临床决策核心锚点:
–治疗决策的“北极星”:患者的治疗目标与预后价值。在查房时,应不断追问(如南医重症的“五连问”精神):“我们当前的所有支持,是为了达到什么目标?是否符合患者本人的价值观?”
–手术决策的锚点:不仅看血量,更看“效应”。小脑出血10ml引起脑积水,手术指征强于壳核30ml但意识清楚者。核心指征是:神经功能恶化、脑干受压、颅高压药物难以控制。
–撤机与拔管锚点:神经功能恢复是前提。需评估意识水平、咳嗽反射、吞咽功能,而不仅仅是血气指标。
五、诊疗计划与依据:从问题清单到循证方案
每日查房后,应形成清晰的诊疗计划:
1.问题清单:按优先级列出,如:① 颅内高压;② 高血压;③ 潜在肺炎;④ 低钠血症。
2.对应计划:
–针对①:继续甘露醇q8h,监测血浆渗透压;维持床头30°;控制体温。
–针对②:静脉泵入尼卡地平,目标收缩压140-150mmHg。
–针对③:完善痰培养,经验性抗感染,加强翻身拍背。
–依据:每条计划后注明简要依据,如“依据《脑出血诊疗指南》”、“依据药敏结果”。
3.设定目标与时限:如“24小时内控制收缩压于目标范围”、“48小时后复查头颅CT评估血肿及水肿情况”。
六、思维进阶与认知偏误防范
重症医学是认知战。必须主动识别和规避偏误:
•锚定效应:切勿因“高血压病史”就停止寻找其他出血原因,特别是病情不典型时。
•确认偏误:不要只关注支持“脑出血”诊断的证据,而忽略新发的发热可能是感染而非中枢性高热。
•从众效应:在上级医生查房时,要敢于基于自己掌握的床旁细节提出不同见解。
•损失厌恶:当一种降压或脱水方案效果不佳时,要勇于及时调整,不要因为已使用多日而拒绝改变。
•应对策略:每日查房时,进行“认知复盘”:我们最初的诊断是否仍能解释所有新情况?是否有被忽略的相反证据?
七、前沿进展整合
将新证据融入日常思考:
•微创手术:对比传统开颅,内镜或立体定向穿刺血肿清除术的适应症与时机。
•脑氧与多模态监测:对于重症患者,有创颅内压、脑组织氧分压监测如何指导个体化治疗。
•靶向治疗:针对血肿周围水肿的机制(如铁离子过载),探讨去铁胺等药物的潜在角色(虽尚处研究阶段)。
•人工智能:AI辅助的CT血肿体积自动测量、水肿带预测、预后模型。
八、患者沟通与共享决策
这是现代重症医学的伦理核心。
1.早期沟通,建立信任:入院即与家属充分沟通病情的严重性、不确定性及治疗路径。
2.运用“了解我”(Get to Know Me)工具:了解患者的职业、爱好、价值观。这不仅体现人文关怀,更能为后续决策(如是否进行有创手术或生命支持)提供至关重要的背景。
3.预后沟通与目标设定:基于客观数据(如出血量、部位、年龄、并发症)和临床经验,坦诚沟通可能的预后范围(功能恢复、残疾、植物状态、死亡)。在病情转折点,引导家属思考“如果患者自己能表达,他/她会如何选择?”。
4.多学科家庭会议:在重大决策(如是否手术、是否放弃积极治疗)前,组织医生、护士、社工共同与家属沟通,确保信息一致,支持家属决策。
总结:对重症脑出血的管理,是一个将“标准化流程”(急会诊、查房、集束化护理)与“个体化精准决策”(基于解剖、生理、患者价值观)深度融合的过程。它要求临床医生既是一名熟练运用清单和指南的“技师”,更是一名能整合多维信息、洞察认知陷阱、并引导人文伦理决策的“战略家”。通过上述维度的系统整合,我们的临床思维将从处理“一个疾病”升维至管理“一个处于危机中的完整的人及其家庭”。
相关学习:
颅脑损伤下PaCO₂与瞳孔大小变化的生理机制整合解析,一文读懂
ICU急会诊快速鉴别策略:基于VINDICATE的加权排查法
知识库分享:

附注:
陈-施呼吸(Cheyne-Stokesrespiration,CSR)是一种周期性呼吸模式,表现为呼吸幅度与频率逐渐增强(crescendo)后又逐渐减弱(decrescendo),并在每个周期末端伴随规律性的呼吸暂停(apnea);其本质是呼吸反馈控制系统不稳定导致的振荡,常见触发机制为短暂过度通气使PaCO₂降至呼吸暂停阈值以下,引发中枢性呼吸暂停,随后PaCO₂回升再次驱动通气,形成循环。
呼吸波形特征与识别要点
·典型周期构成:低通气/浅慢→渐强渐快→过度通气→中枢性呼吸暂停,随后进入下一个周期。
·时间尺度:成人常见为20–30秒过度通气期交替10–40秒中枢性呼吸暂停。
·关键鉴别点:呼吸暂停期通常为中枢性(呼吸努力消失/降低),而非阻塞性(上气道塌陷但仍有呼吸努力)。
发生机制的临床理解框架
1)控制论解释:环路增益(loopgain)过高导致“过冲-欠冲”
·环路增益(loopgain):代表呼吸控制系统对扰动的反应幅度;当loopgain>1时,系统易失稳并产生振荡。
·组成要素:
·控制器增益(controllergain):化学感受器敏感性(对CO₂变化反应过强)。
·植物增益(plantgain):通气改变引起血气变化的程度(受基础PaCO₂、肺容量等影响)。
·反馈增益(feedbackgain):信号传递速度,主要由循环时间(cardiacoutput决定)决定;心衰时循环延迟延长,促进振荡。
2)CO₂储备变窄与呼吸暂停阈值上移
·CO₂储备(CO₂reserve):清醒期PaCO₂与睡眠期呼吸暂停阈值之间的差值;该储备越窄,越容易因轻微通气波动使PaCO₂跨越阈值而诱发中枢性呼吸事件。
·心衰情境下:肺淤血刺激肺J受体等导致慢性轻度过通气、PaCO₂偏低,同时化学感受器敏感性增高,使CO₂储备变窄并提高呼吸暂停阈值,从而更易发生CSR。
3)时间延迟放大振荡
·从肺泡通气改变到动脉血气变化被中枢感知存在循环延迟;延迟越大,越容易出现“纠正过度—再反向纠正”的振荡,最终形成CSR极限环。
临床定位价值与常见病因谱
·神经重症语境下的定位意义有限:CSR可见于双侧大脑半球或间脑病变,但也可由代谢性脑病等弥漫性损伤诱发,因此不能作为特异性脑干受压体征;真正提示脑干受压风险更高的是Biot呼吸/共济失调呼吸等。
·更常见的病因组合:
·心力衰竭:CSR/CSA在慢性心衰中常见(约30%–50%),并与严重程度相关。
·卒中:可出现CSR,但并不指示卒中解剖部位。
·肾衰、阿片长期使用、高海拔等亦可出现相关中枢性呼吸暂停模式。
与“脑干受压”相关呼吸异常的区分要点
呼吸模式 | 关键特征 | 更支持的定位/病因线索 |
陈-施呼吸(CSR) | 渐强-渐弱+周期性中枢性呼吸暂停 | 心衰、卒中、肾衰等;定位价值差 |
Biot呼吸 | 规则呼吸中突然出现呼吸暂停,或“几口同深浅呼吸+突然暂停”的混乱模式 | 提示延髓/低位脑桥呼吸节律中枢受损 |
中枢性过度通气 | 持续过度通气(低PaCO₂),常伴多种全身因素 | 定位价值差;需排查缺氧、感染、酸中毒、药物毒性等 |
监测与床旁判读要点
·观察重点:除呼吸频率外,应关注呼吸幅度是否呈周期性起伏以及是否存在规律性呼吸暂停。
·氧饱和度解读:CSR可在呼吸暂停期出现氧合下降,但部分病例在心源性CSR中可见“呼吸暂停期SpO₂反而较高”的现象,提示并非所有CSR都必然伴随明显发绀。
