
[核心素养发展目标] 1.掌握氧化还原反应方程式配平的依据,学会配平氧化还原反应方程式的一般步骤。2.掌握配平氧化还原反应方程式的常用技巧。
一、正向配平氧化还原反应方程式的依据及步骤
1.氧化还原反应方程式配平的依据
(1)得失电子守恒:氧化剂和还原剂得失电子总数相等,化合价__________=化合价__________。
(2)质量守恒:反应前后元素的__________和原子的__________不变。
(3)电荷守恒(离子方程式):反应前后电荷总数不变。
2.氧化还原反应方程式配平的一般步骤
以H2O2+H2CrO4——O2↑+Cr(OH)3↓+H2O为例
(1)标价态:标出发生氧化反应和还原反应的元素的化合价。
H2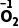 +H2
+H2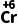 O4——
O4——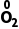 ↑+
↑+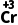 (OH)3↓+H2O
(OH)3↓+H2O
(2)列变化:标出反应前后元素化合价的变化,分析“1分子氧化剂→还原产物”化合价降低数值,“1分子还原剂→氧化产物”化合价升高数值。
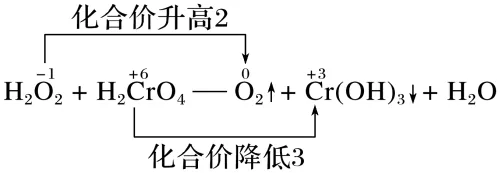
(3)求总数:配出氧化剂、还原剂及氧化产物和还原产物的化学计量数。
计算化合价升高总数与降低总数的最小公倍数为6,使化合价升高和降低的总数相等,即得失电子守恒。“×”后面的数字就是反应物或生成物的化学计量数。
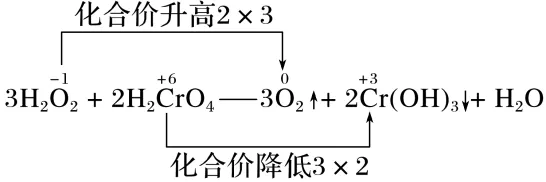
(4)根据原子守恒配平其他物质的化学计量数。
3H2O2+2H2CrO4——3O2↑+2Cr(OH)3↓+2H2O
(5)查守恒:原子个数是否守恒,配平后,把单线改成长等号,标注反应条件。
3H2O2+2H2CrO4 2↑+2Cr(OH)3↓+2H2O
2↑+2Cr(OH)3↓+2H2O

1.配平下列化学方程式。
(1)__________Mg+__________CO2
(2)__________Na2SO3+__________KIO3+__________H2SO4 2SO4+__________K2SO4+__________I2+__________H2O
2SO4+__________K2SO4+__________I2+__________H2O
2.运动会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生的化学反应为KClO3+PP2O5+KCl(未配平)。下列有关该反应的叙述正确的是( )
A.氯酸钾被氧化
B.反应中每生成1个P2O5时,转移5个电子
C.单质P被还原,发生还原反应
D.配平后反应的化学方程式为5KClO3+6P3P2O5+5KCl
二、配平氧化还原反应方程式的常用技巧
题型1 逆向配平法
分解反应、歧化反应、部分氧化还原反应,一般使用逆向配平的方法,即先从氧化产物和还原产物开始配平。
例1 __________S+__________KOH__________K2S+__________K2SO3+__________H2O
分析
硫单质既是氧化剂又是还原剂,K2S是__________产物,K2SO3是__________产物。
(1)化合价的变化,生成“1个K2S”化合价__________价,生成“1个K2SO3”化合价__________价,化合价变化的最小公倍数为__________,因而K2S化学计量数为__________,K2SO3的化学计量数为__________。
(2)根据S原子守恒确定单质硫的化学计量数为__________。
(3)再根据K原子守恒配出KOH的化学计量数为__________。
(4)最后定H2O的化学计量数为__________。

1.一定条件下,硝酸铵受热分解的化学方程式(未配平)为NH4NO3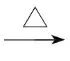 3+N2↑+H2O,下列说法错误的是( )
3+N2↑+H2O,下列说法错误的是( )
A.配平后H2O的系数为6
B.NH4NO3既是氧化剂又是还原剂
C.该反应既是分解反应也是氧化还原反应
D.氧化产物和还原产物的质量之比为5∶3
题型2 离子方程式的配平
首先根据得失电子守恒和原子守恒配平氧化剂、还原剂和氧化产物、还原产物,根据电荷守恒,配平离子方程式两边电荷数,最后根据原子守恒配平未变价元素的原子。
例2 __________Mn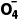 +__________H++__________H2O2
+__________H++__________H2O2 2++__________O2↑+__________H2O
2++__________O2↑+__________H2O
分析
先根据得失电子守恒确定氧化剂Mn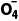 、还原剂H2O2、还原产物Mn2+、氧化产物O2的化学计量数分别是__________、__________、__________、__________;根据电荷守恒确定H+的化学计量数为__________,根据H原子守恒确定H2O的化学计量数为__________,最后用O原子守恒检验。
、还原剂H2O2、还原产物Mn2+、氧化产物O2的化学计量数分别是__________、__________、__________、__________;根据电荷守恒确定H+的化学计量数为__________,根据H原子守恒确定H2O的化学计量数为__________,最后用O原子守恒检验。

2.(2023·湖北孝感一中高一期中)已知在碱性条件下,发生反应:Fe3++ClO-+OH-
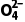 +Cl-+H2O(未配平)。
+Cl-+H2O(未配平)。
(1)Fe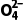 中铁元素化合价为__________。
中铁元素化合价为__________。
(2)Fe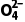 是__________(填“氧化”或“还原”)产物。
是__________(填“氧化”或“还原”)产物。
(3)配平该离子方程式:__________。
题型3 缺项配平类[一般缺的为酸(H+)、碱(OH-)、水]
(1)先将得失电子数配平,再观察两边电荷。若反应物这边缺正电荷,一般加H+,生成物一般加水;若反应物这边缺负电荷,一般加OH-,生成物一般加水,然后根据两边电荷数进行配平。
(2)当化学方程式中有多个缺项时,应根据化合价的变化找准氧化剂、还原剂、氧化产物、还原产物。
例3 __________Mn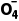 +__________I-+____________________Mn2++__________I2+__________H2O
+__________I-+____________________Mn2++__________I2+__________H2O

3.已知离子方程式:As2S3+H2O+N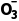

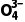 +S
+S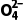 +NO↑+__________(未配平),下列说法错误的是( )
+NO↑+__________(未配平),下列说法错误的是( )
A.配平后H2O的化学计量数为4
B.反应后溶液呈酸性
C.配平后氧化剂与还原剂的化学计量数之比为3∶28
D.氧化产物为As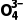 和S
和S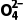


通过网盘分享的文件:【学生用书Word版文档】 整本等5个文件
链接: https://pan.baidu.com/s/15FiK8RTPyvbiSWACNxFztg?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享